Przeczytaj
E‑materiały powiązane z tematem
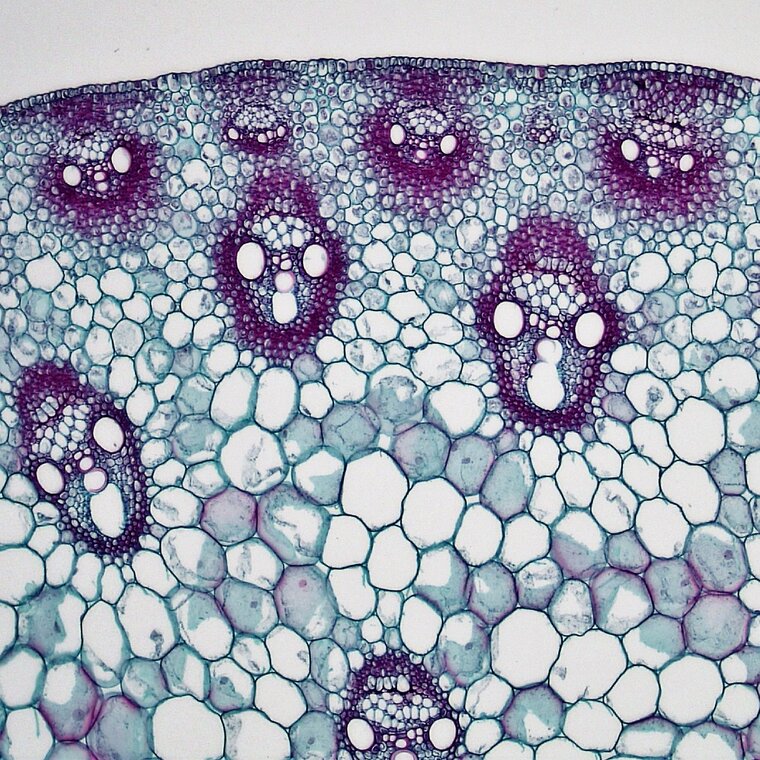
Obserwacja mikroskopowa tkanek roślinnych
Do obserwacji struktur tkankowych i komórkowych używa się głównie mikroskopów (z gr. mikros – mały, skopeo – patrzę, obserwuję) – przyrządów optycznych pozwalających na otrzymywanie powiększonych obrazów obiektów niewidocznych gołym okiem. Najczęściej stosowanym mikroskopem do obserwacji tkanek roślinnych jest mikroskop świetlny, który wykorzystuje wiązkę światła przechodzącą przez specjalny układ optyczny, tworzony przez zestaw soczewek umieszczonych w obiektywie i okularze.
Taka obserwacja jest jednak utrudniona, gdyż komórki i ich elementy nie wykazują różnic w absorpcji promieniowania elektromagnetycznego. Przekłada się to na brak wyraźnego kontrastu między poszczególnymi elementami. Nie ma więc możliwości rozróżnienia szczegółów budowy danej tkanki czy też elementów komórki. Z tego powodu w preparatach mikroskopowych niezbędne jest zastosowanie barwników histologicznych, które wybarwiają komórki wraz z ich elementami strukturalnymi, a tym samym umożliwiają ich dokładną obserwację i identyfikację.
Barwniki histologiczne
Barwniki histologiczne to związki chemiczne wykorzystywane w mikroskopii świetlnej do wybarwiania struktur komórkowych i tkankowych. Typowy barwnik zawiera dwie grupy chemiczne: chwytną i barwną. Część chwytna łączy się z elementami komórkowymi o określonym składzie chemicznym, natomiast barwna absorbuje światło o określonej długości fali, dzięki czemu możliwe jest dostrzeżenie wybarwionych struktur.
W zależności od struktury, jaką się będzie obserwować, należy zastosować odpowiedni barwnik histologiczny. Do wykrywania amyloplastów, czyli leukoplastów magazynujących skrobię, stosuje się jodek w jodku potasu, który barwi skrobię na kolor od jasnoniebieskiego do granatowego. Celulozowe ściany komórkowe wykrywa się za pomocą roztworu chlorku cynku z jodem, pod wpływem którego ściany komórkowe zbudowane z celulozy wybarwiają się na kolor fioletowy. Ściany komórkowe inkrustowane ligniną po zastosowaniu floroglucyny z kwasem solnym barwią się na kolor czerwony. Natomiast ściany komórkowe adkrustowane suberyną pod wpływem sudanu III nabierają barwy żółtoczerwonej.
Barwienie różnicowe
Aby odróżnić od siebie poszczególne struktury komórkowe i tkankowe, dany preparat należy potraktować jednocześnie dwoma różnymi barwnikami – jest to tzw. barwienie różnicowe. Dzięki tej technice można odróżnić m.in. zdrewniałe ściany komórkowe, które pod wpływem safraninysafraniny barwią się na kolor czerwony, od celulozowych ścian komórkowych, które pod wpływem zieleni świetlistej barwią się na kolor niebieskozielony. Innym przykładem barwników stosowanych w barwieniu różnicowym są: karmin ałunowy, barwiący ściany celulozowe na kolor czerwony, oraz zieleń metylenowa, barwiąca zdrewniałe ściany komórkowe na kolor zielony.
Hematoksylina i eozyna
Najczęściej stosowanymi barwnikami w histologii są hematoksylinahematoksylina oraz eozynaeozyna (H+E).
Hematoksylina to niebieski barwnik, którym wykrywa się kwasowe (zasadochłonne) elementy komórki, takie jak jądro komórkowe czy siateczka śródplazmatyczna szorstka. Zazwyczaj stosowana jest w połączeniu z eozyną.
Eozyna to kwasowy barwnik o czerwonej barwie służący do wykrywania zasadowych (kwasochłonnych) struktur komórkowych, takich jak cytoplazma.
Jak przygotować preparat mikroskopowy z łodygi?
Ilustracja przedstawia przygotowanie preparatu mikroskopowego z łodygi. Na szkiełko podstawowe nanieś zakraplaczem kroplę wody. Na ilustracji jest szkiełko podstawowe, na które zakraplaczem naniesiono kroplę wody. Za pomocą skalpela lub żyletki odetnij cienki fragment łodygi, a następnie umieść go w kropli wody. Na ilustracji jest żyletka. Prowadzi od niej strzałka do zielonej łodygi. Wykorzystując igłę laboratoryjną, rozłóż równo odcięty fragment. Na ilustracji jest szkiełko podstawowe. Na nim za pomocą igły laboratoryjnej w naniesionej kropli wody zostaje umieszczony odcięty fragment łodygi. Ustaw szkiełko nakrywkowe pod kątem 30° w stosunku do szkiełka podstawowego, a następnie delikatnie połóż je na preparacie. Sprawdź, czy nie powstały pęcherze powietrza między szkiełkiem podstawowym a nakrywkowym. Jeśli powstały, spróbuj je usunąć lub wykonaj preparat ponownie. Na ilustracji preparat na szkiełku podstawowym z fragmentem łodygi zostaje przykryty za pomocą pęsety szkiełkiem nakrywkowym. Zostaje sprawdzone drugim szkiełkiem nakrywkowym, czy między szkiełkiem podstawowym a nakrywkowym nie znajdują się pęcherze.
Podczas przygotowywania preparatu istnieje ryzyko pojawienia się artefaktówartefaktów, np. pęcherzyków powietrza. Jest to bardzo częste zjawisko towarzyszące samodzielnemu sporządzaniu preparatów. Duża liczba artefaktów uniemożliwia przeprowadzenie obserwacji mikroskopowych. W takiej sytuacji należy spróbować usunąć pęcherzyki powietrza poprzez delikatne ruchy góra‑dół, lewo‑prawo szkiełka nakrywkowego lub wykonać preparat na nowo.
Barwienie hematoksyliną i eozyną
Procedura barwienia
Naklejone i odparafinowane skrawki nawodnij w szeregu alkoholowym.
Umieść skrawki na 2–3 minuty w wodzie destylowanej.
Zanurzaj skrawki przez 4–5 minut w roztworze hematoksylinyhematoksyliny (im starszy barwnik, tym krócej).
Przebarwione skrawki odbarw przez 2–3 sekundy w zakwaszonym alkoholu (0,25 ml HCl na 100 ml alkoholu 70%).
Przepłucz preparat pod bieżącą wodą lub umieść w wodzie z kilkoma kroplami nasyconego roztworu węglanu litu, aż do uzyskania niebieskiego zabarwienia jąder komórkowych (kontrola pod mikroskopem lub do widocznej makroskopowo zmiany zabarwienia skrawka).
Zanurz skrawki w roztworze eozynyeozyny przez 1 minutę.
Przepłucz wodą destylowaną.
Zamknij skrawek w medium na bazie wody (np. glicerożelatyna).
Wyniki barwienia
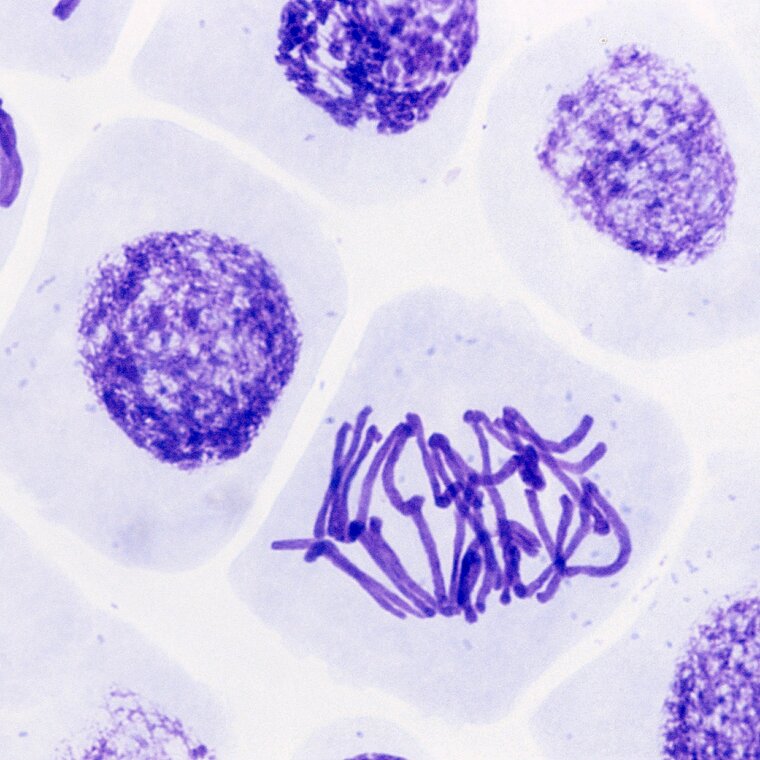
Elementy zasadochłonne (np. jądra komórkowe) barwią się na niebiesko, a elementy kwasochłonne na czerwono.
Jądra komórkowe (chromatyna): barwa niebieska
Cytoplazma: barwa różowa
Barwienie safraniną z zielenią trwałą
Przygotowanie roztworu do barwienia
Dodaj 20 mg safraninysafraniny w proszku do zlewki o pojemności 100 ml.
Wlej 20 ml wody destylowanej do zlewki i przez ciągłe mieszanie przygotuj 0,1‑procentowy roztwór barwiący safraniny.
Przenieś 20 mg zieleni trwałejzieleni trwałej do innej zlewki o pojemności 100 ml.
Dodaj do niej 20 ml wody destylowanej i przygotuj 0,1‑procentowy roztwór barwiący.
Przefiltruj oba roztwory barwiące.
Przygotowanie szkiełek do obserwacji
Nawodnij preparaty po deparafinizacji (przeprowadź przez szereg alkoholowy, zanurzając je kolejno w alkoholu: 99,8%, 90%, 80%, 70% i 50%, a następnie w wodzie).
Zanurz skrawki w 0,1‑procentowym roztworze zieleni trwałej na 5–10 minut.
Przepłucz szkiełka 0,1‑procentowyn kwasem octowym przez 10–15 sekund.
Zanurz szkiełka w 0,1‑procentowym roztworze safraniny na 20–30 minut.
Wyczyść i odwodnij szkiełka (odwodnienie w etanolu 95% i 100%).
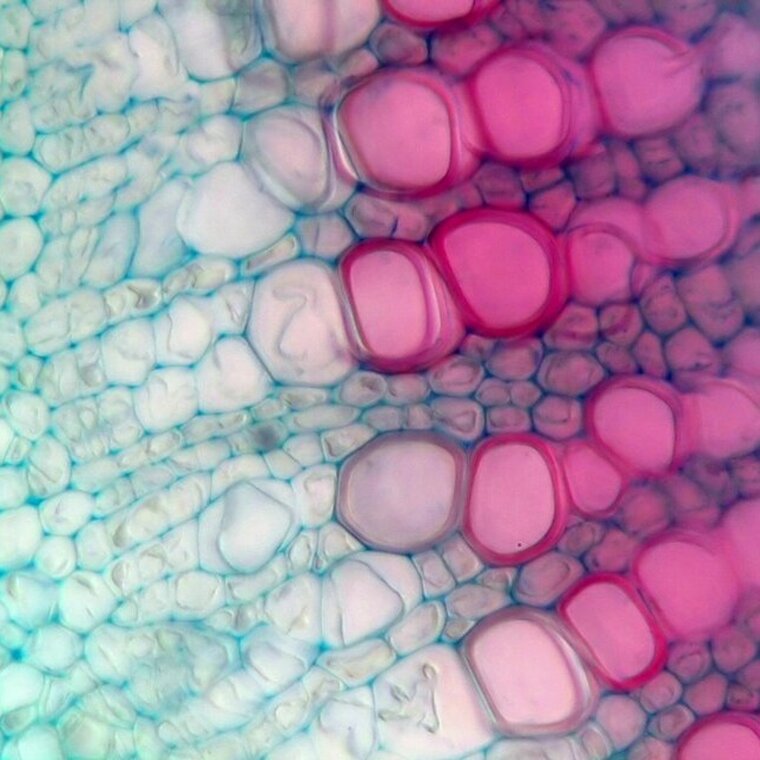
Wyniki barwienia
Ściana komórkowa celulozowa: barwa niebieskozielona
Ściana komórkowa zdrewniała: barwa czerwona
Słownik
struktury obserwowane w preparatach mikroskopowych powstałe podczas przygotowywania preparatów, niewystępujące w żywych komórkach lub tkankach
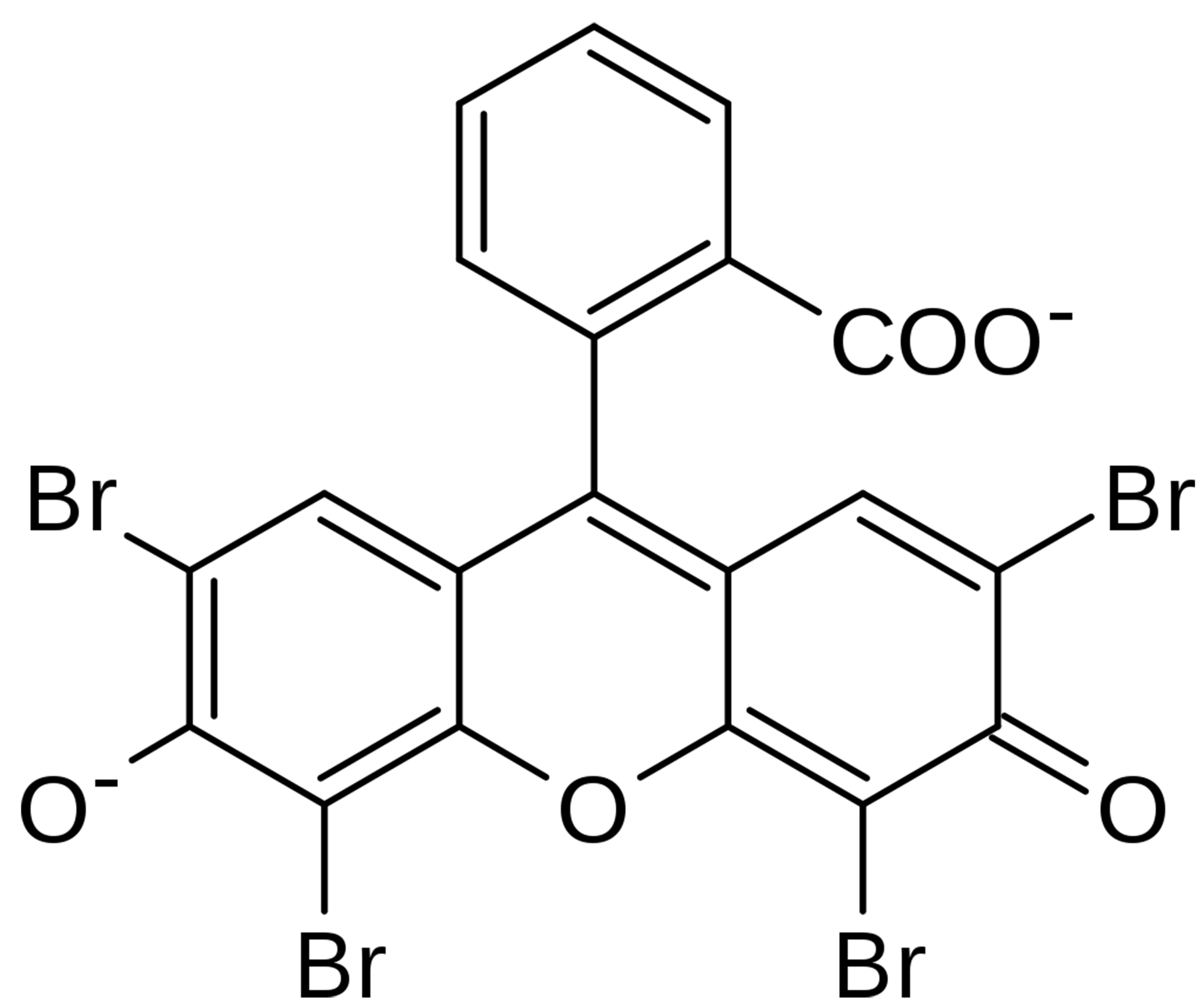
bromowa pochodna fluoresceiny; barwnik o właściwościach kwasowych, wykazujący silne powinowactwo do kwasochłonnych elementów komórki
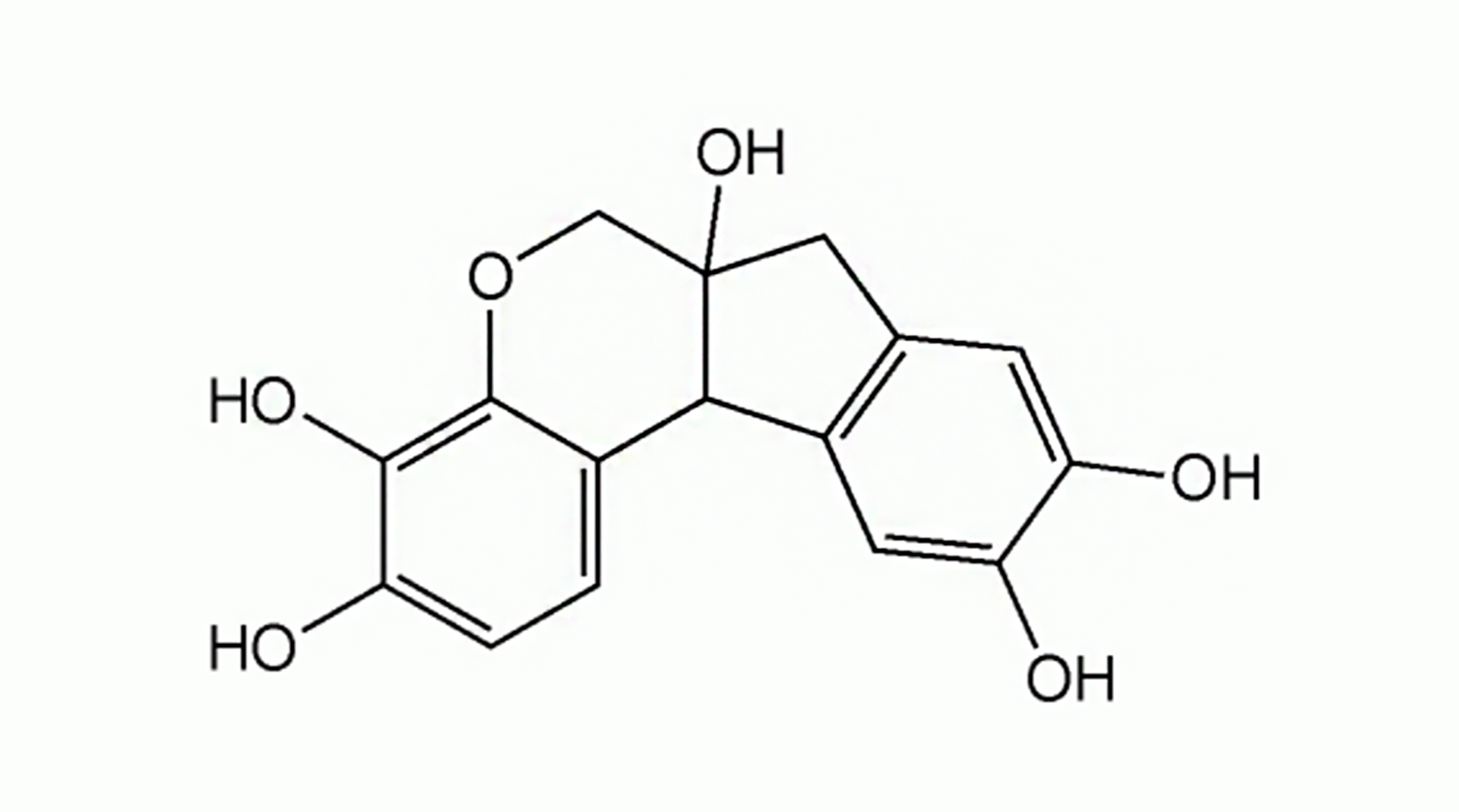
naturalny barwnik pozyskiwany z amerykańskiego drzewa Erythroxylon campechianum; używa się jej w postaci złożonych roztworów zawierających sole glinu, żelaza, chromu lub wolframu; zawartość tych metali sprawia, że tkanka przyjmuje barwnik
podstawowa technika obserwacji w mikroskopii optycznej; polega na oświetleniu preparatu wiązką światła uformowaną przez kondensor i wykorzystaniu różnicy pochłaniania (odbijania) przez elementy preparatu światła oświetlającego; często gdy elementy preparatu nie są zbyt kontrastowe, wykorzystuje się technikę barwienia bądź trawienia preparatów, opierającą się na różnicy w przyjmowaniu barwników przez różne elementy preparatu

zasadowy barwnik organiczny, trwały (odporny na działanie światła, wody, mydła itp.), stosowany w histologii i cytologii, używany podczas barwienia kontrastowego; wiąże się z jądrami (DNA) i innymi polianionami tkankowymi oraz składnikami ligniny i plastydami w tkankach roślinnych
niebieskozielony barwnik rozpuszczalny w alkoholu; może być stosowany z safraniną jako barwnik do tkanek roślinnych