Przeczytaj
Badanie procesu wysalania białek
Pamiętasz z pewnością, że roztwory dzielą się na trzy główne typy: roztwory właściwe, koloidalnekoloidalne oraz zawiesiny. To, co je od siebie odróżnia, to średnica cząstek fazy rozproszonej (składnik, który chcemy rozpuścić) w fazie rozpraszającej, czyli w rozpuszczalniku. W tym rozdziale zajmiemy się koloidami, a właściwie jednym szczególnym, z punktu widzenia nauki w szkole średniej, typem roztworu koloidalnego, czyli wodnym roztworem białek.
Koloidy należą do mieszanin niejednorodnych, heterogenicznych, w których średnica cząstek fazy rozproszonej mieści się w przedziale od do (czyli od do ). W roztworze wodnym białka fazą rozproszoną jest np. białko jaja kurzego, a fazą rozpraszającą (rozpuszczalnikiem) woda.
Białka to makrocząsteczki, które występują w każdym żywym organizmie. Musimy pamiętać, że istnieje wiele typów białek, a funkcje, jakie spełniają są bardzo różnorodne. Jednak wszystkie białka łączy to, że są zbudowane z dużej liczby reszt jednostek aminokwasowych połączonych w długi łańcuch. Istotne jest również to, że łańcuchy te zawierają wiele hydrofilowych (polarnych) elementów strukturalnych. A ta cecha z kolei jest kluczowa w tym rozdziale.
Badanie rozpuszczalności białka w wodzie
Wyobraź sobie, że rozpuszczamy białko jaja kurzego w wodzie.
Obserwujemy wówczas, że białko „wisi” w wodzie, a po dokładnym wymieszaniu, tworzy się emulsja. Otrzymaliśmy typowy roztwór koloidalny.
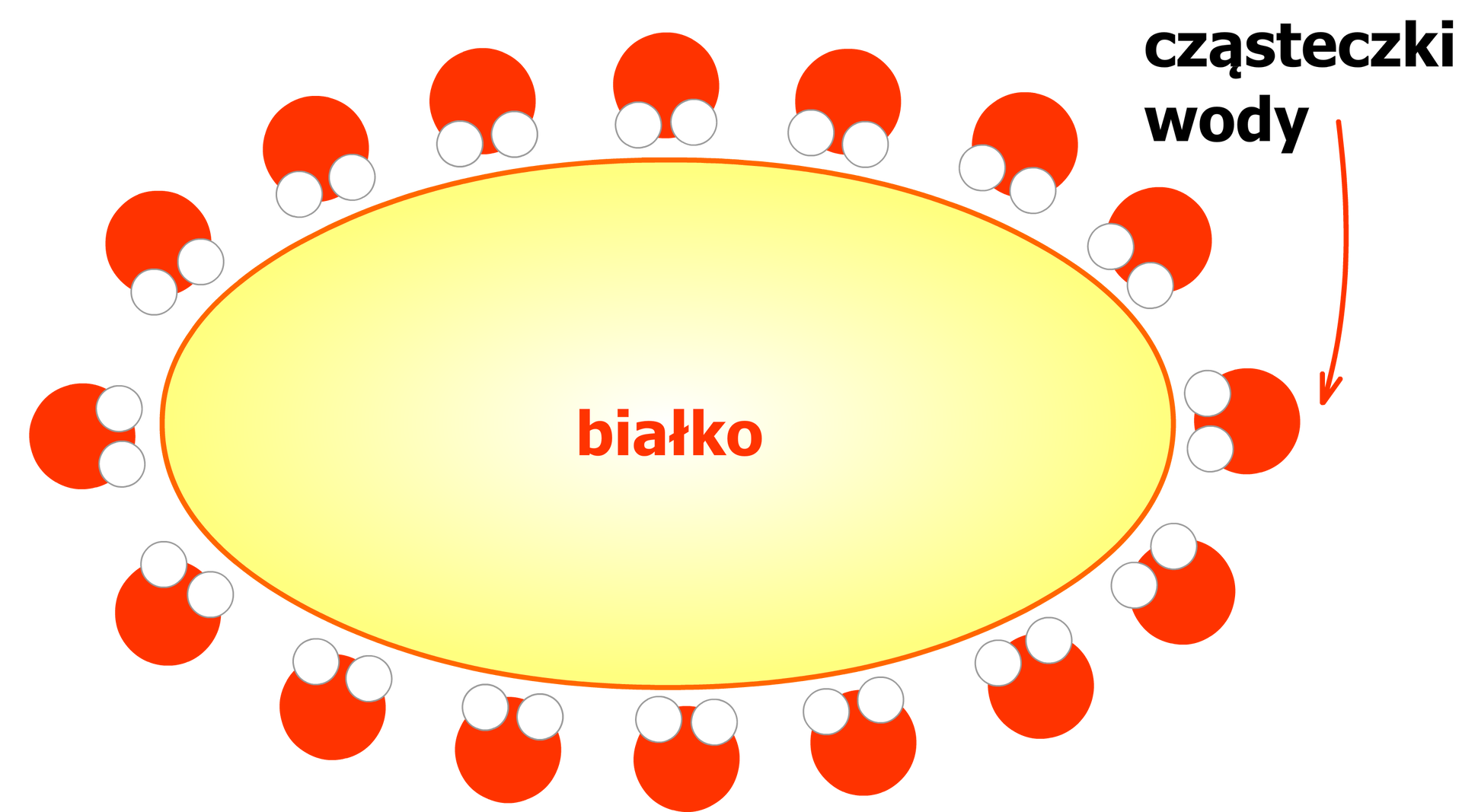
Przyczyną powstawania koloidu jest duży rozmiar cząsteczek białka. Oddziałują one solwatacyjnie z cząsteczkami wody. Innymi słowy są przez wodę hydratowane. A hydratacja to proces otaczania cząsteczek rozpuszczanego związku chemicznego przez wodę. To zjawisko jest możliwe dzięki własnościom polarnym wody oraz obecności w łańcuchach aminokwasowych białek grup polarnych, takich jak np.:
(grupa karboksylowa),
(grupa aminowa),
które oddziałują z wodą za pomocą wiązań wodorowych.
Koagulacja odwracalna czyli wysalanie białka
Kiedy mamy już przygotowany roztwór białka w wodzie, to wyobraźmy sobie, że dodajemy do niego nasycony roztwór soli kuchennej (). Obserwujemy wówczas zmianę konsystencji. Roztwór białka robi się gęstszy i powstają w nim białe grudki. Natomiast kiedy dodamy do roztworu wodę, to zaobserwujemy ponowne utworzenie roztworu koloidalnego.

Po dodaniu soli metalu lekkiego, otoczka solwatacyjna tworzona przez wodę zostaje zniszczona. Jony mocnego elektrolitu są silniej solwatowane niż białko. Następuje wówczas wytrącenie białka z roztworu w postaci charakterystycznego osadu – żelużelu. Jest to proces koagulacji odwracalnej,koagulacji odwracalnej, czyli wysalania. Po dodaniu wody, białko przyjmuje pierwotną postać, ponieważ nadmiar wody odbudowuje otoczkę hydratacyjną. Takie ponowne przejście żelu w zol zol nazywane jest peptyzacją.peptyzacją.

Należy pamiętać, że proces wysalania nie niszczy struktur białka, co wiąże się z zachowaniem przez białko swojej biochemicznej funkcjonalności. Koagulację odwracalną powodują tylko nasycone roztwory soli metali lekkich oraz amonowych.
Popularnym sposobem konserwacji śledzi było ich solenie. Śledzie układano w beczkach i zasypywano grubą warstwą soli w czasach, kiedy transport trwał kilkanaście dni. W ten sposób przedłużano termin ich spożycia. Następnie śledzie były tak długo moczone w wodzie, aż pozbyto się nadmiaru soli, by mogły być gotowe do konsumpcji. Tę metodę wykorzystuje się w kuchni do dzisiaj.

Słownik
stałe cząstki koloidalne rozproszone w cieczy (liozole), gazie (gazozole) lub nawet w ciele stałym (dirozole)
taki roztwór, w którym średnica cząstek substancji rozproszonej w ośrodku rozpraszającym waha się od do
efekt koagulacji zolu z ośrodkiem rozpraszającym w postaci cieczy, których cząstki koloidalne są tak blisko siebie, że układ zachowuje stabilność kształtu
proces wysalania
proces denaturacji
proces odwrotny do koagulacji; przejście żelu w zol
Bibliografia
Danikiewicz W., Część . Chemia organiczna, Warszawa 2009.
Kaznowski K., Chemia.Vademecum maturalne, Warszawa 2016.
McMurry J., Chemia organiczna, Warszawa 2000.
McMurry J., Chemia organiczna, Warszawa 2016.
Morrison R. T., Boyd R. N., Chemia organiczna, Warszawa 1985.