Przeczytaj
Aminokwasy
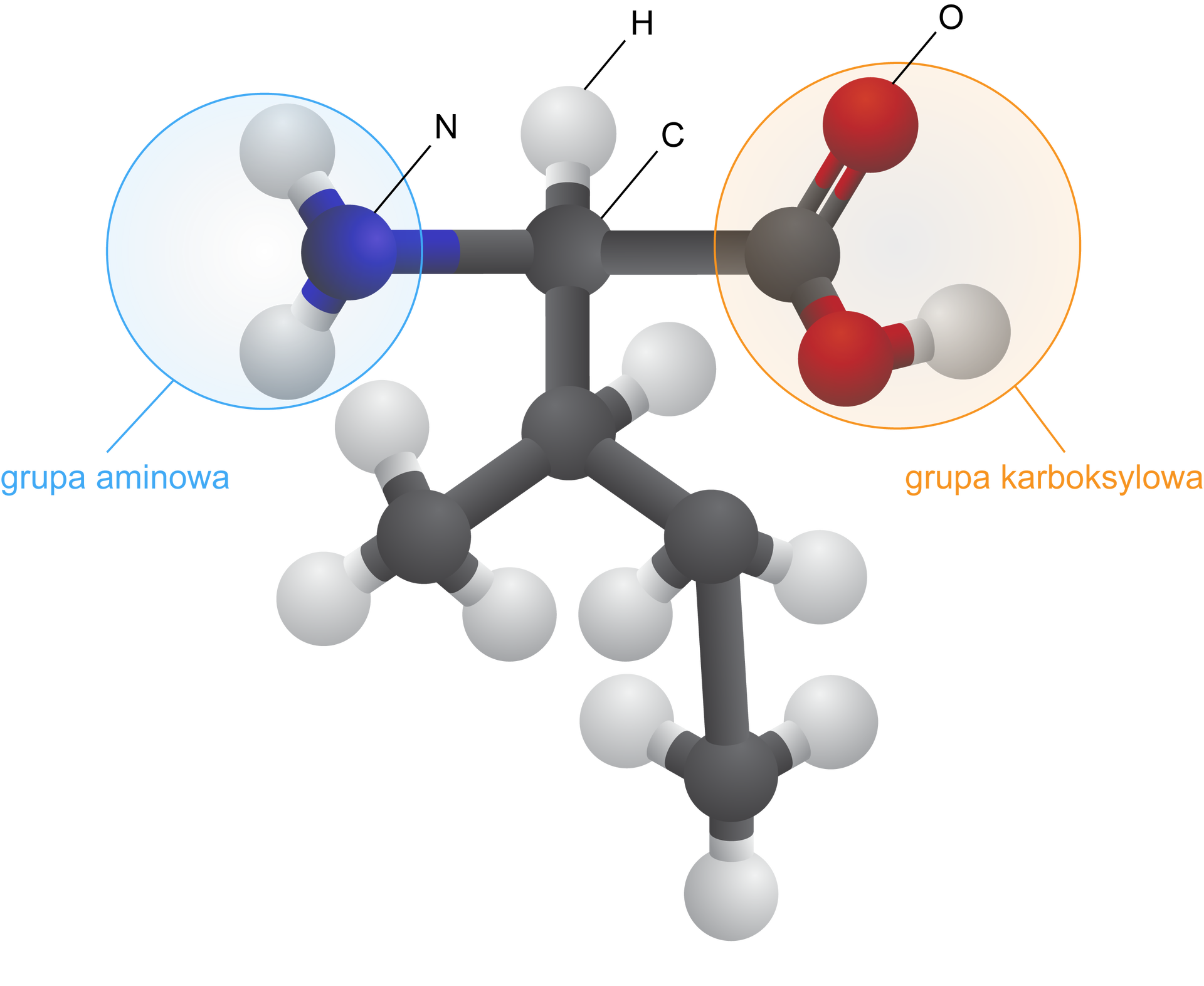
Aminokwasy to związki dwufunkcyjne zawierające w swych cząsteczkach grupę karboksylową -COOH oraz grupę aminową -NHIndeks dolny 22. Często aminokwasy są uznawane za pochodne kwasów karboksylowych, w których atom wodoru, w grupie węglowodorowej, został podstawiony przez grupę aminową. Do aminokwasów zalicza się również związki, zawierające również inne grupy funkcyjne, np. dodatkową grupę aminową lub karboksylową, grupę tiolową lub hydroksylowąhydroksylową, układy heterocykliczne, pierścienie aromatyczne.
Wiązania w peptydach
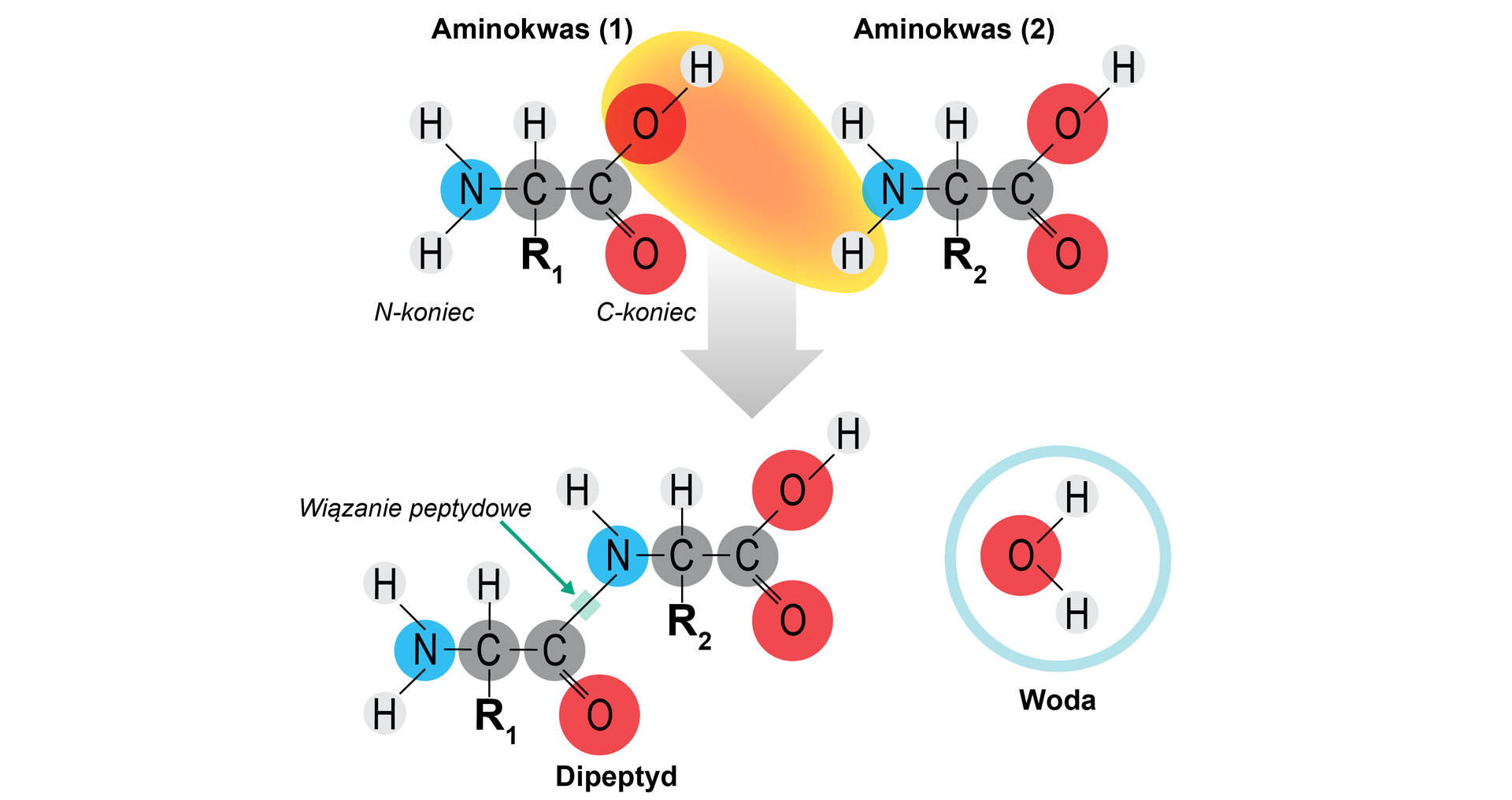
Każdy z aminokwasów łączy się z kolejnym aminokwasem za pomocą wiązania peptydowegowiązania peptydowego, zwanego również wiązaniem amidowym. Łączy ono grupę aminową jednego aminokwasu z grupą karboksylową drugiego aminokwasu. W wyniku tej reakcji powstaje woda.

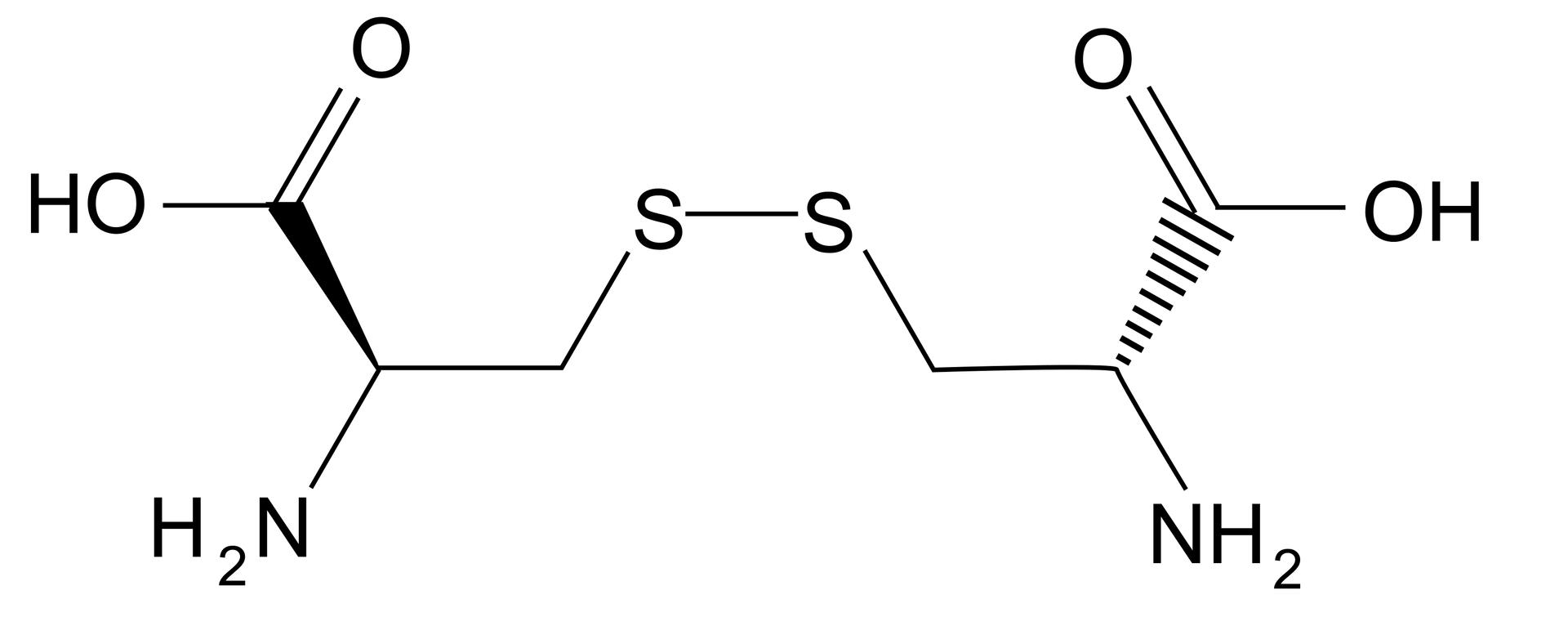
W peptydachpeptydach występują nie tylko wiązania peptydowe. Innym ważnym wiązaniem występującym w cząsteczkach peptydów jest wiązanie disiarczkowe (disulfidowe), które tworzy się przez utlenienie grupy funkcyjnej -SH cysteiny.
Struktura peptydów umożliwia również tworzenie się wiązań wodorowych powstających w wyniku oddziaływań między atomami tlenu i azotu jednej cząsteczki, a grupami -NH i -OH drugiej cząsteczki.
Cząsteczki peptydów są dodatkowo stabilizowane przez wiązania jonowe, które powstają w wyniku elektrostatycznych oddziaływań pomiędzy dodatnimi i ujemnymi ładunkami grup aminowych i karboksylowych, a także oddziaływania hydrofobowe.
Peptydy
Zbudowane są z reszt aminokwasów, połączonych wiązaniem peptydowym. Ze względów praktycznych peptydy o cząsteczkach zawierających mniej niż 10 reszt aminokwasowych są określane jako oligopeptydy, a zawierające do ok. 100 reszt — jako polipeptydy. Związki, których cząsteczki są zbudowane z ponad 100 reszt są określane jako białka.
Peptydy powstają na drodze kondensacji aminokwasów. Aminokwasy, ze względu na obecność w cząsteczkach grupy karboksylowej i grupy aminowej, mogą się ze sobą łączyć w tzw. reakcji kondensacji aminokwasów. W reakcji kondensacji dwóch różnych aminokwasów można uzyskać cztery różne dipeptydy, które zawierają wolną grupę aminową oraz wolną grupę karboksylową.
Naturalne peptydy to glutation, protaminy, hormony peptydowe (np. oksytocyna, wazopresyna, adrenokortykotropina), także niektóre antybiotyki (np. penicylina, gramicydyna) i jady (np. falloidyna).
Słownik
(gr. piepsilonpitauίdeltaiotaalfa „strawne”) związki organiczne zbudowane z reszt aminokwasów, połączonych wiązaniem peptydowym
wiązanie amidowe między grupą alfa‑karboksylową jednego aminokwasu a grupą alfa‑aminową drugiego; występuje w peptydach, białkach
–OH, jednowartościowa grupa wchodząca w skład cząsteczek wielu związków chemicznych, jak np. nadtlenek wodoru HO–OH, tlenowe kwasy nieorg. (np. azotowy(V) ), grupa funkcyjna alkoholi i fenoli oraz związków wielofunkcyjnych (np. hydroksykwasów)
Bibliografia
Encyklopedia PWN
Berg J. M., Stryer L., Tymoczko J. L., Gatto G. J., Biochemia, Warszawa 2018.
Jakubke H. D., Jeschkeit H., Aminokwasy, peptydy, białka, Warszawa 1989.