Sprawdź się
Na podstawie poniższych nazw, narysuj wzory strukturalne soli:
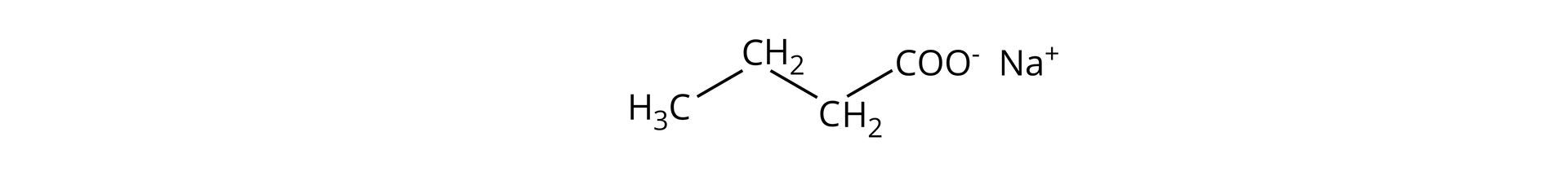
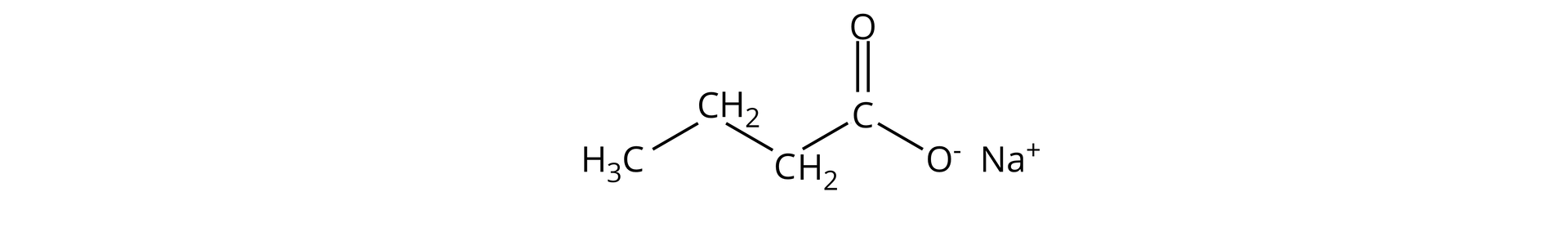
butanian sodu;
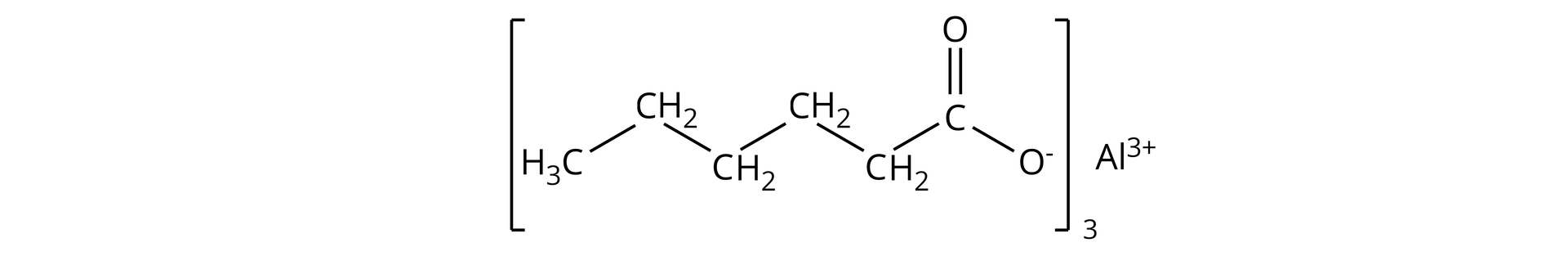
heksanian glinu;
heksadekanian potasu;
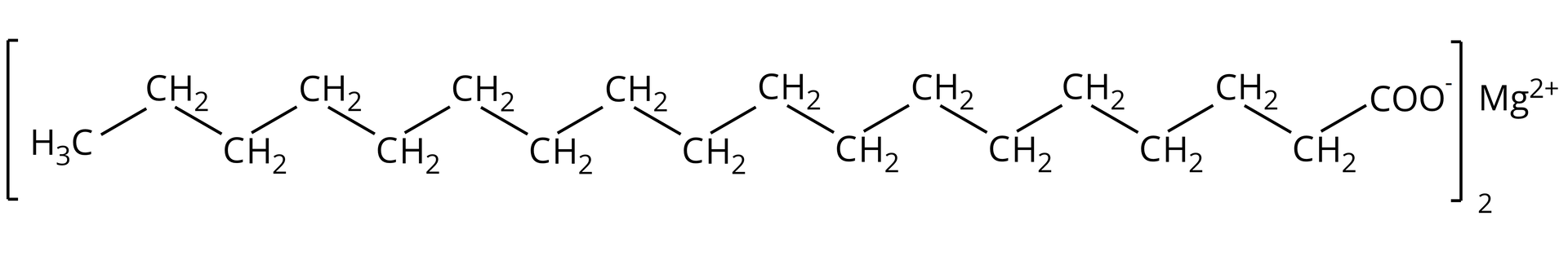
oktadekanian magnezu (stearynian magnezu).
Na podstawie poniższych nazw, opisz wzory strukturalne soli:
butanian sodu;
heksanian glinu;
heksadekanian potasu;
oktadekanian magnezu (stearynian magnezu).
Ogólny wzór mydeł, które są solami metalu wyższych kwasów tłuszczowych o 12–20 atomów węgla, można zapisać jako . Mydła składają się z dwóch fragmentów. Jeden z nich jest dłuższy, mający właściwości hydrofobowe i lipofilowe, natomiast druga część charakteryzuje się właściwościami hydrofilowymi i lipofobowymi. Który z fragmentów ( czy ) kryje się na schemacie pod określeniem „głowa”, a który pod określeniem „ogon”?
Zaznacz nazwę systematyczną przedstawionego poniżej związku.
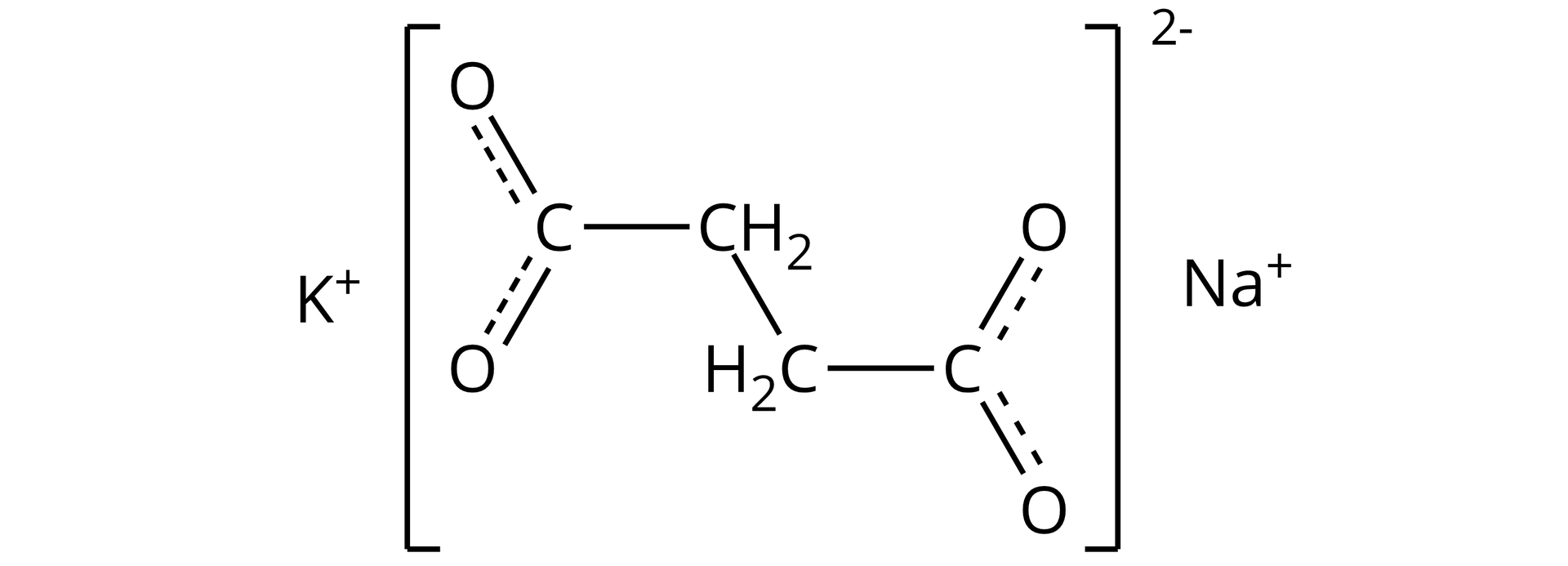
- butanodian potasu sodu
- butanodian sodu potasu
- winian potasu sodu
- winian sodu potasu
Pisząc odpowiednie równania reakcji, udowodnij, jaki jest odczyn wodnego roztworu etanianu potasu. Zaproponuj, jak doświadczalnie sprawdzić odczyn tego roztworu.
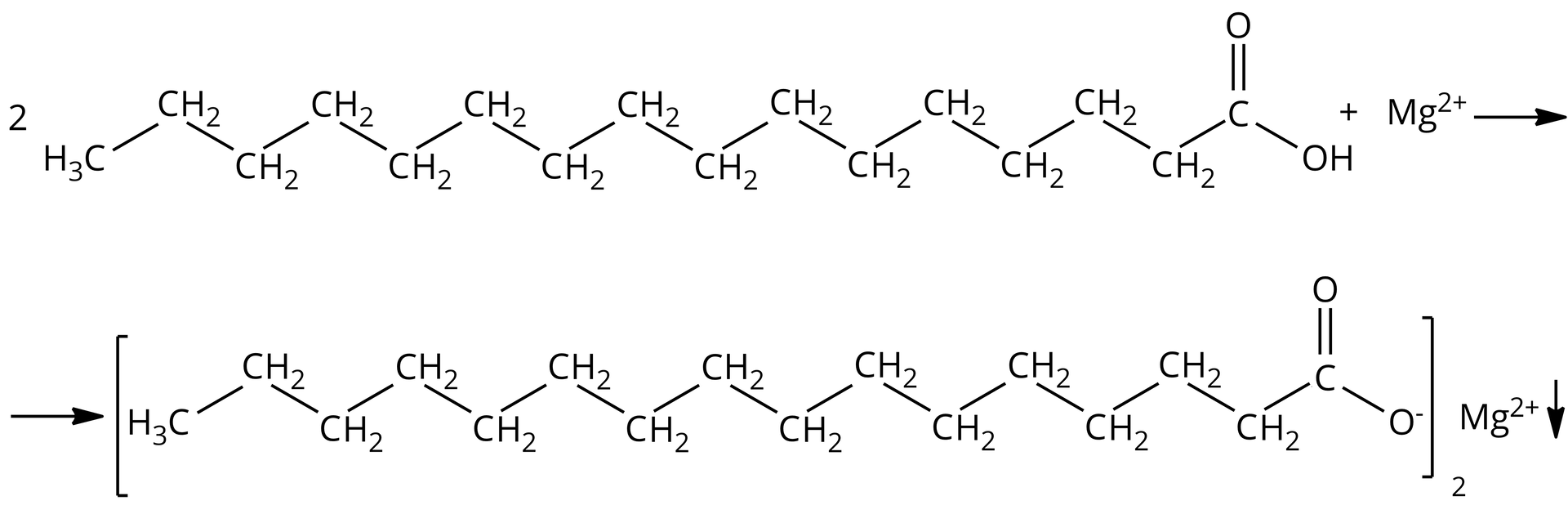
Twardość wody można wyrazić jako sumę stężeń takich jonów, jak: wapnia, magnezu, żelaza czy manganu. Im stężenie tych jonów jest większe, tym gorsze są właściwości myjące mydeł, ze względu na zachodzące reakcje składników mydła, np. kwasu heksadekanowego (kwasu palmitynowego) z twardą wodą. Na postawie odpowiedniej reakcji kwasu karboksylowego z jonami magnezu wyjaśnij, czym skutkuje obecność twardej wody.
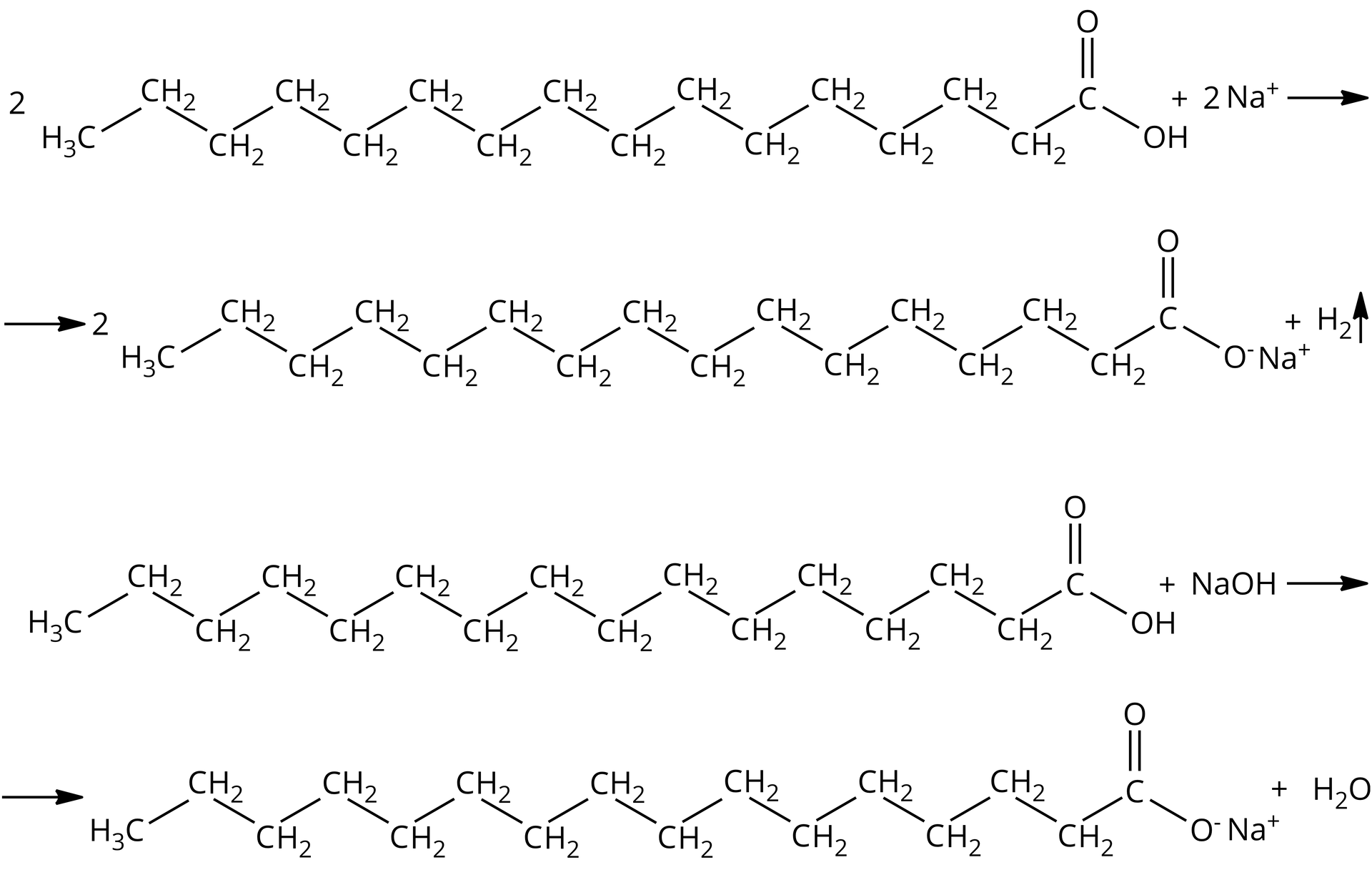
Sole kwasów karboksylowych można otrzymać w wyniku bezpośredniej reakcji kwasu karboksylowego z metalem 1. i 2. grupy układu okresowego lub w wyniku reakcji z wodorotlenkiem. Jednym ze składników mydeł jest heksadekanian sodu (palminitynian sodu) o wzorze grupowym . Zapisz równanie otrzymywania tego mydła dwoma sposobami, narysuj wzór półstrukturalny produktu.
Sole kwasów karboksylowych można otrzymać w wyniku bezpośredniej reakcji kwasu karboksylowego z metalem 1. i 2. grupy układu okresowego lub w wyniku reakcji z wodorotlenkiem. Jednym ze składników mydeł jest heksadekanian sodu (palminitynian sodu). Wskaż jego wzór sumaryczny.
- C15H31COOH
- C17H33COOH
- C11H31COOH
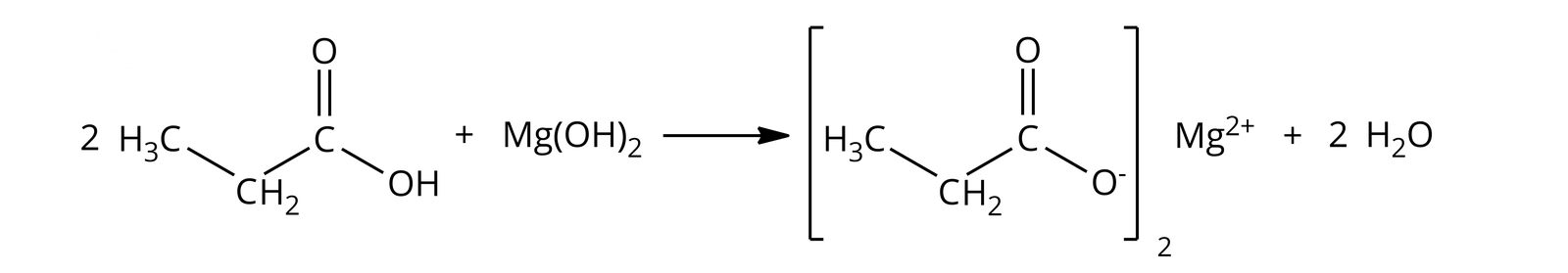
Analiza elementarna pewnej soli monokarboksylowego nasyconego kwasu karboksylowego wykazała, że składa się on z 42,28% masowych węgla, 5,91% masowych wodoru, 14,26% masowych magnezu, a resztę stanowi tlen. Masa molowa kwasu karboksylowego wynosi 170,3 . Na podstawie odpowiednich obliczeń, ustal:
wzór empiryczny soli kwasu karboksylowego;
wzór rzeczywisty soli kwasu karboksylowego.
Zaproponuj reakcje, w wyniku których można otrzymać tę sól – podaj jej nazwę. Dla obliczeń przyjmij następujące masy molowe: