Sprawdź się
Aluminotermia to metoda otrzymywania niektórych metali przez redukcję ich tlenków za pomocą glinu. Do jakiego typu procesów należy?
- metalotermicznych
- elektrolitycznych
- hydrometalurgicznych
Napisz równanie reakcji otrzymywania chromu z tlenku chromu(III) metodą aluminotermii.
Jak zmienia się charakter kwasowo‑zasadowy tlenków chromu, na II, III i VI stopniu utlenienia chromu? Połącz tlenki chromu z ich charakterem chemicznym.
kwasowy, amfoteryczny, zasadowy
| CrO | |
| Cr2O3 | |
| CrO3 |
Napisz konfigurację elektronową atomu chromu w stanie podstawowym. Ile elektronów niesparowanych znajduje się w atomie chromu? Jakie są typowe stopnie utlenienia chromu w związkach?
Liczba elektronów niesparowanych: 1. 6, 2. 7, 3. 24, 4. 4s1, 5. I,II i III, 6. II, III i VI, 7. 25, 8. 3d5, 9. 26, 10. 5, 11. 3d6, 12. II, III i VI, 13. 3d10, 14. 4s2
Typowe stopnie utlenienia chromu: 1. 6, 2. 7, 3. 24, 4. 4s1, 5. I,II i III, 6. II, III i VI, 7. 25, 8. 3d5, 9. 26, 10. 5, 11. 3d6, 12. II, III i VI, 13. 3d10, 14. 4s2
4s2, II, III i VI, 26, II, III, 7, 3d6, 5, 3d5, 6, 4s1, 3d10, 24, 25, I, II i III
Konfiguracja elektronowa: [..........................Cr] : 1s22s22p63s23p6....................................................
Liczba elektronów niesparowanych: ..........................
Typowe stopnie utlenienia chromu: ..........................
Chrom na powietrzu w wyniku pasywacji chrom pokrywa się warstewką tlenku chromu(III). Dlatego, mimo że jest metalem o ujemnym potencjale elektrochemicznym, nie reaguje z wodą, a w reakcji z kwasem solnym i rozcieńczonym kwasem siarkowym(VI) tworzy – obok wydzielonego wodoru – związki na II (warunki beztlenowe) lub III stopniu utlenienia (warunki tlenowe).
Zapisz równania reakcji chromu z kwasem solnym w warunkach beztlenowych i tlenowych.
Tetrahydroksochromian(III) sodu to rozpuszczalny związek koordynacyjny chromu. Do roztworu tej soli, dodano kwasu solnego i wtedy wytrącił się szarozielony osad wodorotlenku chromu(III). W reakcji tej powstaje także inna sól oraz woda. Napisz i uzgodnij równanie tej reakcji.
Do roztworu siarczanu(VI) chromu(III) dodano roztwór wodny wodorotlenku sodu oraz 6% roztwór nadtlenku wodoru.
A. Napisz przewidywane obserwacje oraz wnioski, jakie wynikają z tych obserwacji.
B. Napisz równanie zachodzącej reakcji chemicznej.
Wnioski:
Równanie reakcji chemicznej:
Odpowiedź zapisz w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Zapisz równania reakcji przedstawionych na schemacie.
Zapisz równania reakcji opisanych na schemacie.
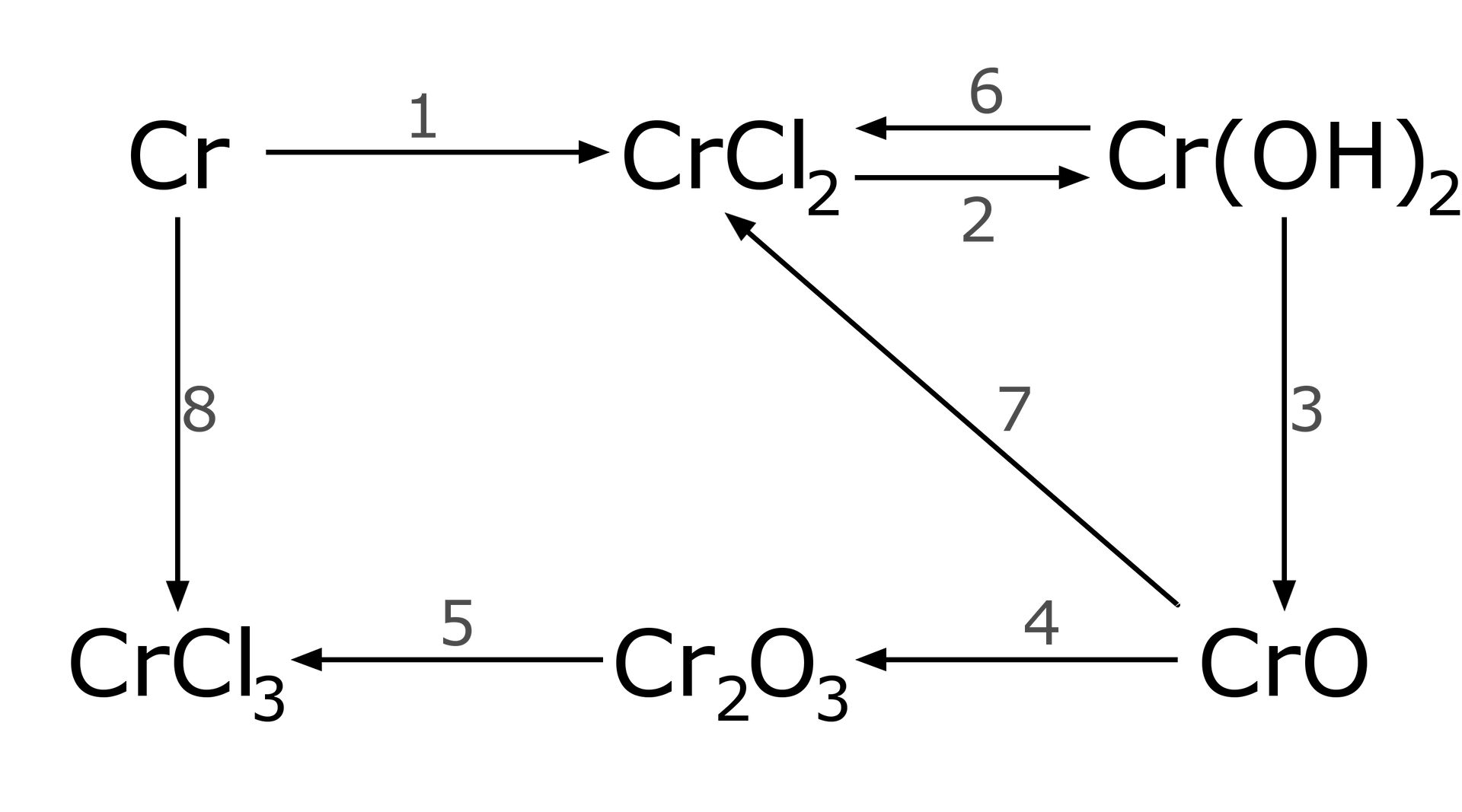
Dokończ poniższe równania reakcji lub napisz, że dana reakcja nie zachodzi.