Sprawdź się
1. , 2. , 3. , 4. , 5. , 6.
Etap
1. , 2. , 3. , 4. , 5. , 6. 1. , 2. , 3. , 4. , 5. , 6.
Etap
1. , 2. , 3. , 4. , 5. , 6.
Kwas siarkowy() jest substancją oleistą, silnie higroskopijną cieczą o gęstości
. Podczas rozcieńczania go w wodzie wydziela się ciepło. Wyjaśnij, dlaczego podczas rozcieńczania kwasu siarkowego() należy wlewać go do wody, a nie wodę do kwasu?
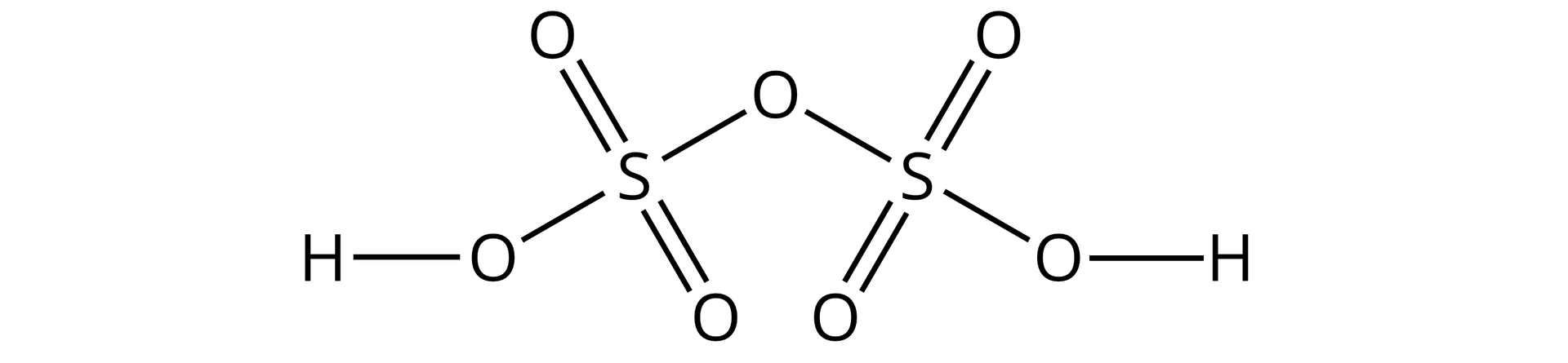
Narysuj wzór strukturalny kwasu heptaoksodisiarkowego.
Oblicz, ile moli kwasu siarkowego() otrzyma się w trzyetapowym procesie, w którym wykorzystano czystej siarki. Załóż, że każdy etap procesu zachodzi z wydajnością . Wynik podaj w kilogramach z dokładnością do trzech cyfr po przecinku. Do obliczeń przyjmij następujące wartości mas molowych:
,
,
.
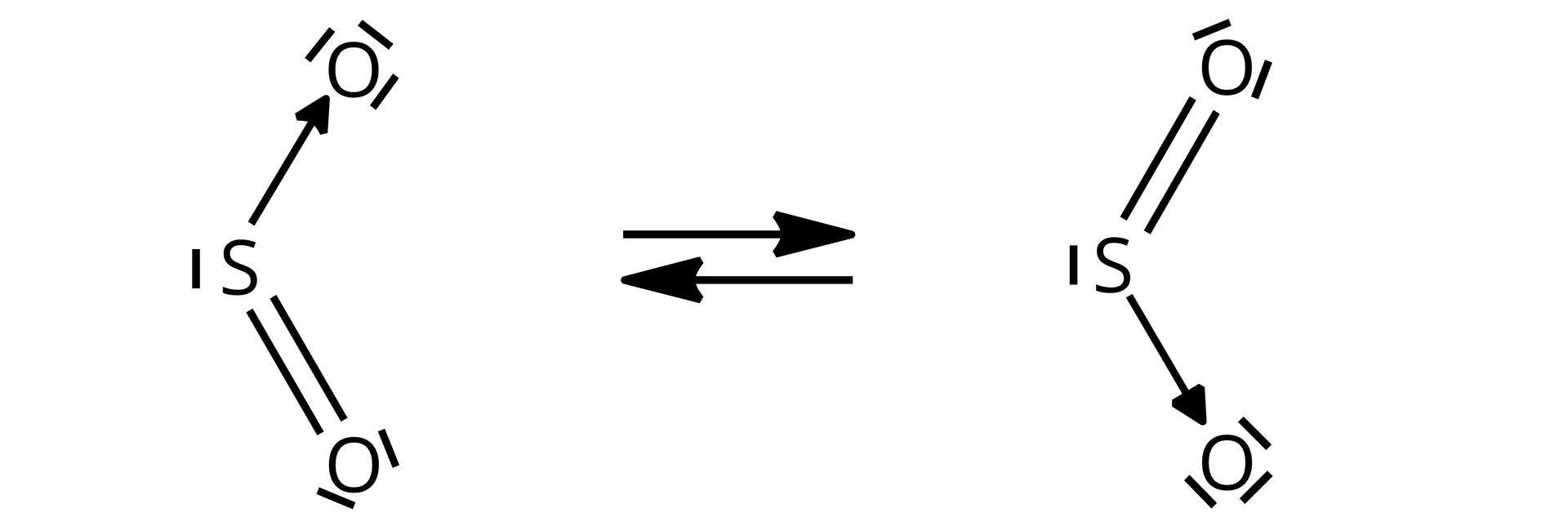
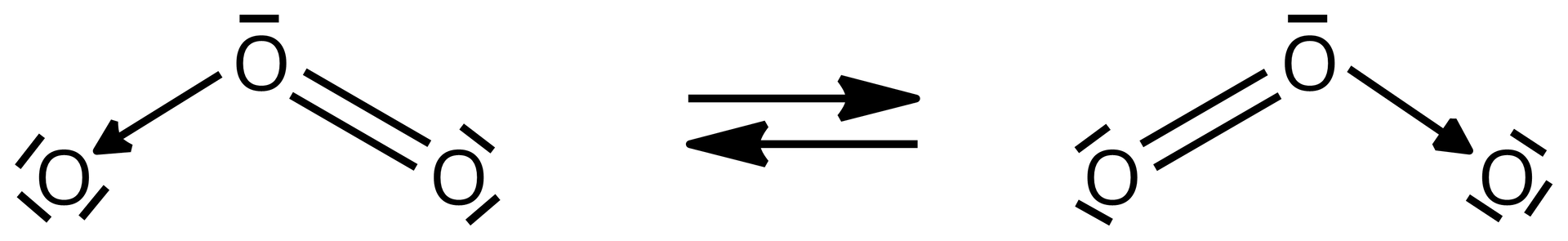
Struktury elektronowej cząsteczki tlenku siarki() nie udaje się przedstawić pojedynczą strukturą Lewisa, podobnie jak w przypadku cząsteczki ozonu.
Indeks górny Bielański A., Podstawy chemii nieorganicznej, t. 2, Warszawa 2007. Indeks górny koniecBielański A., Podstawy chemii nieorganicznej, t. 2, Warszawa 2007.
W tworzeniu wiązań typu w cząsteczce tlenku siarki() biorą udział orbitale typu . Skutkiem tego jest istnienie dwóch granicznych form, stąd wiązanie ma charakter pośredni między wiązaniem pojedynczym a podwójnym. Narysuj wzory elektronowe dwóch form granicznych tlenku siarki().
W tworzeniu wiązań typu w cząsteczce tlenku siarki () biorą udział orbitale typu . Skutkiem tego jest istnienie dwóch granicznych form, stąd wiązanie ma charakter pośredni między wiązaniem pojedynczym a podwójnym. Opisz dwie formy graniczne tlenku siarki ().
Wykonano następujące doświadczenie.

Zapisz obserwacje, równanie zachodzącej reakcji chemicznej oraz wnioski. Odpowiedz, czy tlenek siarki() jest tlenkiem kwasotwórczym, zasadotwórczym, czy obojętnym wobec wody?
Do probówki zawierającej wodny roztwór oranżu metylowego dodano tlenek siarki().
Zapisz obserwacje, równanie zachodzącej reakcji chemicznej oraz wnioski. Odpowiedz, czy tlenek siarki() jest tlenkiem kwasotwórczym, zasadotwórczym, czy obojętnym wobec wody?