Sprawdź się
Wybierz poprawną odpowiedź.
Wybierz odpowiednie określenia, aby powstały zdania prawdziwe.
Zapisz równanie reakcji w formie jonowej skróconej tworzenia kompleksu niklu() z amoniakiem, wiedząc że liczba koordynacyjna niklu w tym kompleksie wynosi . Przyjmij, że w roztworze wodnym jony niklu() występują w postaci heksaakwakompleksu.
Do wodnego roztworu dodawano kroplami wodny roztwór . Zaobserwowano wytrącanie osadu, który następnie uległ roztworzeniu. Określ, jakie obserwacje można będzie zauważyć podczas stopniowego dodawania roztworu do otrzymanego końcowego roztworu. Wyjaśnij przyczyny zachodzenia obserwowanych zjawisk za pomocą odpowiednich równań reakcji chemicznych.
Do jasnoniebieskiego wodnego roztworu dodawano kroplami wodny roztwór . Zaobserwowano zmianę barwy roztworu wskutek utworzenia jonu kompleksowego heksaaminamiedzi(). Zapisz równanie procesu, przyjmując, że jony miedzi() w wodnym roztworze występują w postaci jonu .
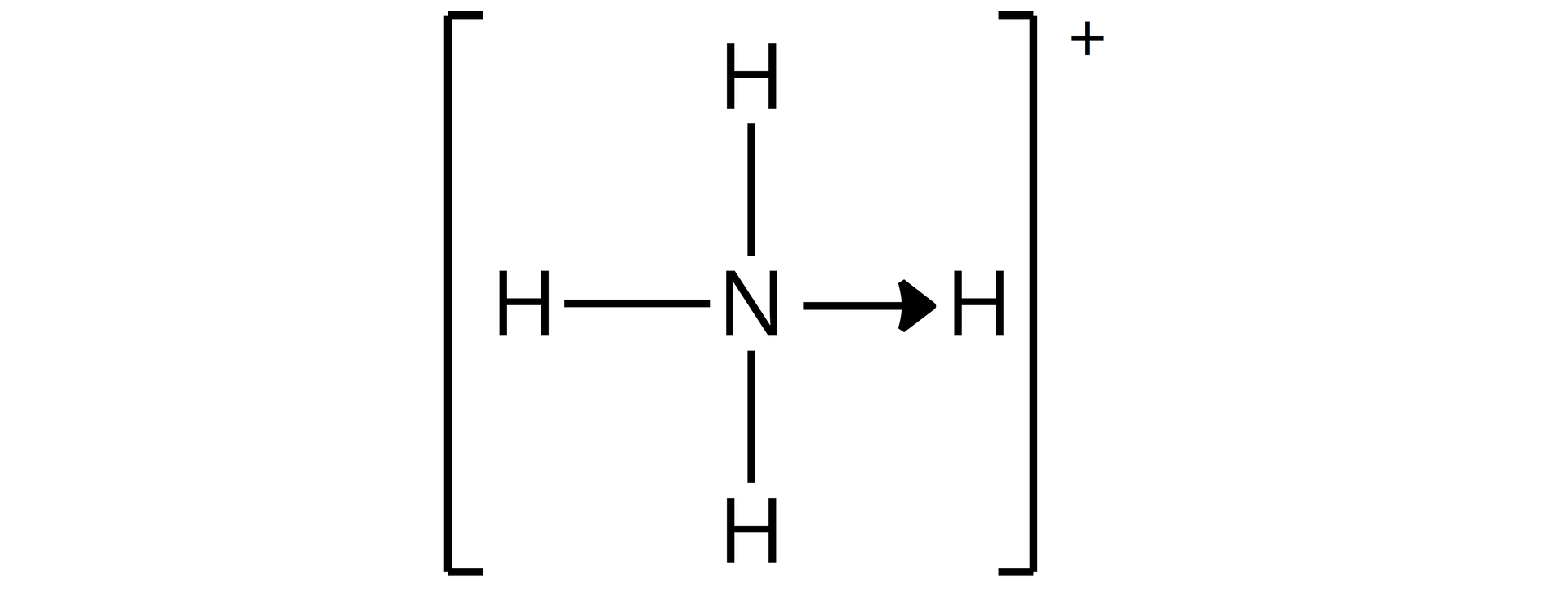
Określ, czy jon może być ligandem? Odpowiedź uzasadnij w oparciu o wzór elektronowy (kreskowy) tego jonu.
Do roztworu zawierającego jony dodano niewielką ilość stężonego kwasu siarkowego() i zamieszano. Zaobserwowano zanik charakterystycznego ciemnoniebieskiego zabarwienia. Zapisz równanie tego procesu w postaci jonowej skróconej.
Wodorotlenki cynku i glinu roztwarzają się w roztworze , natomiast reakcji z wodą amoniakalną ulega tylko . Zapisz równania reakcji w formie cząsteczkowej, przyjmując, że w powstających związkach kompleksowych liczba koordynacyjna wynosi 4, lub zaznacz, że reakcja nie zachodzi: