Sprawdź się
Zaznacz poprawne odpowiedzi.
Zaznacz poprawną odpowiedź.
Uczeń otrzymał zadanie zaproponowania metody oddzielenia jonów ołowiu() od jonów wapnia, znajdujących się w tym samym roztworze. Stąd zaproponował, aby do roztworu, zawierającego jony i , dodawać kroplami rozcieńczony roztwór kwasu siarkowego(), aż do całkowitego wytrącenia osadu. Oceń, czy zaproponowana przez ucznia metoda pozwoli na realizację postawionego celu. Odpowiedź uzasadnij.
Informacja do ćwiczenia
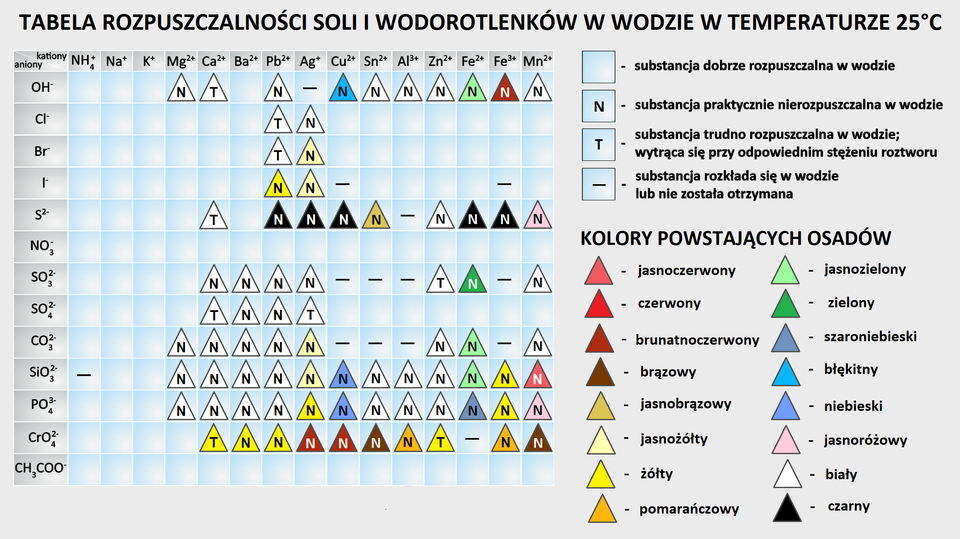
W tabeli rozpuszczalności można znaleźć informacje dotyczące jonów wymienionych w treści zadania. W przypadku obecności w roztworze jonów oraz jonów powstaje biały, praktycznie nierozpuszczalny w wodzie osad, zaś w przypadku obecności w roztworze jonów oraz jonów powstaje biały, trudno rozpuszczalny w wodzie osad. Osad ten powstaje przy odpowiednich stężeniach roztworu.
Zaproponuj metodę otrzymywania siarczku ołowiu() w oparciu o reakcję soli z inną solą.
Zapisz równanie reakcji chemicznej w formie cząsteczkowej, jonowej oraz jonowej skróconej.
Zapisz przynajmniej dwie różne pary różnych soli, których można użyć w tej reakcji.
Zaznacz produkt trudno rozpuszczalny (lub nierozpuszczalny) odpowiednim symbolem.

Informacja do ćwiczenia
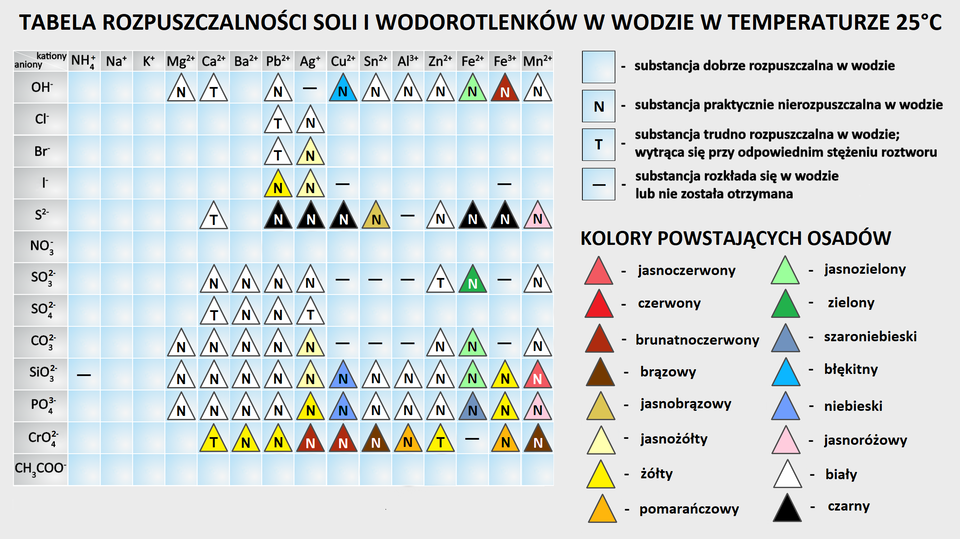
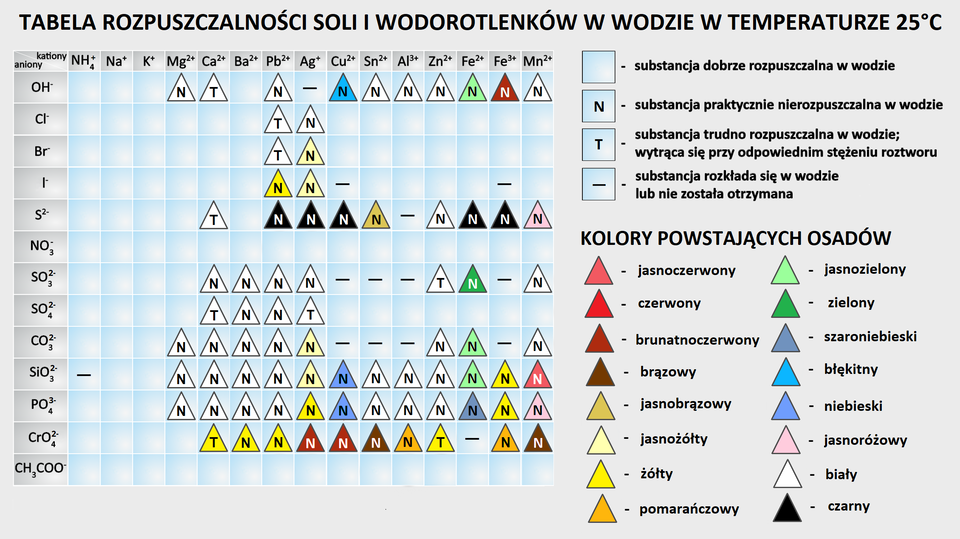
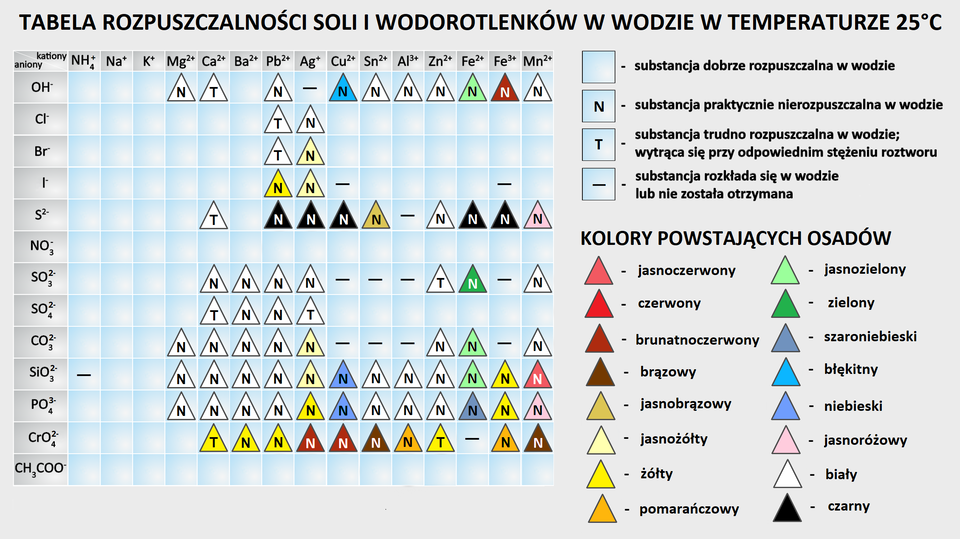
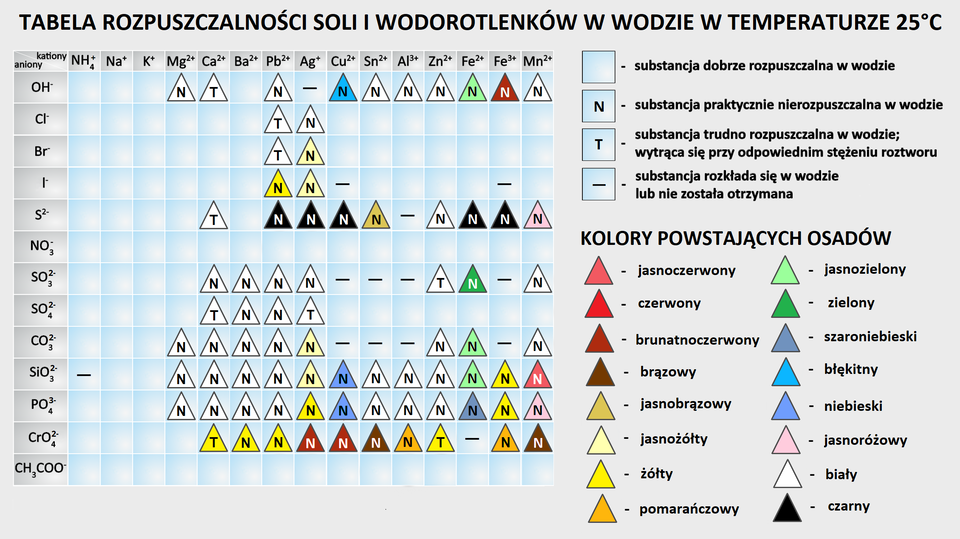
Fragment tabeli rozpuszczalności soli i wodorotlenków w wodzie w temperaturze dwudziestu pięciu stopni Celsjusza. Z tabeli można odczytać, które substancje są dobrze rozpuszczalne w wodzie, praktycznie nierozpuszczalne w wodzie, trudno rozpuszczalne w wodzie, to jest osad wytrąca się przy odpowiednim stężeniu roztworu lub substancje rozkładające się albo takie, dla których substancja chemiczna nie została otrzymana. Ponadto zaznaczono kolory otrzymywanych osadów.
Dane pochodzące z tabeli rozpuszczalności dla anionu siarczkowego. Trudno rozpuszczalny biały osad siarczku wapnia. Nierozpuszczalny czarny siarczek srebra. Nierozpuszczalny czarny osad siarczku miedzi. Nierozpuszczalny brązowo‑żółty siarczek cyny. Siarczek glinu oznaczony znakiem minus, co oznacza, że związek rozkłada się lub nie powstaje. Nierozpuszczalny biały osad siarczku cynku. Nierozpuszczalny czarny siarczek żelaza(). Nierozpuszczalny czarny siarczek żelaza(). Różowy, nierozpuszczalny osad siarczku manganu(). Pozostałe siarczki są dobrze rozpuszczalne, a wśród nich siarczki: amonu, sodu, potasu, magnezu i baru.
Dane pochodzące z tabeli rozpuszczalności dla kationu ołowiu. Nierozpuszczalne i białe związki ołowiu: wodorotlenek ołowiu, siarczan() ołowiu oraz siarczan() ołowiu, węglan ołowiu, krzemian ołowiu oraz fosforan() ołowiu, a także czarny siarczek ołowiu oraz żółte sole: jodek ołowiu i chromian() ołowiu. Do trudno rozpuszczalnych i białych związków ołowiu zaliczono chlorek ołowiu oraz bromek ołowiu. Pozostałe sole, to jest azotan() i octan są dobrze rozpuszczalne.
Uczeń otrzymał zadanie zaproponowania metody oddzielenia jonów ołowiu() od jonów wapnia, znajdujących się w tym samy roztworze.
Korzystając z tablicy rozpuszczalności wodorotlenków i soli w wodzie, zastanów się i odpowiedz, jakiego anionu należałoby użyć, aby rozdzielić tę mieszaninę i otrzymać sól jednego kationu w formie osadu. Uzasadnić swój wybór w oparciu o odpowiednie równania reakcji zapisane w formie jonowej skróconej.
Informacja do ćwiczenia
Dane pochodzące z tabeli rozpuszczalności dla kationu ołowiu. Nierozpuszczalne i białe związki ołowiu: wodorotlenek ołowiu, siarczan() ołowiu oraz siarczan() ołowiu, węglan ołowiu, krzemian ołowiu oraz fosforan() ołowiu, a także czarny siarczek ołowiu oraz żółte sole: jodek ołowiu i chromian() ołowiu. Do trudno rozpuszczalnych i białych związków ołowiu zaliczono chlorek ołowiu oraz bromek ołowiu. Pozostałe sole, to jest azotan() i octan są dobrze rozpuszczalne.
Dane pochodzące z tabeli rozpuszczalności dla kationu wapnia. Do nierozpuszczalnych soli należą białe: siarczan() wapnia, węglan wapnia, krzemian wapnia i fosforan() wapnia. Do trudno rozpuszczalnych należą białe: wodorotlenek wapnia, siarczek wapnia, siarczan() wapnia oraz żółty chromian() wapnia. Pozostałe sole wapnia są rozpuszczalne, wśród nich: chlorek, bromek, jodek, azotan() oraz octan.
Do octanu wapnia (etanianu wapnia) wkraplano powoli wodorotlenek potasu. Zaobserwowano wytrącenie białego osadu. Korzystając z tabeli rozpuszczalności wodorotlenków i soli w wodzie, zapisz równanie reakcji, jaka zaszła w roztworze. Zapisz równanie reakcji w formie cząsteczkowej, jonowej oraz jonowej skróconej. Zaznacz produkt trudno rozpuszczalny odpowiednim symbolem.
Informacja do ćwiczenia
Zgodnie z danymi pochodzącymi z tablicy rozpuszczalności wszystkie sole potasu są dobrze rozpuszczalne.
Dane pochodzące z tabeli rozpuszczalności dla kationu wapnia informują, że do związków trudnorozpuszczalnych należy między innymi biały wodorotlenek wapnia. Z kolei octanwapnia jest solą dobrze rozpuszczalną.
W roztworze znajdowały się azotan() magnezu i azotan() żelaza(). Następnie do roztworu wkroplono siarczek sodu. Korzystając z tablicy rozpuszczalności, zastanów się, czy wytrąci się osad. Odpowiedz, czy w wyniku strącenia osadu można rozdzielić tę mieszaninę kationów poprzez wydzielenie przynajmniej jednego kationu. Odpowiedź uzasadnij odpowiednimi równaniami reakcji.
Informacja do ćwiczenia
Dane pochodzące z tabeli rozpuszczalności dla anionu siarczkowego. Trudno rozpuszczalny biały osad siarczku wapnia. Nierozpuszczalny czarny siarczek srebra. Nierozpuszczalny czarny osad siarczku miedzi. Nierozpuszczalny brązowo‑żółty siarczek cyny. Siarczek glinu oznaczony znakiem minus, co oznacza, że związek rozkłada się lub nie powstaje. Nierozpuszczalny biały osad siarczku cynku. Nierozpuszczalny czarny siarczek żelaza(). Nierozpuszczalny czarny siarczek żelaza(). Różowy, nierozpuszczalny osad siarczku manganu(). Pozostałe siarczki są dobrze rozpuszczalne, a wśród nich siarczki: amonu, sodu, potasu, magnezu i baru. Azotany() soli wymienionych w zadaniu są dobrze rozpuszczalne.
Zapisz równania jonowe skrócone otrzymywania poniższych wodorotlenków i soli.
Wodorotlenku żelaza()
Wodorotlenku glinu
Ortofosforanu() srebra()
Chromianu() baru
Informacja do ćwiczenia
Zgodnie z informacjami zawartymi w tablicy rozpuszczalności wszystkie wymienione w treści ćwiczenia związki są nierozpuszczalnymi w wodzie.