Sprawdź się
Poniżej przedstawiono symbole litowców. Uszereguj przedstawione pierwiastki zgodnie z ich malejącą aktywnością chemiczną. Zapisz równania reakcji z wodą najbardziej aktywnego i najbardziej biernego chemicznie litowca.
Uszeregowanie:
Rysunek przedstawia sposób przeprowadzenia reakcji sodu z wodą.
Zapoznaj się z opisem rysunku, przedstawiającego schemat reakcji sodu z wodą.
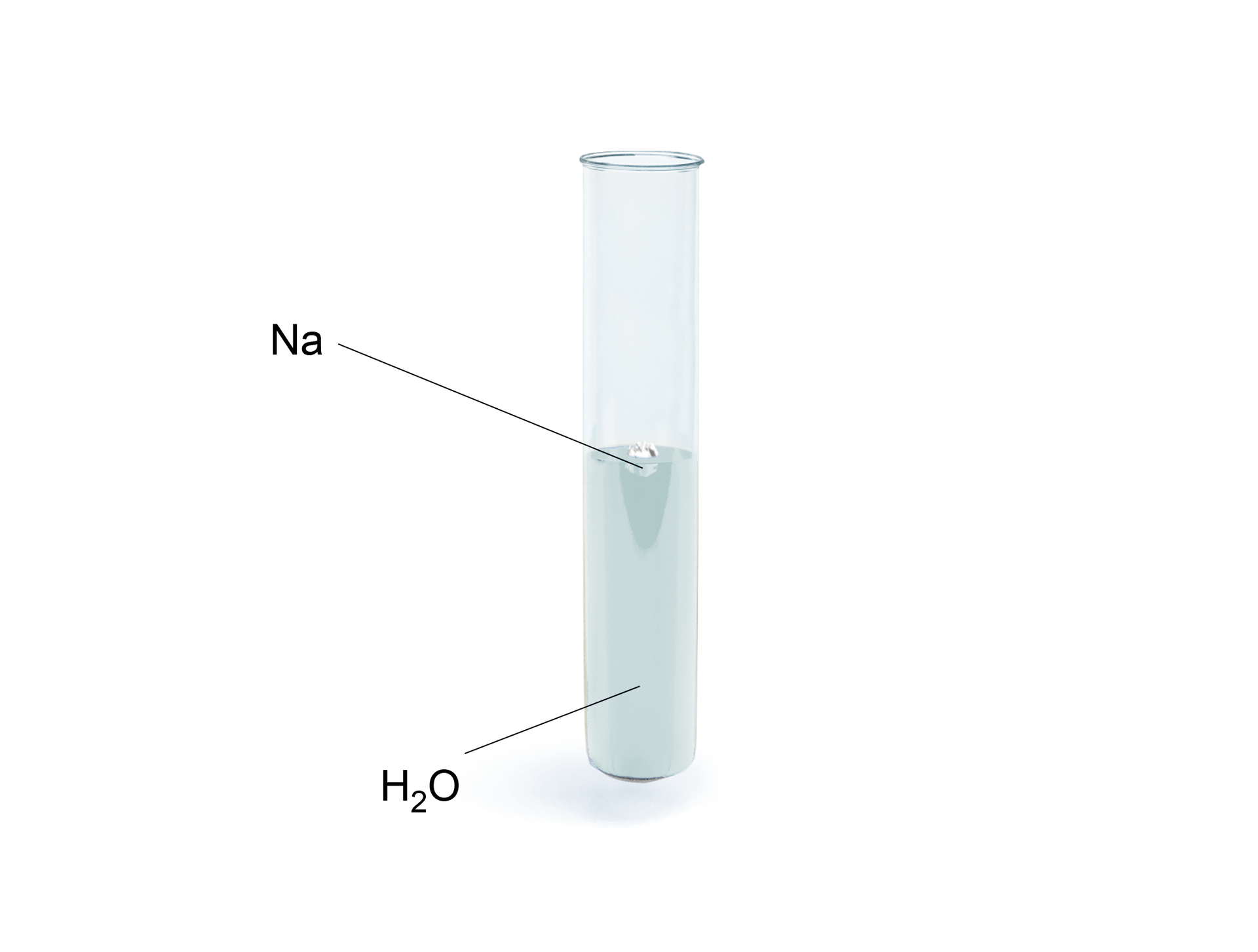
A. Na podstawie rysunku określ, czy gęstość sodu jest większa od gęstości wody.
B. Odpowiedz, jaki gaz wydziela się w czasie tej reakcji.
C. Po reakcji dodano do roztworu kroplę alkoholowego roztworu fenoloftaleiny. Odpowiedz, jak zabarwi się roztwór.
D. Odpowiedz, jaki odczyn ma roztwór po reakcji.
E. Napisz odpowiednie równanie jonowe reakcji zachodzącej w probówce.
Stały wodorotlenek litu stosuje się do usuwania z powietrza w statkach kosmicznych.
A. Napisz równanie reakcji opisanej w zadaniu.
B. Oblicz masę , która może zostać pochłonięta przez wodorotlenku litu.
Ponadtlenek potasu powstaje w czasie spalania potasu w tlenie. Wiadomo, że w tym związku tlen występuje na ułamkowym stopniu utlenienia ().
Ułamkowy stopień utlenienia wynika z faktu, że suma stopni utlenienia wszystkich atomów wchodzących w skład związku chemicznego wynosi . Natomiast litowce w związkach chemicznych mają zawsze stopień utlenienia.
A. Napisz równanie reakcji spalania potasu w tlenie.
B. Ponadtlenek potasu reaguje z wodą. Napisz równanie reakcji i uzgodnij ją w oparciu o bilans elektronowy.
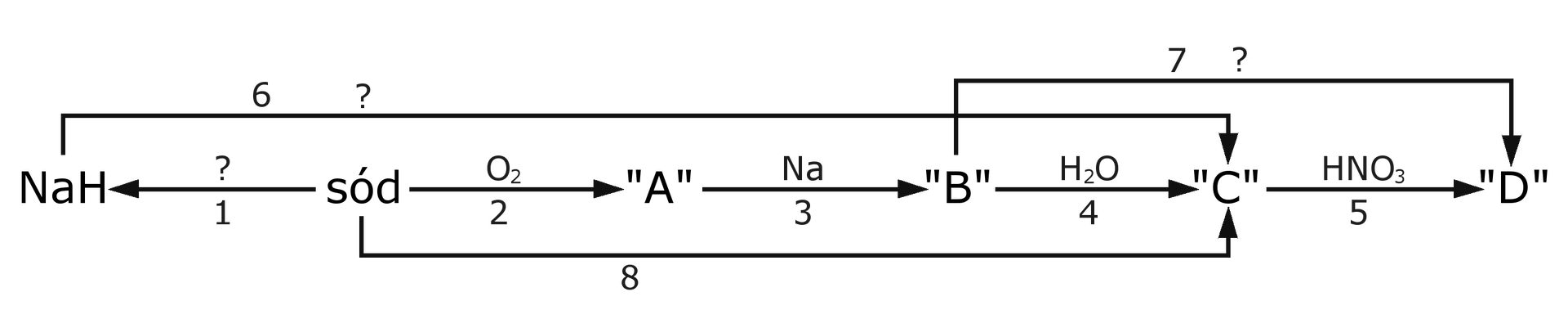
Za pomocą odpowiednich równań reakcji chemicznych zapisz przemiany przedstawione na poniższym schemacie.
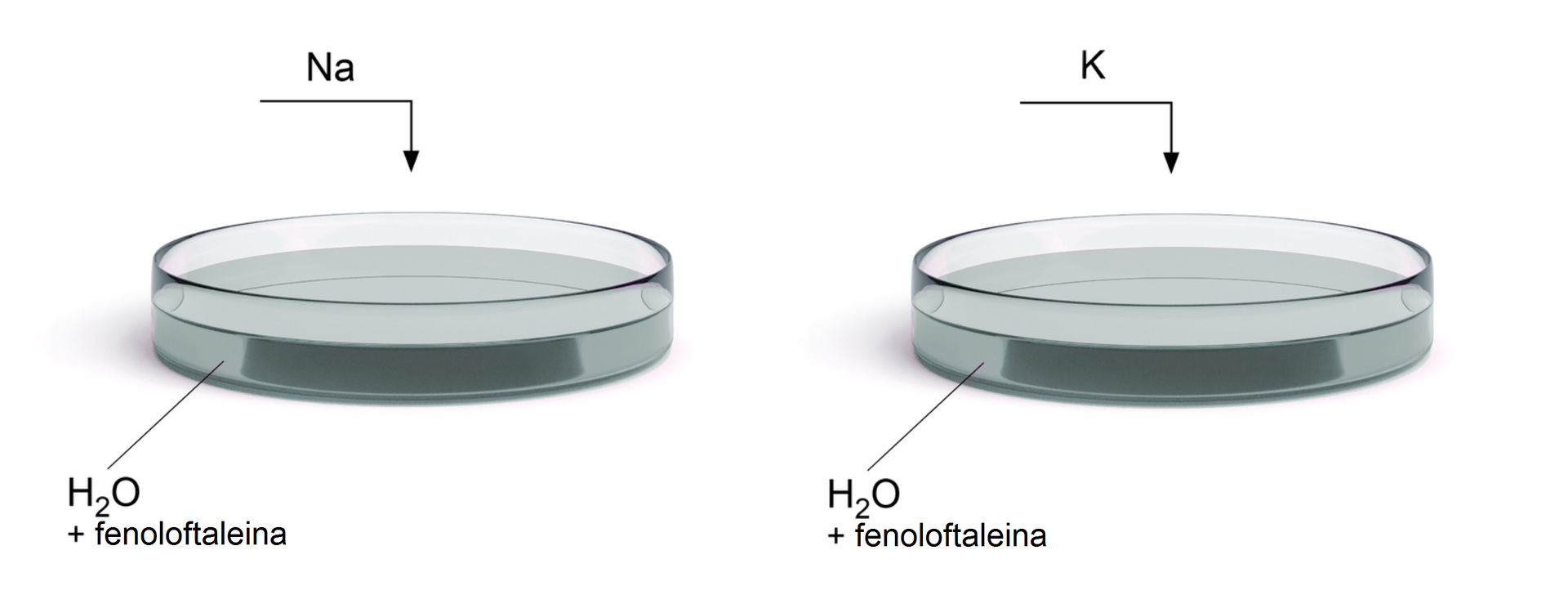
Zaprojektuj doświadczenie, którego celem jest porównanie aktywności sodu i potasu. W tym celu sporządź schematyczny rysunek, podaj obserwacje i wniosek.
Zapisz równania reakcji zaznaczonych na poniższym schemacie, podając warunki umożliwiające ich przebieg.