Węglowodory nienasycone‑alkeny- otrzymywanie
Otrzymywanie alkenów
Otrzymywanie alkenów z dihalogenopochodnych
W reakcjach eliminacji z dihalogenopochodnych alkanów istotne jest, aby atomy tego samego fluorowca były umieszczone na sąsiednich atomach węgla. O takich dihalogenopochodnych mówi się wówczas, że są to wicynalnewicynalne dihalogenowodory. Poniżej przedstawiono przykłady takich związków.
Uczniowie mieli za zadanie otrzymać w warunkach laboratoryjnych węglowodór nienasyconywęglowodór nienasycony, eten, oraz potwierdzić jego obecność. W tym celu przeprowadzili trzy równoległe eksperymenty.
Zapoznaj się z poniższymi informacjami, a następnie zaproponuj problem badawczy oraz hipotezę. Na podstawie opisu eksperymentów oraz obserwacji przedstawionych przez uczniów, sformułuj wniosek z doświadczeń oraz spróbuj zapisać równania reakcji chemicznych, które zaszły podczas doświadczeń. Do rozwiązania tego zadania wykorzystaj również inne źródła informacji, np. podręcznik.
Eksperyment 1.
Opis wykonania eksperymentu
W kolbie okrągłodennej, wyposażonej w mieszadło magnetyczne, umieszczono
1 g 1,2‑dichloroetanu w roztworze kwasu octowego (), a następnie dodano równomolową ilość metalicznego cynku.Kolbę zamknięto szczelnie korkiem z rurką odprowadzającą gazy, którą zanurzono w probówce zanurzonej w krystalizatorze z wodą.
Kolbę umieszczono na mieszadle z płaszczem grzejnym i rozpoczęto mieszanie zawartości w temperaturze 70°C.
W trakcie reakcji obserwowano zarówno kolbę, jak i zawartość probówki.
Po zakończeniu reakcji do probówki dodano nasycony roztwór manganianu(VII) potasu.
Obserwacje
W kolbie, po ochłodzeniu, osadziły się białe kryształki nieznanej substancji. W trakcie reakcji w probówce wydzielały się pęcherzyki bezbarwnego gazu, który nie rozpuszczał się w wodzie. Po dodaniu do probówki nasyconego roztworu manganianu(VII) potasu, roztwór zmienił barwę z fioletowej na bezbarwną, a w probówce wytrącił się brunatny osad.
Eksperyment 2.
Opis wykonania eksperymentu
W kolbie okrągłodennej, wyposażonej w mieszadło magnetyczne, umieszczono
1 g 1,2‑dichloroetanu w roztworze metanolu, a następnie dodano równomolową ilość sproszkowanego metalicznego cynku.Kolbę zamknięto szczelnie korkiem z rurką połączoną z probówką zanurzoną w krystalizatorze z wodą.
Kolbę umieszczono na mieszadle z płaszczem grzejnym i rozpoczęto mieszanie zawartości w temperaturze 70°C.
W trakcie reakcji obserwowano zarówno kolbę, jak i zawartość probówki.
Po zakończeniu reakcji, do probówki dodano nasycony roztwór manganianu(VII) potasu.
Obserwacje
W kolbie po ochłodzeniu osadziły się białe kryształki nieznanej substancji. W trakcie reakcji w probówce wydzielały się pęcherzyki bezbarwnego gazu, który nie rozpuszczał się w wodzie. Po dodaniu do probówki nasyconego roztworu manganianu(VII) potasu, roztwór zmienił barwę z fioletowej na bezbarwną, a w probówce wytrącił się brunatny osad.
Eksperyment 3.
Opis wykonania eksperymentu
W kolbie okrągłodennej wyposażonej w mieszadło magnetyczne umieszczono 1 g 1,2‑dichloroetanu i dodano etanol.
Kolbę zamknięto szczelnie korkiem z rurką połączoną z probówką zanurzoną w krystalizatorze z wodą.
Kolbę umieszczono na mieszadle magnetycznym i mieszano w ciągu dwóch godzin w temperaturze pokojowej.
W trakcie reakcji obserwowano zarówno kolbę, jak i zawartość probówki.
Po zakończeniu reakcji, do probówki dodano nasycony roztwór manganianu(VII) potasu.
Obserwacje
Nie zaobserwowano zmian w trakcie, jak i po reakcji z manganianem(VII) potasu.
Dibromoalkany mogą ulegać reakcji dehalogenacji zgodnie z mechanizmem eliminacjieliminacji, gdy zostaną poddane działaniu jodku sodu w roztworze propan‑2-onu (acetonu). Reakcja ta jest mniej popularna przy otrzymywaniu alkenów, natomiast częściej stosowana podczas otrzymywania alkinów. Spróbuj przeprowadzić omówioną reakcję w poniższym wirtualnym laboratorium.

W wirtualnym laboratorium możesz przeprowadzić doświadczenie, które pozwoli na otrzymanie alkenów z dihalogenopochodnych. Wiesz, w jakich warunkach zachodzi taka reakcja? Potrafisz wymienić potrzebne odczynniki? Po wykonaniu doświadczenia uzupełnij formularz.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D65CC4XVU
Otrzymywanie alkenów z alkoholi
Dehydratacja alkoholi jest jedną z reakcji eliminacji, w której pojedynczy substrat (alkohol) zostaje rozdzielony na dwa produkty. Innymi słowy alkohol przechodzi w alken, a produktem ubocznym reakcji dehydratacji jest woda. Poniżej przedstawiono mechanizm dehydratacji alkoholu.
Reakcja dehydratacji przebiega zgodnie z regułą Zajcewa, która mówi, że atom wodoru odrywa się od atomu węgla związanego z mniejszą liczbą atomów wodoru. Przykładowo:
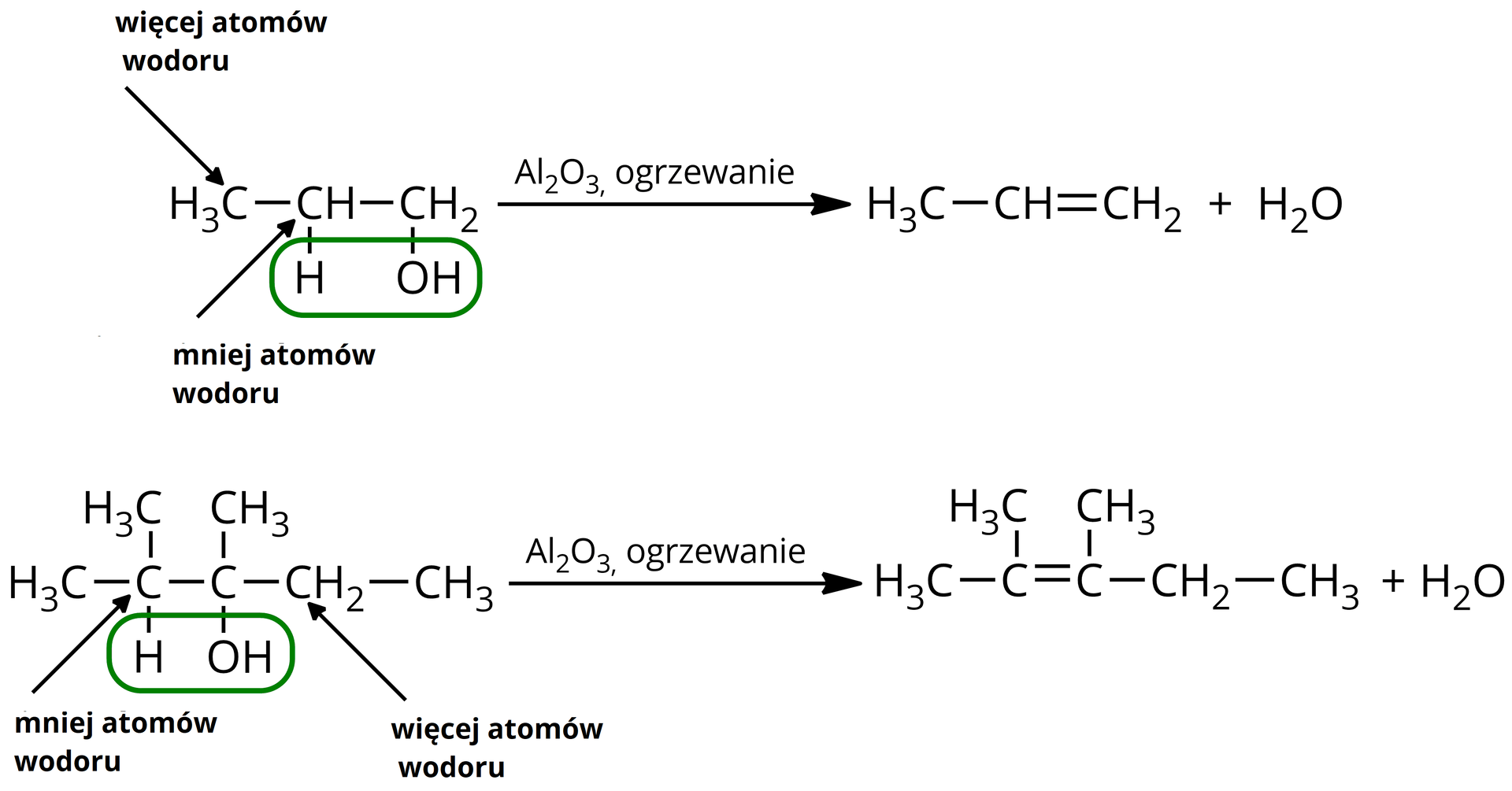
Otrzymywanie alkenów przez dehydratację alkoholi.
Myślisz, że wiesz już wszystko na temat dehydratacji alkoholi? Sprawdź swoją wiedzę, rozwiązując quiz. Gra składa się z trzech poziomów trudności. Aby przejść do następnego poziomu najpierw musisz zaliczyć poprzedni. Powodzenia!
Otrzymywanie alkenów przez dehydratację alkoholi.
Myślisz, że wiesz już wszystko na temat dehydratacji alkoholi? Sprawdź swoją wiedzę, rozwiązując quiz. Gra składa się z trzech poziomów trudności. Aby przejść do następnego poziomu najpierw musisz zaliczyć poprzedni. Powodzenia!
Zaznacz odpowiedź przedstawiającą produkty reakcji chemicznej przedstawionej poniżej:
Zaznacz odpowiedź przedstawiającą produkty opisanej reakcji chemicznej.

Otrzymywanie alkenów z chlorowcopochodnych
Jedną z głównych metod syntezy alkenów w warunkach laboratoryjnych jest reakcja eliminacji halogenków alkilowych, znana jako dehydrohalogenacja. W tym przypadku sąsiedztwo atomu chlorowca (chlor, brom, jod) ułatwia odłączanie się protonu od cząsteczki halogenoalkanu. Ostatecznie cząsteczka halogenopochodnej alkanu traci chlorowcowodór (), w efekcie czego powstaje alken. Chlorowcowodór z kationami, pochodzącymi od zasady, tworzy sól.

Warunki reakcji
Mechanizm reakcji:

Kolejność względnej reaktywności halogenku alkilu RX ( R – grupa alifatyczna) rośnie w szeregu:
Zatem szybciej uda się otrzymać alken z bromku niż z chlorku. W reakcji obserwuje się spadek reaktywności halogenku RX w szeregu:
Regioselektywność jest zwykle kontrolowana przez względną stabilność powstających alkenów.
Uprzywilejowanym produktem jest alken, który ma większą liczbę grup alkilowych przy atomach węgla, połączonych wiązaniem podwójnym.
Często uzyskuje się mieszaninę produktów, jednak przeważa produkt trwalszy (bardziej podstawiony).

Przeanalizuj poniższą symulację interaktywną. Sprawdź, w jaki sposób z 1,2‑dichloroetanu otrzymać eten. W tym celu umieść w probówce kilka kropel wody bromowej. Następnie do kolby okrągłodennej dwuszyjnej dodaj za pomocą pęsety cynk. Do wkraplacza wprowadź kolejno 1,2‑dichloroetan oraz etanol. Połącz probówkę z kolbą za pomocą gumowego wężyka, po czym dodaj całą zawartość wkraplacza do kolby i uruchom płaszcz grzejny. Obserwuj, co się stanie i rozwiąż ćwiczenia sprawdzające.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D65CC4XVU
Zapoznaj się z opisem symulacji interaktywnej, która dotyczy otrzymywania etenu z 1,2‑dichloroetanu, a następnie rozwiąż zadania sprawdzające.
Zadanie:
Synteza etenu z 1,2‑dichloroetanu.
Sprzęt laboratoryjny:
- probówka - podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
- statyw - prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
- pipety Pasteura - wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
- dwuszyjna kolba okrągłodenna - szklane naczynie laboratoryjne z zaokrąglonym dnem;
- pęseta - narzędzie o sprężystych ramionach używane do chwytania przedmiotów, których mały rozmiar utrudnia lub uniemożliwia manipulację za pomocą rąk;
- wkraplacz - naczynie laboratoryjne służące do precyzyjnego dozowania ciekłych substancji, zazwyczaj substratów do prowadzonej w kolbie reakcji chemicznej;
- gumowy korek - niewielki element wykonany z gumy, służący do szczelnego zamykania probówek;
- gumowy wężyk - element sprzętu laboratoryjnego o kształcie miękkiej rurki, służący do łączenia różnych urządzeń i transportowania między nimi gazów i cieczy;
- płaszcz grzejny - sprzęt laboratoryjny umożliwiający podgrzewanie kolb okrągłodennych i ich zawartości. Posiada półokrągłe wgłębienie, w którym umieszcza się kolbę okrągłodenną poddawaną ogrzewaniu.
Odczynniki chemiczne:
- 1,2‑dichloroetan;
- woda bromowa;
- cynk;
- etanol.
Wykonanie:
1. Umieszczono w probówce kilka kropel wody bromowej.
2. Do kolby okrągłodennej dwuszyjnej dodano za pomocą pęsety cynk.
3. Do wkraplacza wprowadzono kolejno 1,2‑dichloroetan oraz etanol.
4. Połączono probówkę z kolbą za pomocą gumowego wężyka, po czym dodano całą zawartość wkraplacza do kolby.
5. Uruchomiono płaszcz grzejny.
Obserwacje:
Woda bromowa w probówce uległa odbarwieniu.
Stosując wzory półstrukturalne związków organicznych, zapisz równanie reakcji chemicznej, która zachodzi po wprowadzeniu zawartości wkraplacza do wnętrza kolby okragłodennej dwuszyjnej.


