Wirtualne laboratorium – I
Przeprowadź doświadczenie w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Zachowanie alkoholi pierwszo-, drugo- i trzeciorzędowych wobec takich utleniaczy jak dichromian(VI) potasu w środowisku kwasowym
Szafa laboratoryjna
Przeprowadzono doświadczenie w laboratorium chemicznym. Zapoznaj się z opisem doświadczenia, a następnie wykonaj polecenia. Analiza doświadczenia: Zachowanie alkoholi pierwszo-, drugo- i trzeciorzędowych wobec takich utleniaczy, jak dichromian() potasu w środowisku kwasowym.
Problem badawczy: Czy produkt powstały w wyniku reakcji alkoholi z utleniaczem, takim jak w środowisku kwasu siarkowego(), zależy od rzędowości alkoholi?
Hipoteza: W wyniku reakcji alkoholi pierwszo-, drugo- i trzeciorzędowych z utleniaczami w środowisku powstają różne produkty.
Odczynniki: etanol, propan--ol, -metylopropan--ol, roztwór dichromianu() potasu roztwór kwasu siarkowego().
Szkło laboratoryjne
probówka – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
kolba kulista płaskodenna – szklane naczynie laboratoryjne o kształcie ściętej kuli od dołu; długa szyjka z nacięciem określa dokładnie określoną objętość kolby; pomimo kulistego kształtu można je stawiać na stole lub szafce;
kolba stożkowa – szklane naczynie laboratoryjne o kształcie stożka z płaskim dnem i wąską szeroką szyjką;
szalki Petriego – szklane spodki do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy;
lejek szklany – podstawowy sprzęt laboratoryjny, zazwyczaj w kształcie stożka zakończonego rurką lub szlifem, który służy do przelewania płynów, przesypywania proszków oraz do sączenia;
bagietka szklana – pręcik szklany, służący do mieszania cieczy
łyżka metalowa – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
łyżka do spalań – sprzęt laboratoryjny stosowany głównie w analizie jakościowej, ściślej płomieniowej wykonywany ze spieków ceramicznych lub wysokoodpornych termicznie stopów metali;
szczypce laboratoryjne – sprzęt przeznaczony do podtrzymywania drobnego sprzętu laboratoryjnego;
pipety Pasteura – wąskie rurki do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łapa drewniana – rodzaj trzymaka służący do uchwycenia probówki lub małej kolby stożkowej;
trójnóg z siatką – urządzenie w kształcie pierścienia, zaopatrzone w trzy wkręcane nogi, mocowane prostopadle do jego powierzchni, służące do ustawiania nad palnikiem naczyń laboratoryjnych, przeznaczonych do podgrzania;
palnik laboratoryjny – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych.
Przebieg doświadczenia:
Przygotowano trzy probówki i do każdej z nich wlano po dwa centymetry sześcienne roztworu dichromianu() potasu oraz dwa centymetry sześcienne roztworu kwasu siarkowego().
Następnie do każdej probówki dodano po dwa centymetry sześcienne innego alkoholu: etanolu, propan--olu, -metylopropan--olu.
Wstrząśnięto probówkami w celu wymieszania reagentów, a następnie ogrzano je w łaźni wodnej.
Obserwacje:
W probówce z etanolem i propan--olem po ogrzaniu zmienia się zabarwienie roztworu z pomarańczowego na zielony. W probówce z -metylopropan--olem roztwór nie zmienia koloru.
Wyniki:
Alkohole pierwszo- i drugorzędowe ulegają przeprowadzonej reakcji.
Wnioski:
Alkohole -rzędowe utleniają się do kwasów karboksylowych.
Alkohole -rzędowe utleniają się do ketonów.
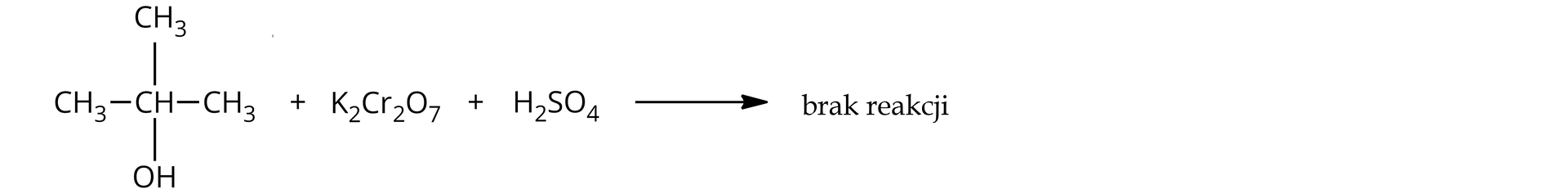
Alkohole -rzędowe nie ulegają reakcji utlenienia.