Wirtualne laboratorium – S
W poniższym wirtualnym laboratorium możesz się zapoznać z często używanym szkłem laboratoryjnym. Masz możliwość sprawdzenia, jak wykorzystywana jest chłodnica Liebiga. Klikając na nią, przenosisz się do laboratorium, w którym poznasz jej zastosowanie. Podobnie klikając na syntezę preparatu możesz zobaczyć, jak wykorzystywane jest szkło laboratoryjne podczas reakcji otrzymywania benzenu.
Dodatkowo poznasz wyposażenie apteczki, która znajduje się w każdym laboratorium. Zobaczysz, co zalicza się do środków ochrony osobistej, a co do środków ochrony zbiorowej.
Zobaczysz również, jaki sprzęt laboratoryjny ułatwia pracę podczas wykonywania doświadczeń. Możesz sprawdzić, kiedy przydaje się przyrząd do pomiaru temperatury topnienia. Klikając właśnie w ten przyrząd, przeniesiesz się do laboratorium, gdzie zadaniem jest sprawdzenie, jaka substancja znajduje się w słoiczku podpisanym , a jaka w słoiczku podpisanym . Powodzenia.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D1C6dj7d4
Zapoznaj się z dwoma przeprowadzonymi doświadczeniami, a następnie wykonaj polecenie.
Doświadczenie
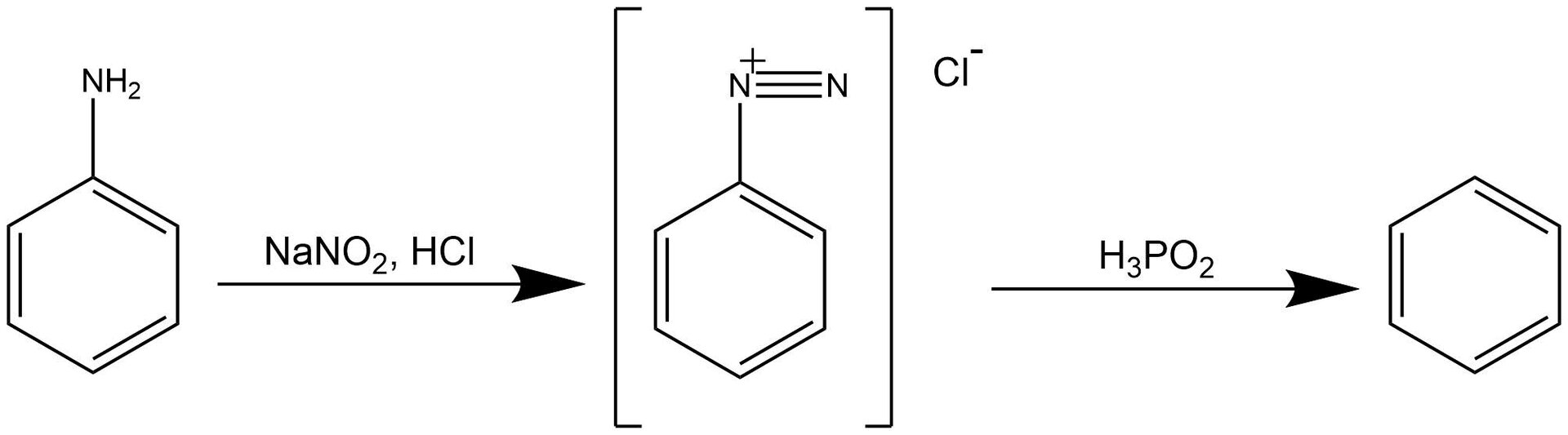
Analiza eksperymentu: Otrzymywanie benzenu.
Problem badawczy: Czy możliwe jest otrzymanie benzenu w reakcji z soli diazoniowej z trihydroksocynianem() sodu?
Hipoteza: Można otrzymać benzen w reakcji z soli diazoniowej z trihydroksocynianem() sodu.
Sprzęt laboratoryjny:
waga – urządzenie do odmierzania masy substancji chemicznych;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy;
pipety – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
kolba okrągłodenna – szklane naczynie laboratoryjne z zaokrąglonym dnem;
termometr ze szlifem – podłużny sprzęt laboratoryjny zawierający najczęściej skalę w stopniach Celsjusza oraz słup wypełniony rtęcią, który pod wpływem temperatury wskazuje pomiar;
płaszcz grzejny – urządzenie przeznaczone do prac laboratoryjnych i służy do podgrzewania różnego rodzaju cieczy;
chłodnica Liebiga – podłużne szkło laboratoryjne, wewnątrz którego znajduje się spiralna rurka, przez którą przepływa zimna woda schładzająca powstające podczas reakcji opary. Służy do skraplania gazów powstających podczas ogrzewania substancji;
kolba stożkowa – szklane naczynie laboratoryjne o kształcie stożka z płaskim dnem i wąską szeroką szyjką;
łaźnia lodowa – naczynie wypełnione lodem, służące do schładzania innych naczyń laboratoryjnych wraz z ich zawartością;
naczynko wagowe – sprzęt laboratoryjny służący do dokładnego odważania substancji stałych;
statyw – element sprzętu laboratoryjnego, rodzaj metalowego statywu służącego do montowania szklanej aparatury.
Odczynniki chemiczne:
anilina;
azotan() sodu;
kwas chlorowodorowy 35%;
wodorotlenek sodu;
chlorek cyny();
woda destylowana.
Przebieg eksperymentu:
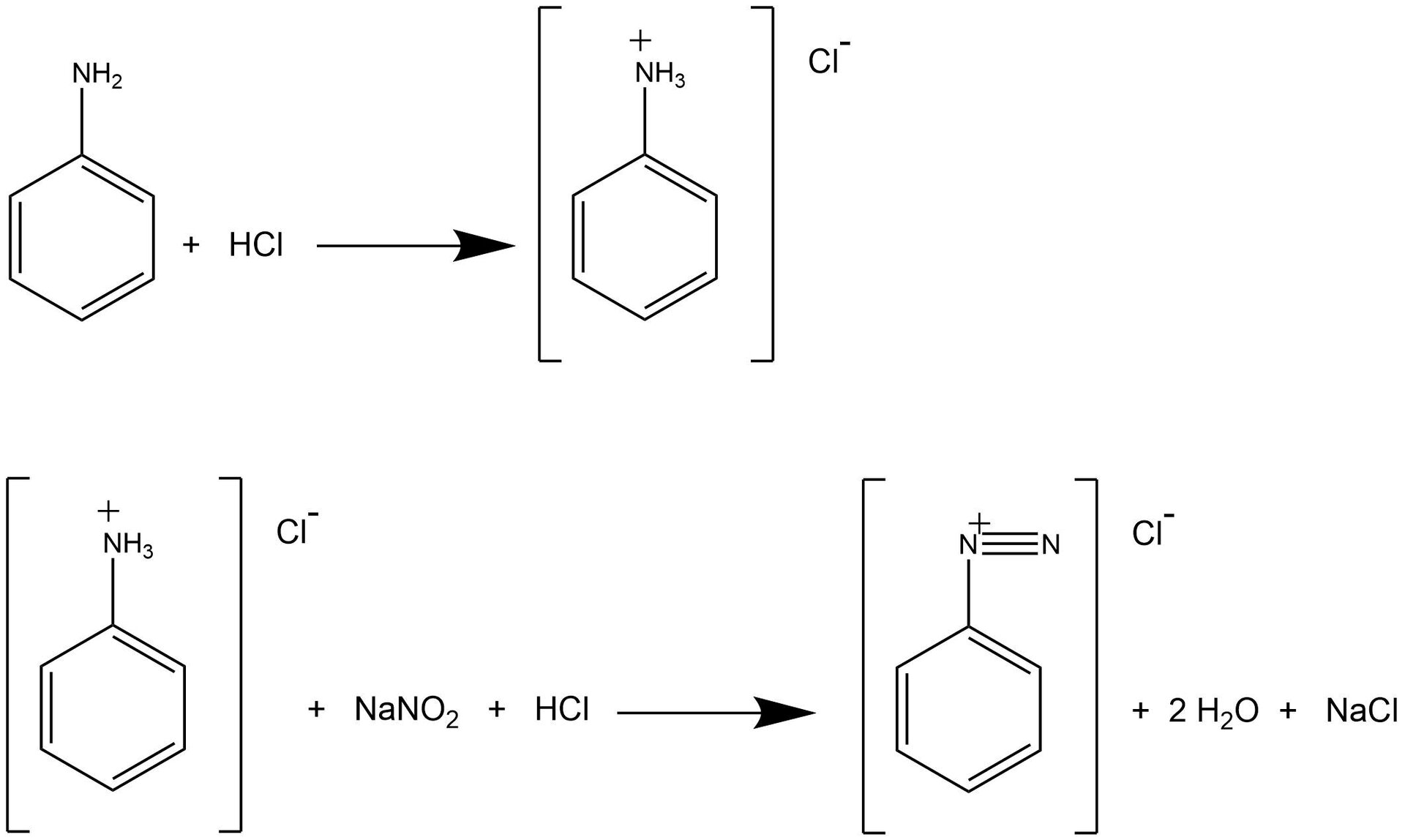
Dodano aniliny do kolby okrągłodennej, następnie stężonego kwasu chlorowodorowego.
Taką mieszaninę włożono do łaźni lodowej.
Kolejno dodano azotanu() sodu rozpuszczonego w wody.
chlorku cyny rozpuszczono w wody. Do sporządzonego roztworu dodano wodorotlenku sodu.
Do powstałego związku w kolbie okrągłodennej, dodawano małymi porcjami roztwór powstałego cynianu() sodu.
Po zakończeniu reakcji, przeprowadzono destylację prostą powstałego roztworu. Pierwszym zebranym produktem był spodziewany produkt.
Obserwacje:
Po dodaniu azotanu() sodu, mieszanina przybiera kolor pomarańczowy. Otrzymany produkt to bezbarwna ciecz.
Wyniki:
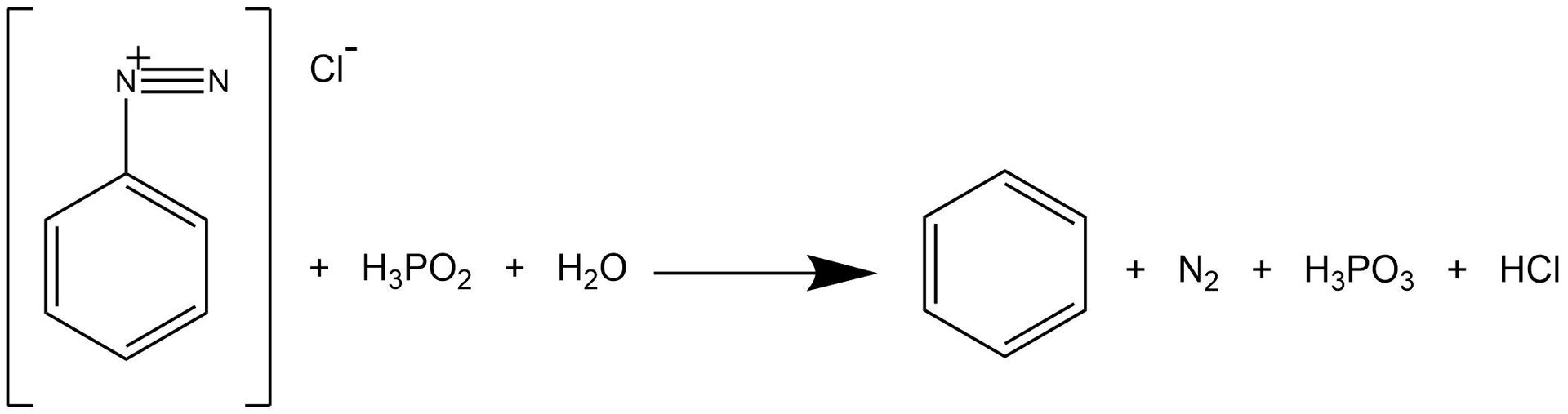
W wyniku reakcji otrzymano benzen.
Wnioski:
W wyniku reakcji aniliny z azotanem() sodu otrzymano jasnożółtą ciecz – jest to benzen. Hipoteza została potwierdzona.
Doświadczenie
Analiza eksperymentu: Wykorzystanie przyrządu do pomiaru temperatury topnienia.
Problem badawczy: Jak najłatwiej odróżnić dwie substancje: kwas benzoesowy od salicylowego?
Hipoteza: Badane kwasy posiadają różne temperatury topnienia.
Sprzęt laboratoryjny:
probówki w statywie – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
palnik – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych;
krystalizator z wodą – płaskie naczynie laboratoryjne, które służy do procesu krystalizacji;
przyrząd do pomiaru temperatury topnienia
uniwersalne papierki wskaźnikowe – kawałek bibuły najczęściej w kształcie paska, nasączony roztworem substancji chemicznej będącej indykatorem i wysuszony;
drewniana łapa do probówek – rodzaj trzymaka, służący do uchwycenia probówki lub małej kolby stożkowej.
Odczynniki chemiczne:
eter dietylowy;
etanol;
woda destylowana.
Przebieg eksperymentu:
Zbadano rozpuszczalność substancji oraz w zimnej wodzie. Następnie sprawdzono rozpuszczalność tych substancji, ale po ogrzaniu. W tym celu probówki z badanymi substancjami (, ) oraz wodą ogrzano w łaźni wodnej.
Sprawdzono odczyn badanych roztworów za pomocą papierka uniwersalnego.
Zbadano rozpuszczalność substancji oraz w eterze dietylowym oraz w etanolu.
Sprawdzono temperaturę topnienia badanych substancji.
Obserwacje:
Badane substancje oraz to białe ciała stałe, nierozpuszczalne w zimnej wodzie, lecz po podgrzaniu. Uniwersalne papierki wskaźnikowe zmieniły barwę z żółtej na czerwoną w obu przypadkach. Substancje rozpuszczają się w eterze dietylowym oraz w etanolu; różnią się temperaturą topnienia.
Wyniki:
Czerwona barwa uniwersalnych papierków wskaźnikowych świadczy o kwasowym odczynie roztworów obu substancji. Związek posiada temperaturę topnienia , natomiast .
Wnioski:
Związek to kwas benzoesowy, a związek to kwas salicylowy. Hipoteza została potwierdzona.