Alkohole polihydroksylowe
Alkohole polihydroksylowe
Do alkoholi polihydroksylowych zalicza się m.in. diole, alkohole mające w cząsteczce dwie grupy hydroksylowe, i triole, alkohole z trzema grupami hydroksylowymi. Wyróżnia się również alkohole z grupy cukrolicukroli, które posiadają więcej niż trzy grupy hydroksylowe.
Gliceryna (glicerol, propano‑1,2,3‑triol)1
Glikol etylenowy (etano‑1,2‑diol)
Alkohole polihydroksylowe, tak jak alkohole monohydroksylowe:
nie ulegają dysocjacji elektrolitycznej;
nie przewodzą prądu elektrycznego;
odczyn ich wodnych roztworów jest obojętny.
Właściwości fizyczne alkoholi polihydroksylowych
Zapoznaj się z filmem, a dowiesz się, w jaki sposób ilość grup hydroksylowych wpływa na właściwości fizyczne związku chemicznego.

Film dostępny pod adresem /preview/resource/RxIQgXyf1mtwB
Film nawiązujący do treści materiału dotyczącej wpływu obecności większej liczby grup hydroksylowy w cząsteczkach na ich właściwości fizyczne.
Przeanalizuj poniższy wykres i wyjaśnij, jak zmienia się temperatura wrzenia i topnienia alkoholi polihydroksylowych w szeregu homologicznym.
Do wyjaśnienia tego problemu skorzystaj również z innych źródeł informacji.
- 1. zestaw danych:
- Alkohol: glikol etylenowy
- Temperatura topnienia[°C]: -13; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 197; Podpis osi wartości: Temperatura (°C)
- 2. zestaw danych:
- Alkohol: gliceryna
- Temperatura topnienia[°C]: 18; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 290; Podpis osi wartości: Temperatura (°C)
- 3. zestaw danych:
- Alkohol: erytrytol
- Temperatura topnienia[°C]: 118; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 329; Podpis osi wartości: Temperatura (°C)
- 4. zestaw danych:
- Alkohol: ksylitol
- Temperatura topnienia[°C]: 94; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 216; Podpis osi wartości: Temperatura (°C)
- 5. zestaw danych:
- Alkohol: sorbitol
- Temperatura topnienia[°C]: 96; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 296; Podpis osi wartości: Temperatura (°C)
- 6. zestaw danych:
- Alkohol: perseitol
- Temperatura topnienia[°C]: 185; Podpis osi wartości: Temperatura (°C)
- Temperatura wrzenia[°C]: 272; Podpis osi wartości: Temperatura (°C)
Właściwości chemiczne alkoholi polihydroksylowych
Alkohole polihydroksylowe ulegają tym samym reakcjom chemicznym, co alkohole monohydroksylowe:
reagują z metalami aktywnymi
W wyniku reakcji etano-,-diolu z sodem powstaje etano-,-diolan sodu i wodór:

ulegają dehydratacji pod wpływem środowiska kwasowego
W wyniku reakcji etano-,-diolu w środowisku kwasowym powstaje acetaldehyd i woda:

Odróżnianie alkoholi polihydroksylowych od monohydroksylowych
Alkohole monohydroksylowe można odróżnić od alkoholi polihydroksylowych za pomocą reakcji z wodorotlenkiem miedzi(II). Pozytywny wynik tej reakcji obserwuje się w przypadku alkoholi polihydroksylowych, w których występują co najmniej dwie grupy –OH przy sąsiadujących atomach węgla. Przeprowadż opisaną reakcję w poniższym laboratorium i wykonaj ćwiczenia.
Przeprowadź doświadczenie w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Szafa laboratoryjna
Analiza doświadczenia: Odróżnianie alkoholu monohydroksylowego od polihydroksylowego.
Problem badawczy: W jaki sposób można odróżnić alkohol monohydroksylowy od polihydroksylowego?
Hipoteza: Za pomocą próby Trommera można odróżnić alkohol monohydroksylowy od polihydroksylowego.
Odczynniki chemiczne: gliceryna (propano-,,-triol), siarczan miedzi – woda , wodorotlenek sodu, etanol, woda destylowana.
Sprzęt laboratoryjny:
dwie zlewki – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
dwie probówki – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Przebieg doświadczenia:
Przygotowano w dwóch zlewkach -molowy roztwór wodorotlenku sodu oraz -molowy roztwór siarczanu miedzi. Masa molowa hydratu wynosi . Masa molowa jest równa .
Otrzymano wodorotlenek miedzi. W tym celu: przygotowano dwie probówki. Wlano do obu probówek po 5 centymetrów sześciennych -molowego roztworu wodorotlenku sodu. Następnie wlano do obu probówek kilka kropli -molowego roztworu siarczanu miedzi.
Do otrzymanego osadu w probówce numer 1 wlano 3 centymetry sześcienne propano-,,-triolu i wstrząśnięto.
Do drugiej probówki wlano 3 centymetry sześcienne etanolu i wstrząśnięto probówką.
Obserwacje:
Przygotowany wodorotlenek miedzi wytrącił się w postaci galaretowatego niebieskiego osadu. W probówce z gliceryną następuje zmiana zabarwienia z błękitnego na szafirowy oraz roztworzenie osadu wodorotlenku miedzi. W probówce z etanolem nie zaobserwowano objawów reakcji – wciąż widoczny jest niebieski osad.
Wyniki:
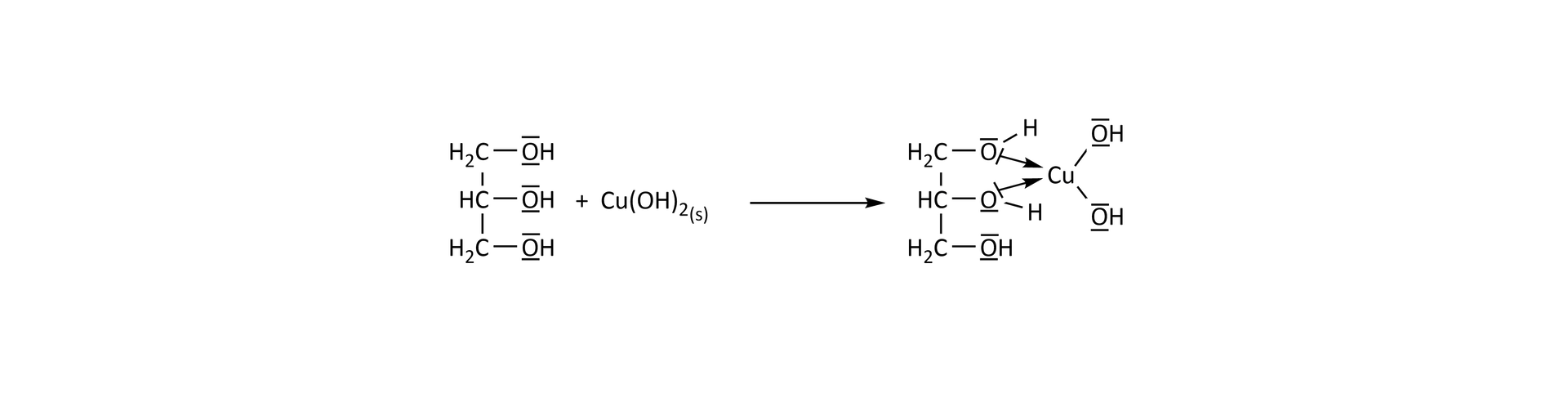
Gliceryna reaguje z wodorotlenkiem miedzi tworząc glicerynian miedzi. Grupy hydroksylowe gliceryny są donorami par elektronowych. Między tymi grupami a atomami miedzi powstają wiązania koordynacyjne. Utworzony kompleks jest łatwo rozpuszczalny w wodzie.
Wnioski:
Jest to reakcja charakterystyczna dla alkoholi polihydroksylowych. Etanol jest alkoholem monohydroksylowym i nie reaguje z wodorotlenkiem miedzi. Za pomocą próby Trommera można odróżnić alkohol monohydroksylowy od polihydroksylowego – hipoteza potwierdziła się.
Zaznacz wzory półstrukturalne alkoholi, które po dodaniu do świeżo strąconego wodorotlenku miedzi spowodują jego roztworzenie, a roztwór przyjmie szafirowe zabarwienie.
Poniższy schemat przedstawia moment doświadczenia, w którym drugi z reagentów nie został jeszcze dodany do probówki. Pod każdą probówką umieść odpowiednie obserwacje po dodaniu drugiego reagenta.