Jak przebiega proces rozpuszczania i co to jest rozpuszczalność?
Rozpuszczanie
Substancje stałe, ciekłe lub gazowe różnią się zdolnościami do tworzenia z innymi substancjami układów homogenicznychukładów homogenicznych. Rozpuszczanie to fizyczny proces mieszania się dwóch substancji, prowadzący do otrzymania roztworu.
Efekty towarzyszące procesowi rozpuszczania to np. zmiana temperatury i zmiana objętości roztworu (zjawisko dylatacji dylatacji lub kontrakcjikontrakcji). W czasie rozpuszczania następuje solwatacja, czyli otaczanie cząsteczek (lub jonów) substancji rozpuszczonej przez cząsteczki rozpuszczalnika. Solwatację w roztworach wodnych nazywamy hydratacją.


Proces rozpuszczania nie odnosi się jedynie do cieczy i gazów. Przykładem są amalgamaty otrzymywane poprzez rozpuszczenie metali w ciekłej rtęci. Ponieważ większość metali jest rozpuszczalna w rtęci, amalgamaty znalazły zastosowanie w kopalniach złota. Dlaczego? Główną trudnością podczas wydobywania złota jest oddzielanie bardzo małych cząstek czystego złota od ton kruszonej skały. Jednym ze sposobów na osiągnięcie tego jest mieszanie zawiesiny pokruszonej skały z ciekłą rtęcią, która rozpuszcza złoto (a także wszelkie metaliczne srebro, które może być obecne). Bardzo gęsty płynny amalgamat złoto‑rtęć jest następnie izolowany, a rtęć oddestylowana.
Rozpuszczalniki
Rozpuszczalniki podzielić można:
ze względu na budowę cząsteczek na:
ciecze polarne, w których rozpuszczają się cząsteczki dipolowe oraz związki jonowe;
ciecze niepolarne, rozpuszczające cząsteczki, które nie są dipolami.
ze względu na własności chemiczne na:
protonowe (protyczne) – zawierające w swojej strukturze tzw. kwaśne protony, które mogą ulec oderwaniu przez cząsteczkę zasady, a także brać udział w tworzeniu wiązań wodorowych;
aprotonowe (aprotyczne) – w strukturze nie posiadające „kwaśnych” protonów.
Reasumując, wszystkie rozpuszczalniki protonowe są też polarne, natomiast aprotonowe mogą być zarówno polarne, jak i niepolarne. Co ostatecznie daje trzy główne grupy rozpuszczalników:
protonowe,
aprotonowe polarne,
aprotonowe niepolarne.
Rozpuszczalniki polarne
Najbardziej popularnym i najczęściej stosowanym rozpuszczalnikiem jest woda. Cechuje ją mała lepkość, dzięki czemu łatwo penetruje rozpuszczaną substancję oraz stosunkowo niska temperatura wrzenia (około ), dzięki czemu można ją łatwo oddestylować bądź odparować z roztworu. Cząsteczka wody ma tę niezwykłą właściwość, że na skutek jej działania, wiązania spolaryzowane lub jonowe innych związków chemicznych ulegają rozerwaniu i substancja rozpada się (dysocjuje) na jony. Wynika to z faktu, że w cząsteczce wody występują wiązania kowalencyjne (atomowe) spolaryzowane (różnica elektroujemności pomiędzy tlenem a wodorem wynosi ). Bardziej elektroujemny atom (tlen) stanowi biegun ujemny, a mniej elektroujemny (wodór) biegun dodatni. Cząsteczka wody posiada zatem dwa bieguny (dodatni i ujemny) i o takiej cząsteczce mówimy, że jest dipolem.
Czy wszystkie kryształy rozpuszczają się w wodzie? Przeprowadź eksperyment w laboratorium chemicznym. Zweryfikuj własną hipotezę. Uzupełnij potrzebny sprzęt oraz odczynniki i zapisz instrukcję wykonania. W formularzu zanotuj swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Zachowanie się kryształów o różnej budowie wobec rozpuszczalników polarnych (woda)
Szafa laboratoryjna
Analiza eksperymentu: Zachowanie się kryształów o różnej budowie wobec rozpuszczalników polarnych (woda).
Problem badawczy: Czy wszystkie typy kryształów rozpuszczają się w rozpuszczalnikach polarnych?
Hipoteza: Wszystkie typy kryształów rozpuszczają się w rozpuszczalnikach polarnych.
Sprzęt laboratoryjny: cztery zlewki () – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych; bagietka – sprzęt laboratoryjny o kształcie prostego pręta szklanego, czasami zakończonego z jednej strony małą rączką, a z drugiej małą łopatką. Służy do mieszania cieczy; łyżka laboratoryjna – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych; pipety Pasteura – wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki; waga laboratoryjna – urządzenie elektryczne służące do wyznaczania mas substancji. Daną substancję umieszcza się na srebrnej tacy umieszczonej na urządzeniu. Masa ważonej substancji wyświetlana jest na wyświetlaczu.
Odczynniki chemiczne: chlorek sodu (sól kuchenna); cukier spożywczy (sacharoza); fosfor czerwony; węgiel (grafit); woda destylowana.
Przebieg eksperymentu: Odmierzono za pomocą wagi po substancji i wsypano do zlewek zgodnie z poniższymi punktami:
do zlewki 1. – chlorek sodu;
do zlewki 2. – sacharoza;
do zlewki 3. – fosfor czerwony;
do zlewki 4. – grafit.
Następnie za pomocą pipet Pasteura odmierzono po wody destylowanej i wlano do każdej ze zlewek. Zawartość każdej zlewki wymieszano dokładnie za pomocą bagietki.
Obserwacje: Kryształy chlorku sodu i sacharozy rozpuściły się w wodzie, zaś kryształy fosforu i grafitu nie uległy rozpuszczeniu. Wyniki: Nie wszystkie badane typy kryształów uległy rozpuszczeniu w rozpuszczalniku polarnym.
Wnioski: Kryształy jonowe (chlorek sodu) oraz kryształy molekularne (sacharoza) ulegają rozpuszczeniu w rozpuszczalnikach polarnych. Kryształy kowalencyjne (fosfor, grafit) nie posiadają takiej zdolności. Hipoteza została obalona – nie wszystkie typy kryształów rozpuszczają się w rozpuszczalnikach polarnych.
Podstawową regułą rządząca zjawiskiem rozpuszczania jest reguła stwierdzająca, że podobne rozpuszcza się (miesza się) w podobnym (łac. „similia similibus solventur”). Przez „podobne” rozumiemy tu przede wszystkim polarność cząsteczek mieszających się w roztworze.
Etapy procesu rozpuszczania
Proces rozpuszczania substancji krystalicznej w ciekłym rozpuszczalniku przebiega w kilku etapach, które zostały przedstawione w poniższej tabeli. Poszczególne etapy mogą być procesami egzoenergetycznymiegzoenergetycznymi lub endoenergetycznymiendoenergetycznymi.
Etapy procesu rozpuszczania | Charakterystyka energetyczna etapów procesu rozpuszczania | Typ procesu pod względem energetycznym |
|---|---|---|
Pokonanie oddziaływań w substancji rozpuszczanej (rozdzielanie jonów lub cząsteczek). | Energia (EIndeks dolny 11) jest pobierana z otoczenia, aby pokonać siły (jonowe w sieci krystalicznej lub międzycząsteczkowe) spajające drobiny substancji rozpuszczanej. | proces endoenergetyczny |
Niszczenie oddziaływań międzycząsteczkowych w rozpuszczalniku | Energia (EIndeks dolny 22) potrzebna do zniszczenia oddziaływań międzycząsteczkowych w rozpuszczalniku jest przekazana z otoczenia do układu. | proces endoenergetyczny |
Powstanie oddziaływań między indywiduami substancji rozpuszczonej a cząsteczkami rozpuszczalnika | Energia (EIndeks dolny 33) jest uwalniana do otoczenia na skutek powstawania nowych oddziaływań między drobinami substancji rozpuszczanej a cząsteczkami rozpuszczalnika. | proces egzoenergetyczny |
Rozpuszczanie stałego w wodzie jest procesem, któremu towarzyszy podwyższenie temperatury układu, gdyż:
Rozpuszczanie stałego w wodzie jest natomiast procesem, któremu towarzyszy obniżenie temperatury układu, gdyż:
Roztwory właściwe

Roztworem nasyconymRoztworem nasyconym nazywamy roztwór, w którym nie można już rozpuścić więcej substancji, a jej nadmiar znajduje się w stanie równowagi dynamicznej z roztworem. Analogicznie, roztworem nienasyconym nazywamy taki, w którym można rozpuścić dodatkową ilość danej substancji.
Rozpuszczalność
Rozpuszczalność jest cechą danej pary substancji rozpuszczanej i rozpuszczalnika w określonej temperaturze. Na ogół ilość substancji, którą można rozpuścić w danej ilości rozpuszczalnika i w określonej temperaturze, jest ograniczona i prowadzi do uzyskania tzw. roztworu nasyconegoroztworu nasyconego. Ilość substancji niezbędnej do uzyskania roztworu nasyconego określa wielkość fizyczna zwana rozpuszczalnością.
Rozpuszczalność substancji zależy od:
rodzaju substancji rozpuszczonej;
rodzaju rozpuszczalnika;
temperatury (rozpuszczalność większości ciał stałych i cieczy rośnie wraz ze wzrostem temperatury, a rozpuszczalność gazów maleje);
ciśnienia – tylko dla gazów (ich rozpuszczalność rośnie wraz ze wzrostem ciśnienia oraz od wpływu wspólnego jonu);
Rozpuszczalność to liczba gramów danej substancji niezbędna do nasycenia 100 g rozpuszczalnika w danej temperaturze.
Poniższa tabela przedstawia rozpuszczalność wybranych substancji w 100 g wody i w temperaturze 25ºC.
Sól | Rozpuszczalność |
|---|---|
Rozpuszczalność gazów
Przeanalizuj poniższą symulację. Zwróć uwagę, jak zmiana temperatury oraz ciśnienia wpływa na rozpuszczalność tlenku węgla() w wodzie. Następnie rozwiąż ćwiczenia sprawdzające.
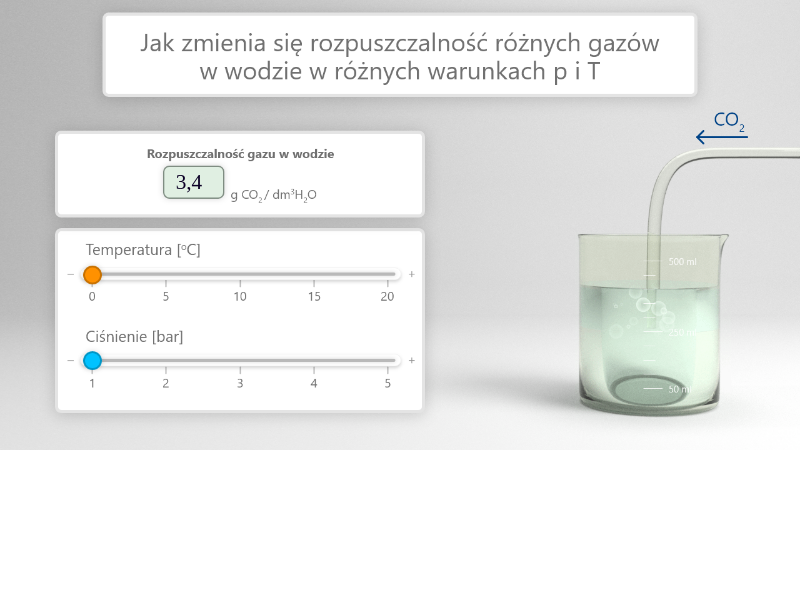
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DFU8FRGC7
Rozpuszczalność gazów zależy od ciśnienia i rośnie wraz z jego wzrostem. Podobnie jak różny wpływ wywiera temperatura na rozpuszczalność, tak wzrost ciśnienia może powodować znaczne zwiększenie rozpuszczalności, tak jak dla dwutlenku węgla, bądź nie powodować tak dużych zmian, jak w przypadku tlenu.
