Zależność rozpuszczalności substancji od temperatury - krzywa rozpuszczalności
Rozpuszczalność jest to maksymalna liczba gramów substancji, jaką można w 100 g rozpuszczalnika w danej temperaturze i pod stałym ciśnieniem.
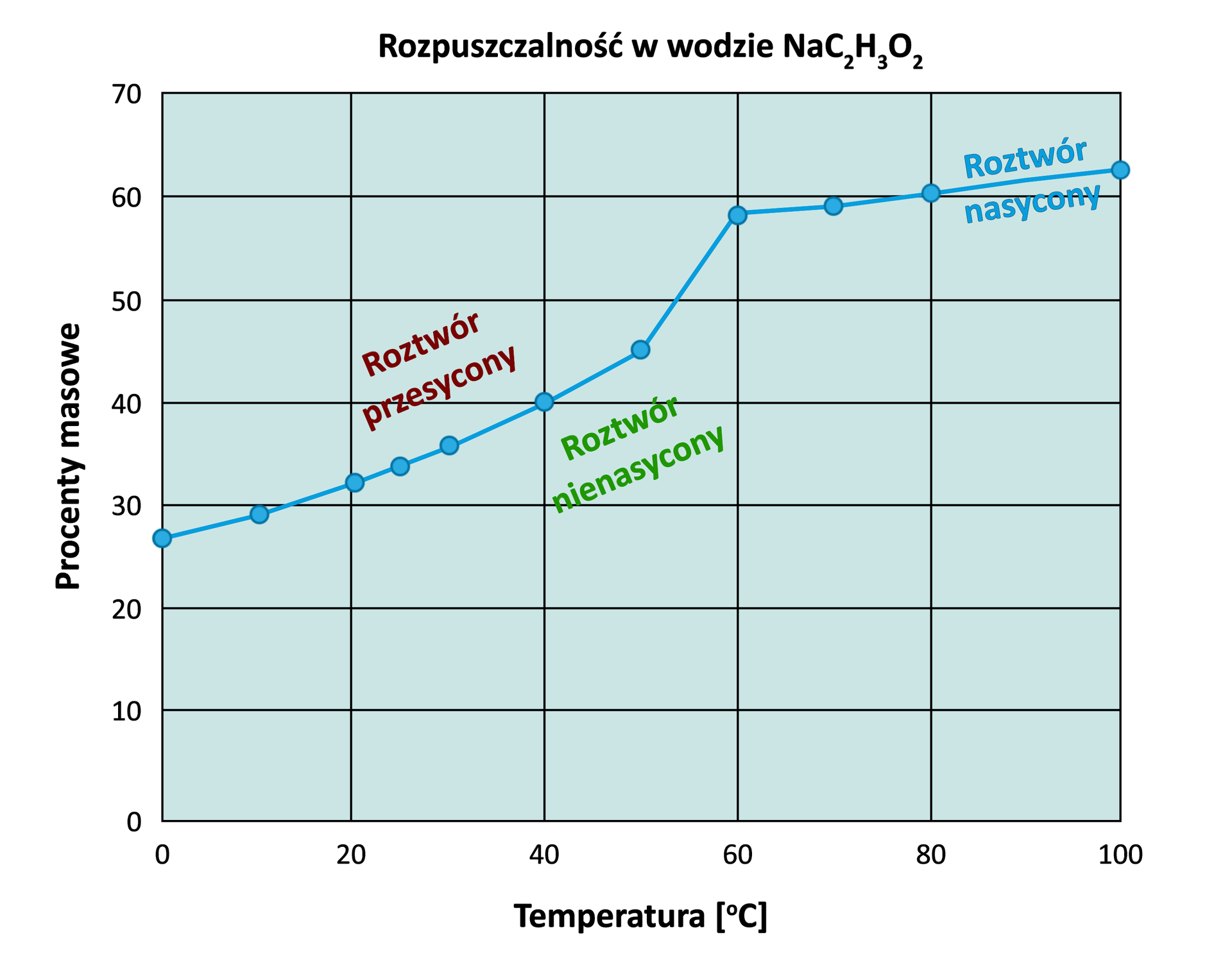
Roztwór nasycony to taki, w którym w danej temperaturze nie można rozpuścić już więcej danej substancji.
Za dobrze rozpuszczalne w wodzie przyjmuje się te substancje, których rozpuszczalność wynosi ponad 1 g na 100 g rozpuszczalnika (wody). Substancje, których rozpuszczalność wynosi mniej niż 0,1 g w 100 g wody uznaje się za praktycznie nierozpuszczalne.
Czym jest krzywa rozpuszczalności i jak odczytać z niej rozpuszczalność substancji?
Wykres przedstawiający zależność rozpuszczalności danej substancji od temperatury nazywa się krzywą rozpuszczalności.
Odczytaj z wykresu rozpuszczalność chlorku sodu () w temperaturze 90°C przy stałym ciśnieniu.
Zapoznaj się z opisem wykresu. Dowiesz się, jaka jest rozpuszczalność chlorku sodu (NaCl) w temperaturze 90°C przy stałym ciśnieniu.
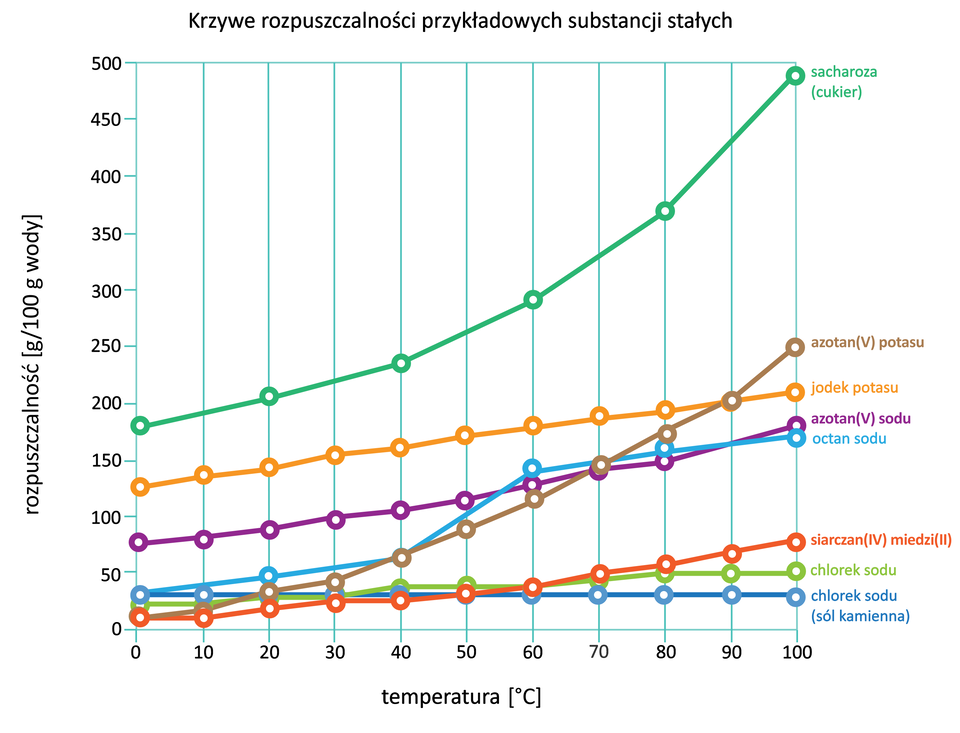
Interpretacja danych z wykresu rozpuszczalności
Ile gramów azotanu(V) sodu należy rozpuścić w 100 g wody, aby w temperaturze 40°C otrzymać roztwór nasycony?

Stan równowagi dynamicznej
Czy potrafisz wyjaśnić, czym jest roztwór nasycony? Czy umiesz powiedzieć, na czym polega stan równowagi w roztworze nasyconym? Zapoznaj się z poniższą animacją i wykonaj zadania.

Film dostępny pod adresem /preview/resource/RFynzNWQT4MSp
Film nawiązujący do treści materiału dotyczącej stanu równowagi dynamicznej w roztworze nasyconym.
Wyjaśnij, czym jest roztwór nasycony.
Czy w roztworze nienasyconym istnieje równowaga dynamiczna?
Co oznacza, że roztwór jest w stanie równowagi dynamicznej?
Jak sprawdzić, czy roztwór jest nasycony?
Czy roztwór otrzymany przez rozpuszczenie 200 g w 150 g wody będzie w temperaturze 70°C roztworem nasyconym?
Rozpuszczalność gazów w cieczach zależy od rodzaju rozpuszczalnika (gazy zazwyczaj lepiej rozpuszczają się w rozpuszczalnikach organicznych) i temperatury – rozpuszczalność gazów w cieczach maleje wraz ze wzrostem temperatury.
Już wiesz, w jaki sposób odczytać wartość rozpuszczalności danej substancji z krzywej rozpuszczalności? Czy wiesz zatem, w jaki sposób obliczyć stężenie substancji na jej podstawie? Zapoznaj się z poniższym filmem, spróbuj samodzielnie wykonać przedstawione w nim zadanie, a następnie rozwiąż ćwiczenia zamieszczone pod filmem.

Film dostępny pod adresem /preview/resource/REx2wn2JacNJ5
Film nawiązujący do treści materiału - dotyczy rozpuszczalności soli i gazów w zależności od temperatury, roztworów nasyconych i nienasyconych oraz rozwiązania zadania.
Na liniowym wykresie interaktywnym przedstawiono rozpuszczalność poniższych soli (w na wody). Krzywe rozpuszczalności dla każdej z soli zostały oznaczone innym kolorem.
azotan() potasu (linia czerwona):
–
–
–
–
–
–
–
–
–
–
–
jodek potasu (linia jasnozielona):
–
–
–
–
–
–
–
–
–
–
–
chlorek sodu (sól kuchenna) (linia pomarańczowa):
–
–
–
–
–
–
–
–
–
–
–
chlorek potasu (linia niebieska):
–
–
–
–
–
–
–
–
–
–
–
azotan() sodu (linia fioletowa):
–
–
–
–
–
–
–
–
–
–
–
Na liniowym wykresie interaktywnym przedstawiono rozpuszczalność poniższych soli (w na wody). Krzywe rozpuszczalności dla każdej z soli zostały oznaczone innym kolorem.
octan sodu (linia pomarańczowa):
–
–
–
–
–
–
sacharoza (cukier) (linia żółtopomarańczowa):
–
–
–
–
–
–
szczawian amonu (linia żółtozielona):
–
–
–
–
–
–
W temperaturze równej rozpuszczalność jodku potasu wynosi , co można zapisać jako ). Co oznacza ten zapis? Wybierz prawidłową odpowiedź.
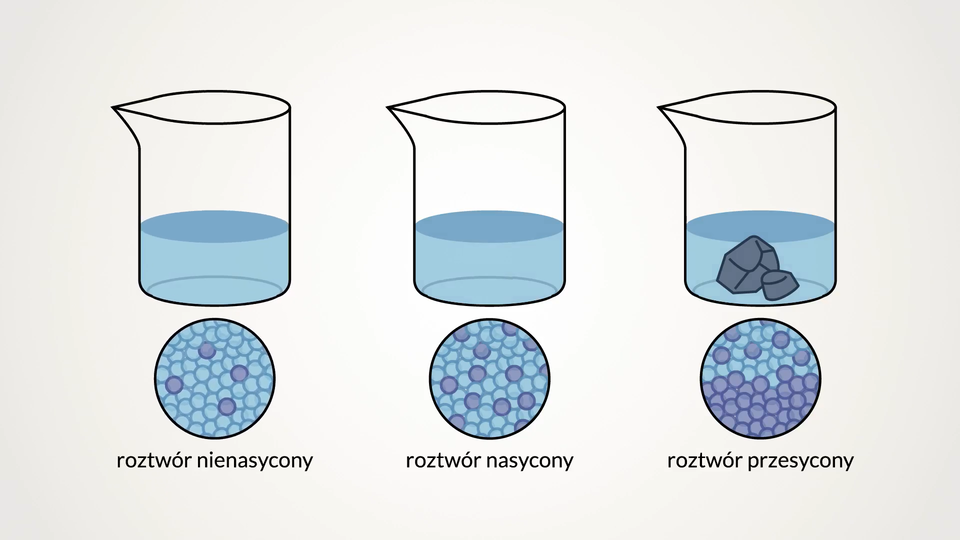
Przygotowanie roztworu nasyconego i przesyconego
Napisz, skąd wiadomo, jaką ilość substancji należy rozpuścić, aby otrzymać roztwór nasycony?
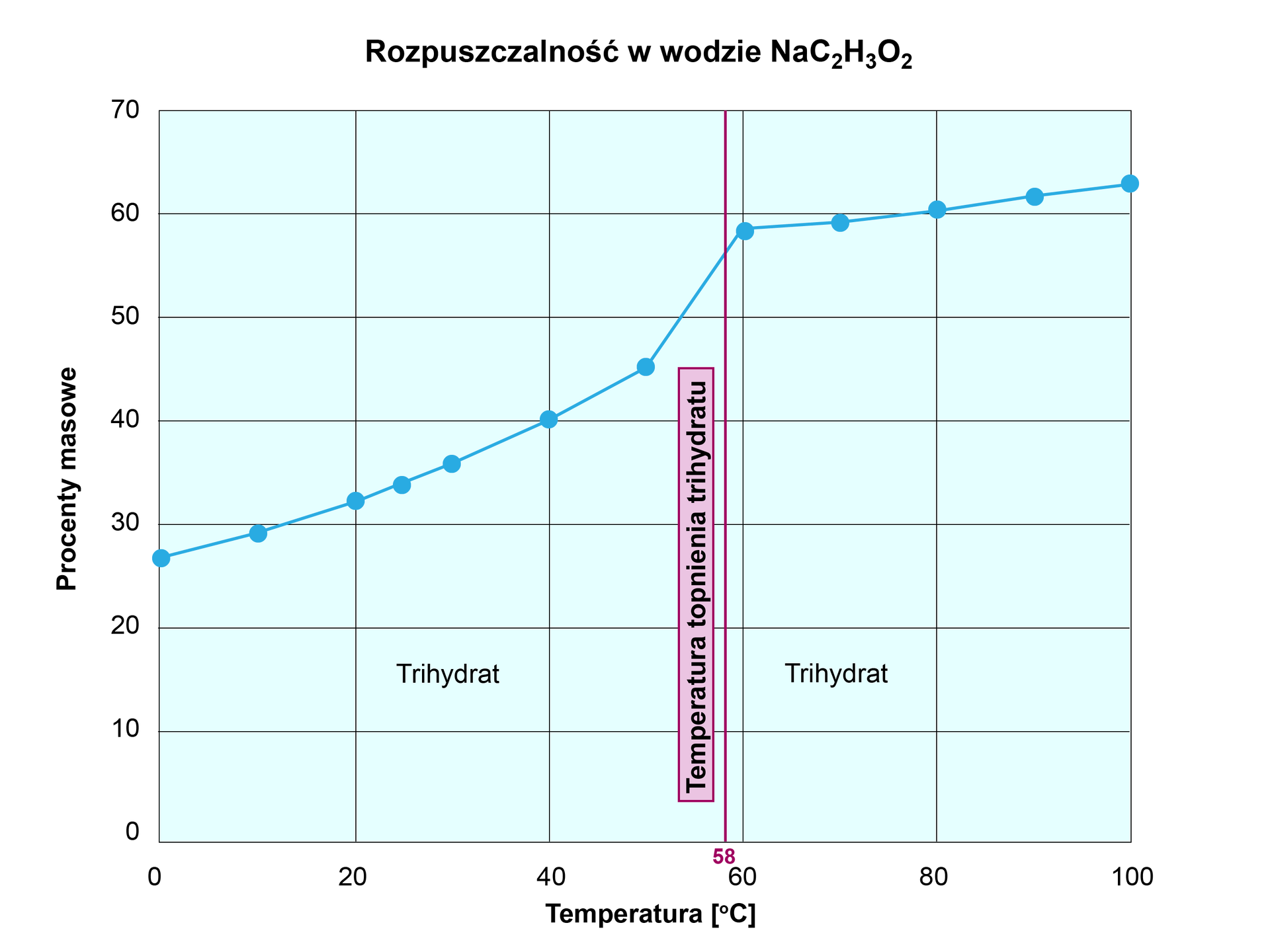
Jak otrzymać roztwór przesyconyroztwór przesycony etanianu sodu (octanu sodu) ?
Aby otrzymać roztwór przesycony, należy oziębić gorący, nasycony roztwór. Z wykresu rozpuszczalności uwodnionego etanianu sodu wynika, że w temperaturze roztwór nasycony etanianu sodu posiada w swoim składzie substancji rozpuszczonej () i wody. Po przygotowaniu roztworu nasyconego, należy szybko go schłodzić. Jeżeli obniżymy temperaturę do i cała rozpuszczona substancja pozostanie w roztworze, wówczas uzyskamy roztwór przesycony.
RozpuszczalnośćRozpuszczalność etanianu sodu (octanu sodu):
Należy najpierw usunąć wszelkie pozostałości stałej substancji rozpuszczanej, żeby nie było zarodków krystalizacji.
Roztwór przesycony jest niestabilny. W praktyce oznacza to, że drobne zaburzenie, np. wstrząs, dostanie się do roztworu zanieczyszczenia lub wrzucenie kryształka, spowoduje krystalizację nadmiaru substancji rozpuszczonej.
Rozpuszczalność w temperaturze wynosi , więc masa wykrystalizowanego osadu powinna wynieść:
Roztwór przesycony można także otrzymać przez odparowanie rozpuszczalnika z roztworu nasyconego.
Miód jest roztworem przesyconym ze względu na ilość zawartych w nim cukrów – głównie glukozy i fruktozy. W warunkach przechowywania, czyli w temperaturze pokojowej, krystalizacja glukozy może przebiegać kilka miesięcy, a nawet kilka lat.

Zjawisko wydzielania się ciepła w procesie krystalizacji roztworu przesyconego zostało wykorzystane w pewnym rodzaju kieszonkowych ogrzewaczy dłoni. Wykorzystuje się w nich etanian sodu lub tiosiarczan sodu.

Zapoznaj się z filmem samouczkiem, a następnie rozwiąż poniższe ćwiczenia.
Film dostępny pod adresem /preview/resource/R1JrJv0dkxMl7
Film nawiązujący do treści materiału dotyczącej zagadnienia otrzymywania roztworu przesyconego z roztworu nienasyconego.
Wymień dwie czynności, które zwiększają szansę na uzyskanie roztworu przesyconego.