Badanie właściwości estrów
Właściwości fizyczne i chemiczne estrów
Zapoznaj się z animacją dotyczącą badania właściwości fizycznych i chemicznych estrów, a następnie rozwiąż ćwiczenia zamieszczone poniżej.

Film dostępny pod adresem /preview/resource/RI3x3rKxgqvsU
Film nawiązujący do treści materiału - dotyczy sposobu badania właściwości fizycznych i chemicznych estrów.
Podaj nazwy związków chemicznych, które są substratami reakcji przedstawionej na animacji.
Podaj nazwy związków chemicznych, które są produktami reakcji przedstawionej na animacji.
Wytłumacz, jakie znaczenie ma obecność kwasu siarkowego(VI)?
Zapoznaj się z krótką animacją, a następnie uzupełnij poniższy formularz.
Film dostępny pod adresem /preview/resource/RIgeZmBdYHbb8
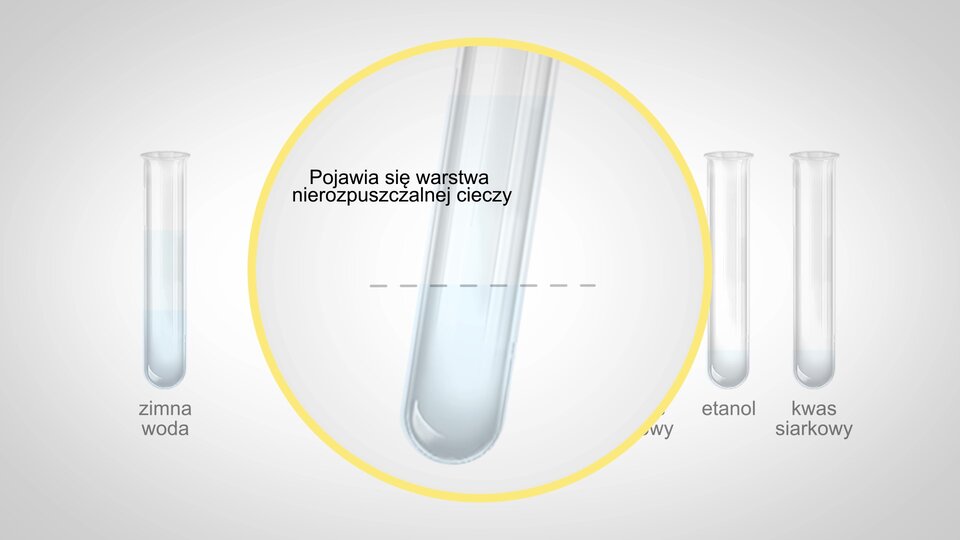
Film prezentujący doświadczenie. Do doświadczenia potrzeba pięciu probówek. Po lewej stronie jest probówka z zimną wodą oraz pusta probówka. Po prawej stronie są trzy probówki, w których kolejno znajdują się: kwas octowy, etanol i kwas siarkowy. Do pustej probówki wlewamy kwas octowy, etanol i kwas siarkowy. Zanurzamy probówkę w gorącej wodzie. Następnie zawartość probówki przelewamy do probówki z zimną wodą. Pojawia się warstwa nierozpuszczalnej cieczy.
Na podstawie przeprowadzonego doświadczenia, można określić trzy właściwości fizyczne octanu etylu jako przedstawiciela estrów:
występuje w postaci cieczy trudno rozpuszczalnej w wodzie;
substancja o gęstości mniejszej niż gęstość wody;
estry posiadają charakterystyczne zapachy, przypominające zapachy owoców lub kwiatów.
Zapoznaj się z animacją, a następnie uzupełnij poniższy formularz.

Film dostępny pod adresem /preview/resource/R1ONL8oiA3Shk
Film prezentuje doświadczenie. Są trzy probówki: w jednej jest pięcioprocentowy roztwór wodorotlenku sodu en a o ha, w drugiej pięcioprocentowy roztwór kwasu siarkowego sześć ha dwa es o cztery, w trzeciej woda destylowana ha dwa o. Do każdej probówki dodano ce 4 ha 8 o 2. Trzy probówki włożono do gorącej wody - ma 70 stopni. Zapach octowy wydzielił się w probówce drugiej. W pozostałych brak zapachu.
Hydroliza jest to reakcja chemiczna, której ulegają między innymi estry. Dla tej grupy związków chemicznych wyróżniamy następujące rodzaje hydrolizy:
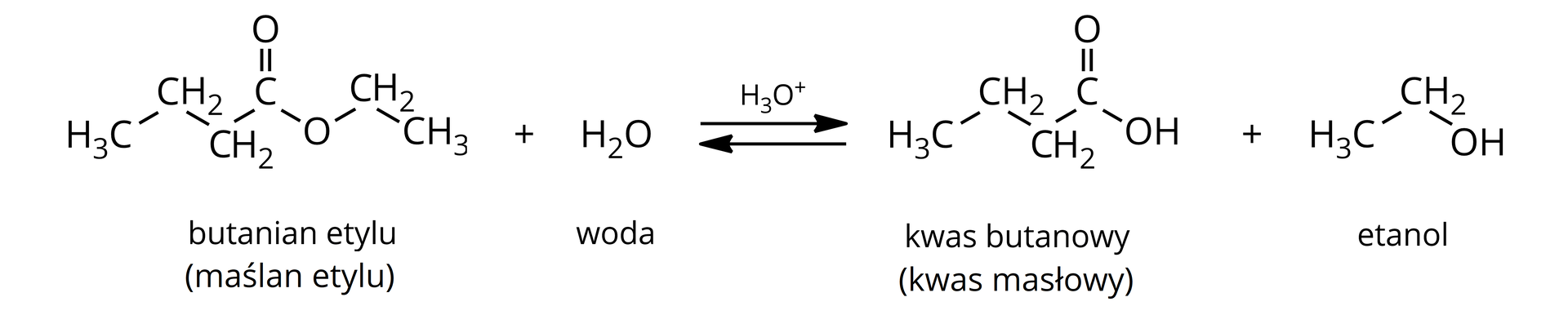
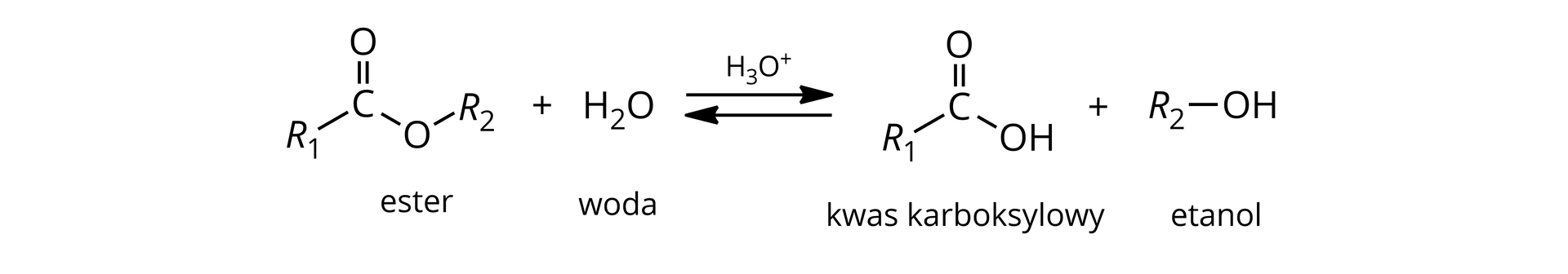
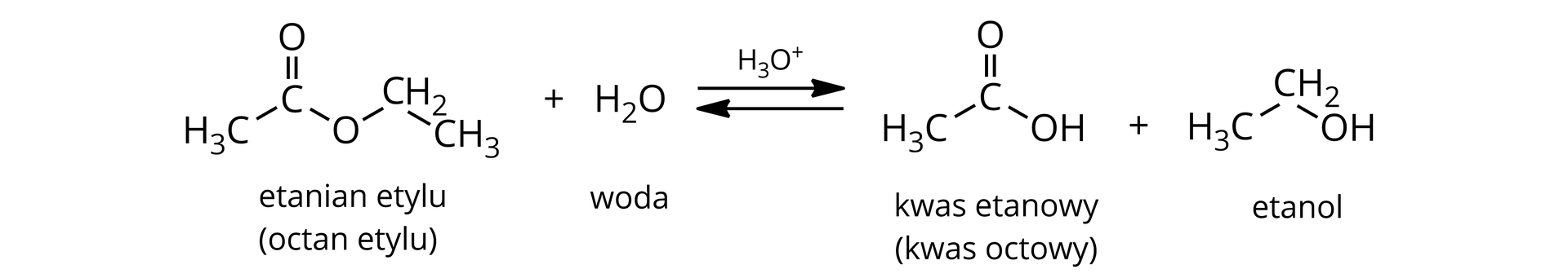
Hydroliza kwasowa – rozpad estru na kwas i alkohol. Hydroliza ta zachodzi pod wypływem wodnego roztworu kwasu. Jest odwróceniem reakcji estryfikacji, czyli jest reakcją odwracalną.
Zapis ogólny hydrolizy kwasowej estrów:
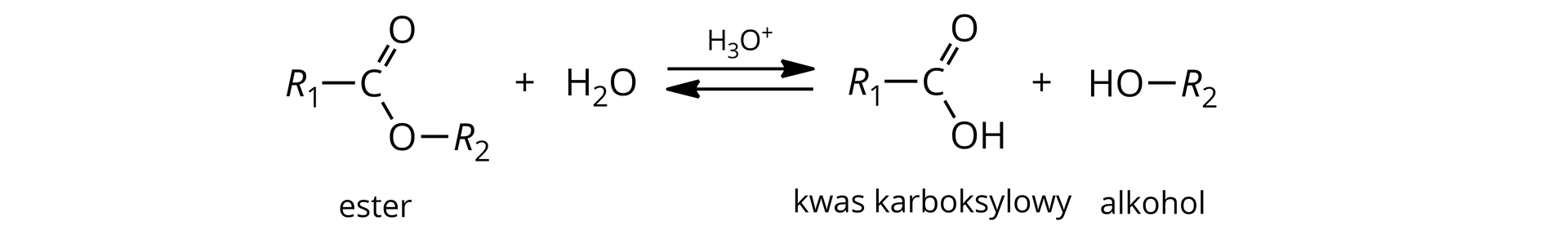
Czy wiesz, jak przebiega hydroliza kwasowa estrów? Czy potrafisz opisać jej mechanizm i warunki, w jakich przebiega? Zapoznaj się z poniższą animacją i wykonaj zadania.
Film dostępny pod adresem /preview/resource/R1P9G9qUDLbp5
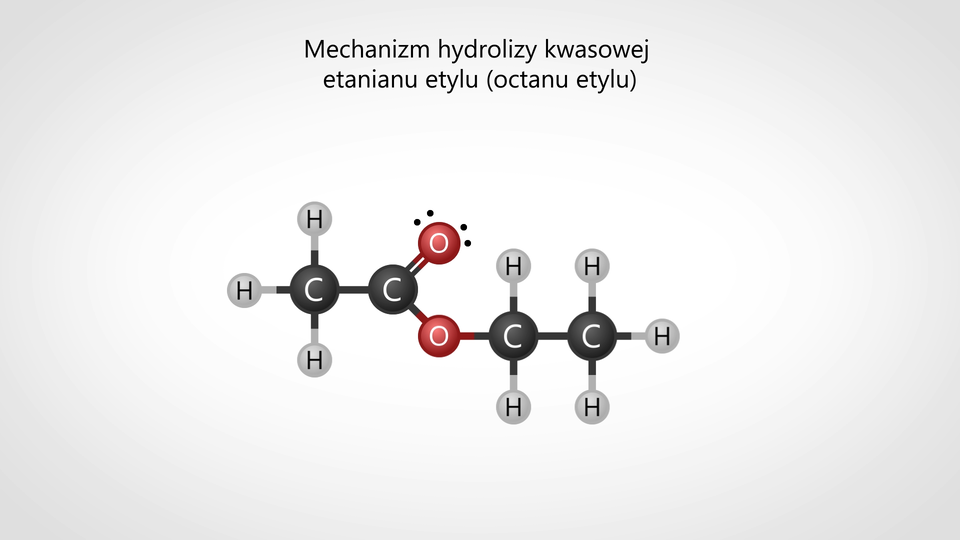
Tematem animacji jest mechanizm hydrolizy kwasowej estru.
Spośród dostępnych poniżej elementów, wybierz odpowiednie i napisz równanie reakcji hydrolizy kwasowej danego estru. Podpisz reagenty.
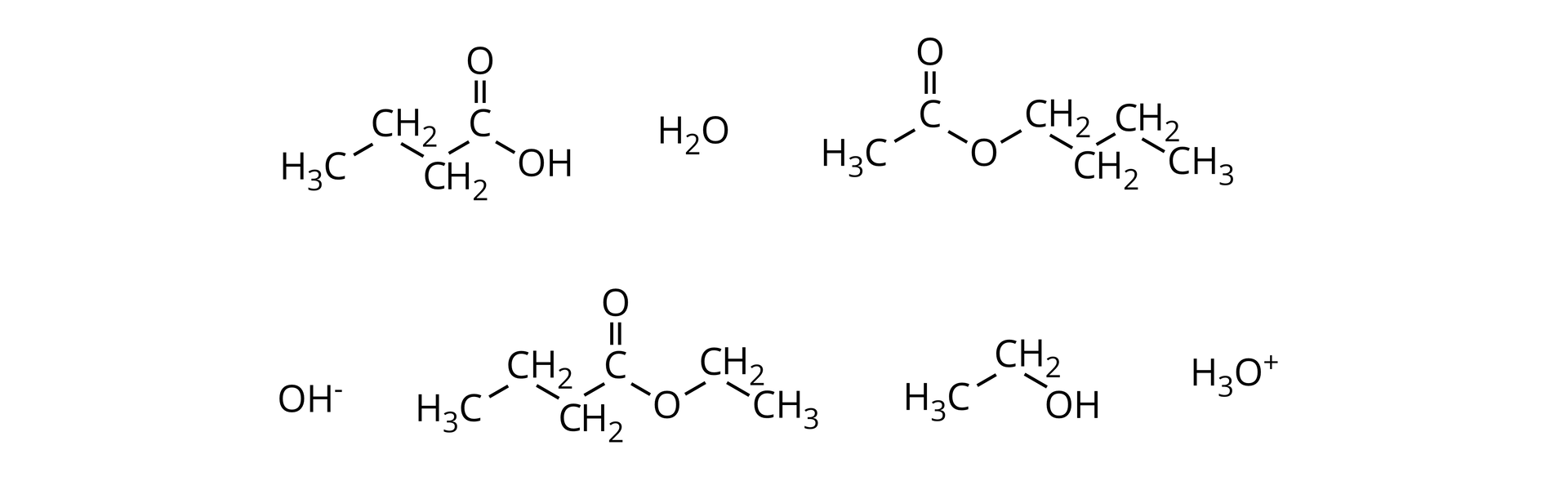
Na podstawie przedstawionej poniżej reakcji hydrolizy kwasowej etanianu etylu (octanu etylu), napisz ogólną reakcję hydrolizy kwasowej estrów. Pamiętaj o podpisaniu reagentów.
Na podstawie opisanej reakcji hydrolizy kwasowej etanianu etylu (octanu etylu), napisz ogólną reakcję hydrolizy kwasowej estrów. Użyj nazw reagentów.
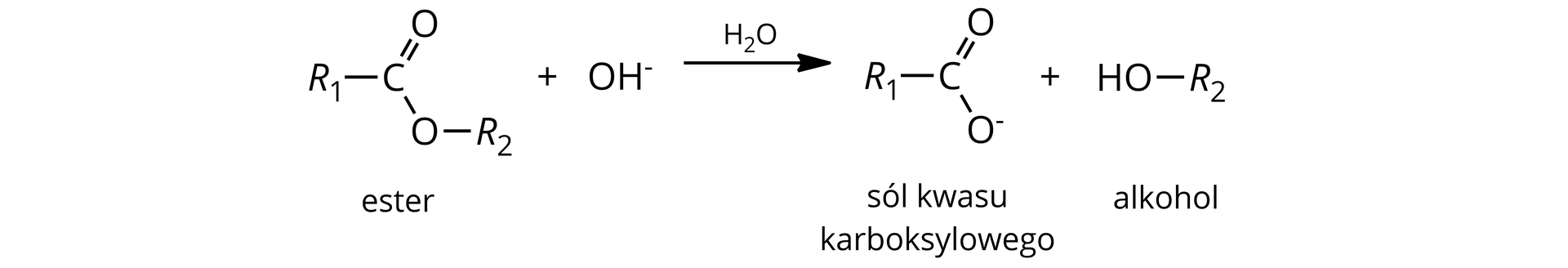
Hydroliza zasadowa – rozpad estru na sól kwasu karboksylowego i alkohol. Zachodzi ona w środowisku zasadowym. Jest to reakcja praktycznie nieodwracalna.
Zapis ogólny równania hydrolizy zasadowej estrów:
Czy wiesz, w jaki sposób przebiega hydroliza estrów w środowisku zasadowym? Czy potrafisz opisać mechanizm tej reakcji i podać powstające produkty? Zapoznaj się z poniższą animacją i wykonaj zadania.
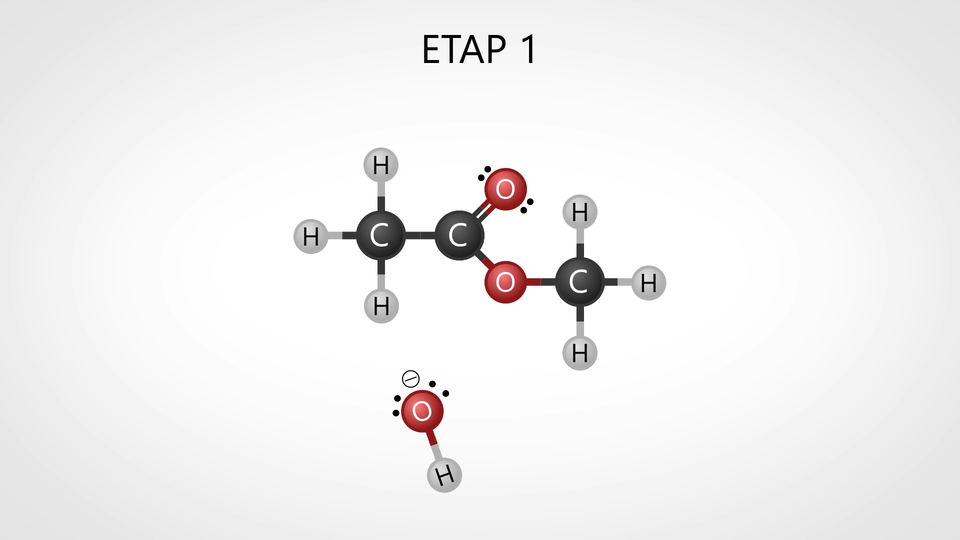
Film dostępny pod adresem /preview/resource/R1ZTMuzjG1o8h
Animacja nawiązująca do treści materiału dotyczącej, w jaki sposób przebiega hydroliza estrów w środowisku zasadowym.
Na podstawie równania reakcji, podaj nazwy wszystkich substratów i produktów.
Spośród dostępnych poniżej elementów, wybierz odpowiednie i napisz równanie reakcji hydrolizy zasadowej odpowiedniego estru. Podpisz reagenty podając ich nazwy.

Mając do dyspozycji związki: alkohol benzylowy, woda, benzoesan metylu, wodorotlenek sodu, propionian benzylu, jon oksoniowy i propionian sodu zapisz słownie równanie reakcji hydrolizy zasadowej odpowiedniego estru. Nie wszystkie wymienione odczynniki są niezbędne w reakcji.
Na podstawie przedstawionej poniżej reakcji hydrolizy zasadowej etanianu metylu (octanu metylu), napisz w sposób ogólny równanie reakcji hydrolizy zasadowej estrów. Pamiętaj o podpisaniu reagentów.

Na podstawie opisu reakcji hydrolizy zasadowej etanianu metylu (octanu metylu), napisz w sposób ogólny równanie reakcji hydrolizy zasadowej estrów. Pamiętaj o podpisaniu reagentów.
Równanie reakcji: cząsteczka octanu metylu dodać cząsteczka wodorotlenku sodu. Strzałka w prawo, nad strzałką zapis: woda. Za strzałką cząsteczka octanu sodu dodać cząsteczka metanolu .
Wyjaśnij, jak powstają jony wodorotlenkowe w roztworach wodnych? Zapisz odpowiednie równanie reakcji chemicznej uzasadniające odpowiedź.