Budowa białek. Strukutry białek
Budowa białek
Białka to substancje o dużej masie cząsteczkowej, składające się wyłącznie lub w większości z reszt aminokwasówaminokwasów. Przyjmuje się, że białka są biopolimerami o masach cząsteczkowych, większych od 10 tysięcy daltonówdaltonów, tj. zbudowane są z co najmniej 90 reszt aminokwasowych. Związki stworzone z mniejszej liczby reszt aminokwasowych nazywane są peptydami. Podział ten ma charakter umowny, a różnice między małymi białkami a dużymi peptydami nie są tak istotne. Reszty aminokwasowe w białkach są ze sobą połączone za pomocą wiązań peptydowych. Poniżej przedstawiono fragment białka z zaznaczonym na niebiesko ugrupowaniem peptydowym.

Podział białek
Ze względu na skład cząsteczki, białka można podzielić na:
białka proste – zbudowane tylko z reszt aminokwasowych, np. insulina, albumina, lizozym;
białka złożone – zbudowane z reszt aminokwasowych oraz części niebiałkowej, tzw. grupy prostetycznej (może nią być np. jon metalu, pierścień porfirynowy ze skoordynowanym jonem żelaza(II) lub magnezu, reszty cukrowe połączone wiązaniem kowalencyjnym z wybranymi aminokwasami, np. z treoniną).

Białka możemy podzielić ze względu na kształt cząsteczki. Właściwości wyodrębnionych w ten sposób typów białek zestawiono w poniższej tabeli.
Typ białka | Charakterystyka | Wybrane funkcje biologiczne | Przykłady |
|---|---|---|---|
Białka globularne | ▪ zwykle rozpuszczalne w wodzie i rozcieńczonych roztworach soli nieorganicznych | ▪ enzymatyczne | hemoglobina, immunoglobuliny, insulina |
Białka fibrylarne | ▪ zwykle nierozpuszczalne w wodzie i rozcieńczonych roztworach soli nieorganicznych | ▪ strukturalne | kolagen, fibrynogen, keratyna |
W celu zrozumienia kształtu lub konformacji białek, wprowadzono pojęcie rzędowości białka. Za pomocą tego terminu struktura białka jest opisywana na czterech poziomach:
Zapoznaj się z filmem poniżej, aby dokładnie zrozumieć, czym polega struktura białek. Następnie wykonaj ćwiczenia sprawdzające.
Zapoznaj się z poniższą animacją i zaznacz prawidłową odpowiedź dotyczącą hemoglobiny.

Film dostępny pod adresem /preview/resource/R17dg6qubUq8K
Film nawiązujący do treści materiału dotyczącej rzędowości struktur białkowych na przykładzie hemoglobiny, czyli białka o strukturze czwartorzędowej.
Wyjaśnij, czym są mostki disiarczkowe.
Wyjaśnij, czym są i w jaki sposób tworzą się alfa helisa i beta harmonijka.
Stabilizacja struktur białkowych
Każda z tych rzędowości jest stabilizowana przez różnego rodzaju oddziaływania. Teraz omówimy każdą z nich po kolei wraz z oddziaływaniami odpowiedzialnymi za stabilizację tej struktury.
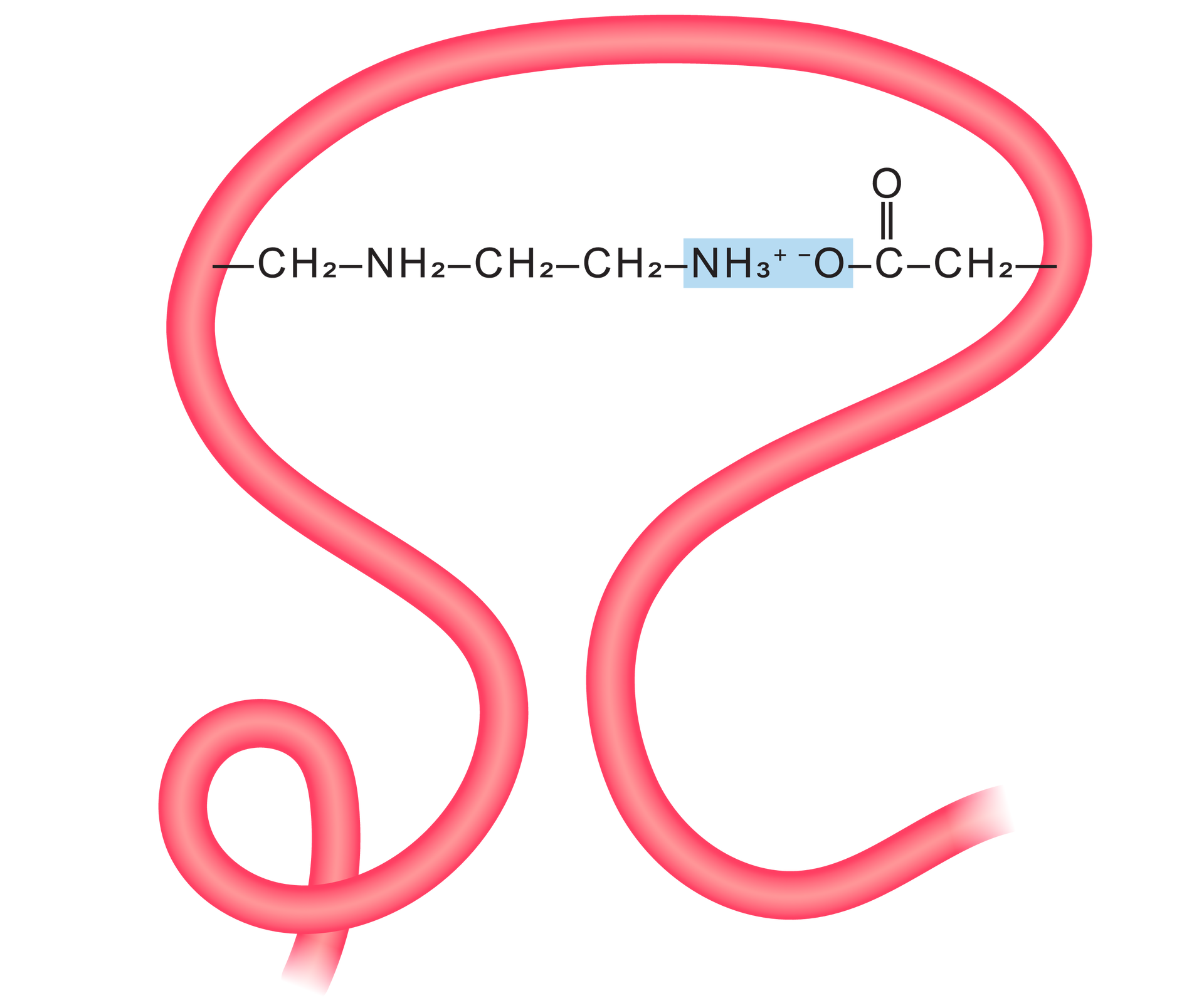
Wiązania jonowe
W białkach występują najczęściej pomiędzy dodatnio naładowanymi grupami aminowymi a ujemnie naładowanymi grupami karboksylowymi.
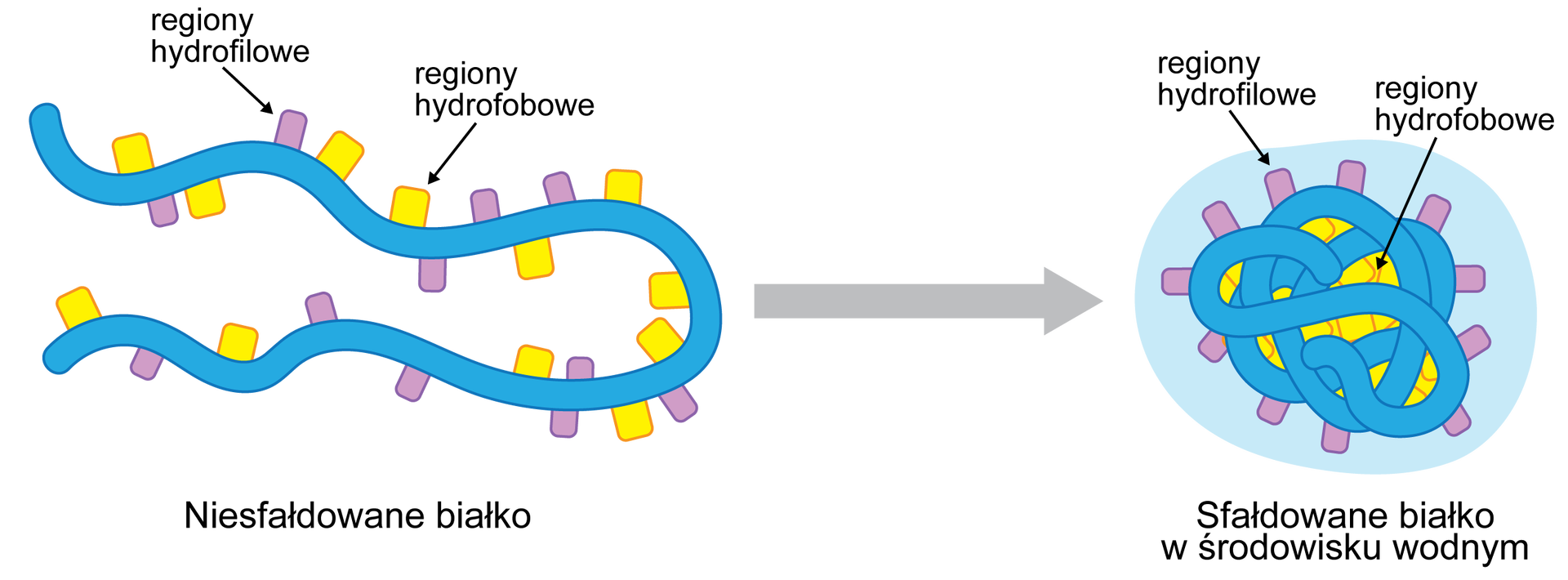
Oddziaływania hydrofobowe
Oddziaływania te występują w cząsteczkach, które posiadają w swojej budowie regiony hydrofobowe i hydrofilowe. Regiony hydrofilowe to takie części cząsteczki, o których można powiedzieć, że „lubią” wodę, co naukowo znaczy – mają budowę polarną. Woda jest cząsteczką polarną, co oznacza, że w swojej cząsteczce ma ładunki elektryczne, rozłożone nierównomiernie. W myśl zasady: podobne rozpuszcza się w podobnym – w wodzie rozpuszczają się cząsteczki polarne. tomiast regiony hydrofobowe to takie części cząsteczki, które przeciwnie do regionów hydrofilowych „boją się wody”, czyli mają budowę niepolarną. Dzięki tej różnicy, występującej w związkach, może dochodzić do oddziaływań hydrofobowych. Polegają one na ograniczeniu dostępu do wody tym częściom cząsteczki, które są hydrofobowe. Jeżeli w jednej, dużej cząsteczce występują odpowiednio regiony hydrofobowe i hydrofilowe, to taka cząsteczka ulega zwijaniu i zmianom w położeniu do takiego stopnia, aby zmniejszyć kontakt z wodą odcinkom hydrofobowym. Używając obrazowego języka możemy stwierdzić, że cząsteczka na zewnątrz, czyli w kierunku cząsteczek wody, kieruje swoje hydrofilowe fragmenty, a fragmenty hydrofobowe chowa niejako do swojego wnętrza. Oddziaływania hydrofobowe zostały zaprezentowane na poniższym obrazku:
Siły van der Waalsa
Są to bardzo słabe oddziaływania pomiędzy atomami występującymi blisko siebie. Większość części białka jest upakowanych, dzięki czemu siły van der Waalsa mogą między nimi zachodzić. Mają bardzo duże znaczenie w przyrodzie, ponieważ to dzięki nim zachodzi wiele procesów fizykochemicznych. Odpowiedzialne za budowę białek czy adsorpcję, są powszechnie występującymi oddziaływaniami. Odgrywają ważną rolę w oddziaływaniach białko‑białko, gdzie dochodzi do dopasowania, jak klucza do zamku. Przykładem takiej sytuacji jest rozpoznawanie antygenu przez przeciwciało.
Wyróżnia się kilka rodzajów sił van der Waalsa:
oddziaływanie dipol - dipol - dwie cząsteczki mające moment dipolowy przyciągają się,
oddziaływanie dipol - dipol indukowany - jedna cząsteczka z momentem dipolowym indukuje moment dipolowy u drugiej cząsteczki i dochodzi do ich przyciągania,
oddziaływanie dipol indukowany - dipol indukowany - obie cząsteczki nie posiadające momentu dipolowego uzyskują chwilowe momenty dipolowe i przyciągają się.
Wiązanie wodorowe
Jest rodzajem oddziaływania elektrostatycznego pomiędzy atomem wodoru a atomem elektroujemnym, który zawiera wolne pary elektronowe. W białkach wiązanie wodorowe powstaje pomiędzy grupą karbonylową jednego aminokwasu a grupą iminową drugiego aminokwasu. Rolą wiązania wodorowego w białkach jest stabilizacja struktury alfa‑helisy i beta‑kartki.

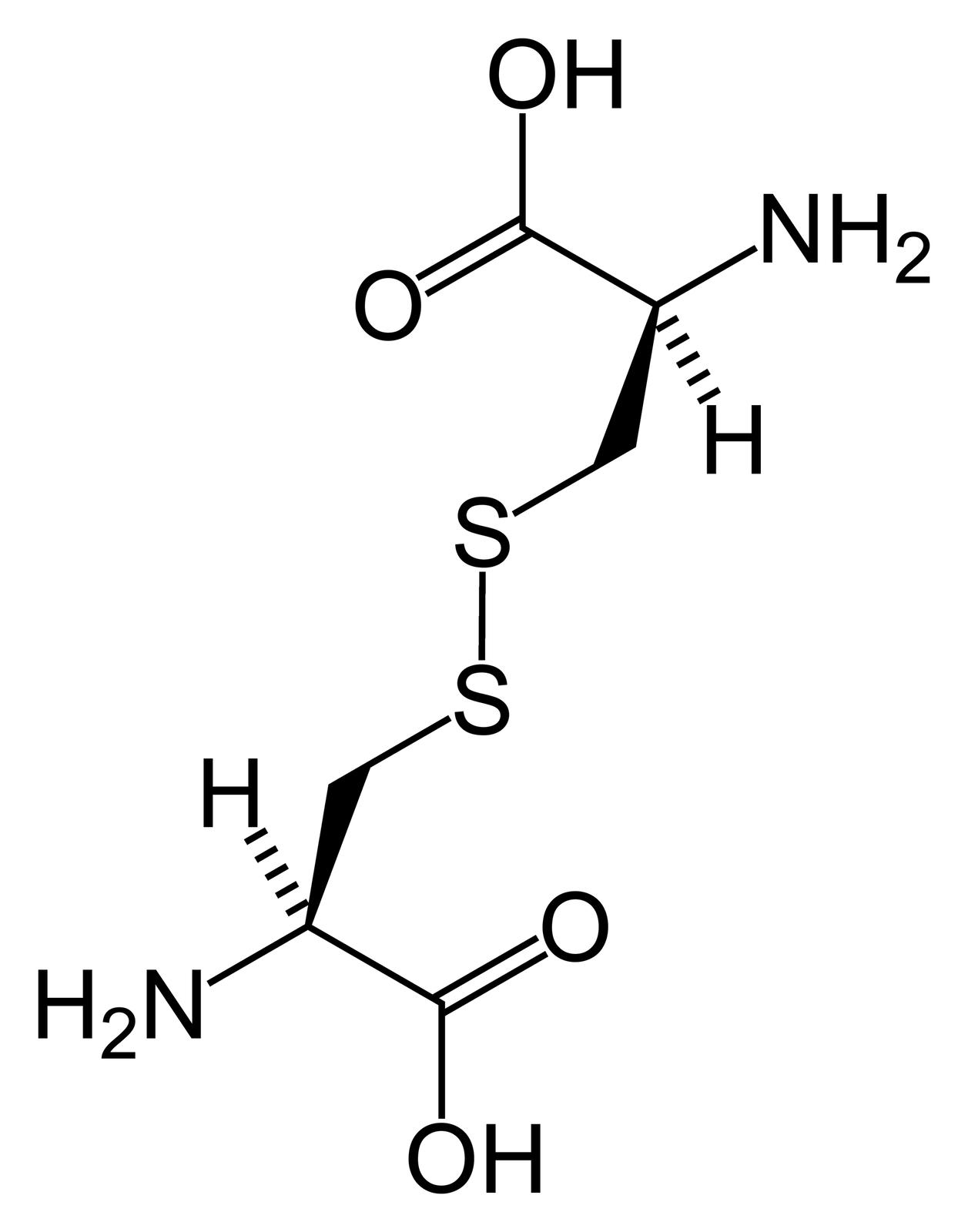
Mostki disiarczkowe
Te struktury powstają, gdy dwie grupy tiolowe () połączą się ze sobą. Grupy te mogą występować w dwóch różnych związkach albo w jednym. Odgrywają ważną rolę w fałdowaniu i stabilności wielu białek. Utrzymuje części białka razem stabilizując jego zwiniętą formę. Mostki disiarczkowe mogą również tworzyć centra hydrofobowe – regiony hydrofobowe białka układają się wokół mostków disiarczkowych, tym samym ograniczając swój kontakt z wodą. Mostek disiarczkowy zaprezentowano na galerii poniżej.

Wykonaj polecenie 2 i zastanów się, które wiązania stablizują poszczególne struktury białek.
Metalotioneiny to niskocząsteczkowe białka bogate w reszty cysteinowe, zdolne do wiązania metali ciężkich. Reszty cysteinowe metalotioneiny odgrywają główną rolę w procesach fizjologicznych, tj. homeostaza pierwiastków niezbędnych do funkcjonowania komórek, unieszkodliwianie metali ciężkich oraz usuwanie wolnych rodników tlenowych. Poniżej zostały ukazane struktury metalotioneiny występującej u bakterii z rodzaju Cyanobacteria. Na ich podstawie odpowiedz na poniższe pytania.
Metalotioneiny to niskocząsteczkowe białka bogate w reszty cysteinowe, zdolne do wiązania metali ciężkich. Reszty cysteinowe metalotioneiny odgrywają główną rolę w procesach fizjologicznych, tj. homeostaza pierwiastków niezbędnych do funkcjonowania komórek, unieszkodliwianie metali ciężkich oraz usuwanie wolnych rodników tlenowych. Zapoznaj się z opisem struktury metalotioneiny występującej u bakterii z rodzaju Cyanobacteria. Na ich podstawie odpowiedz na poniższe pytania.