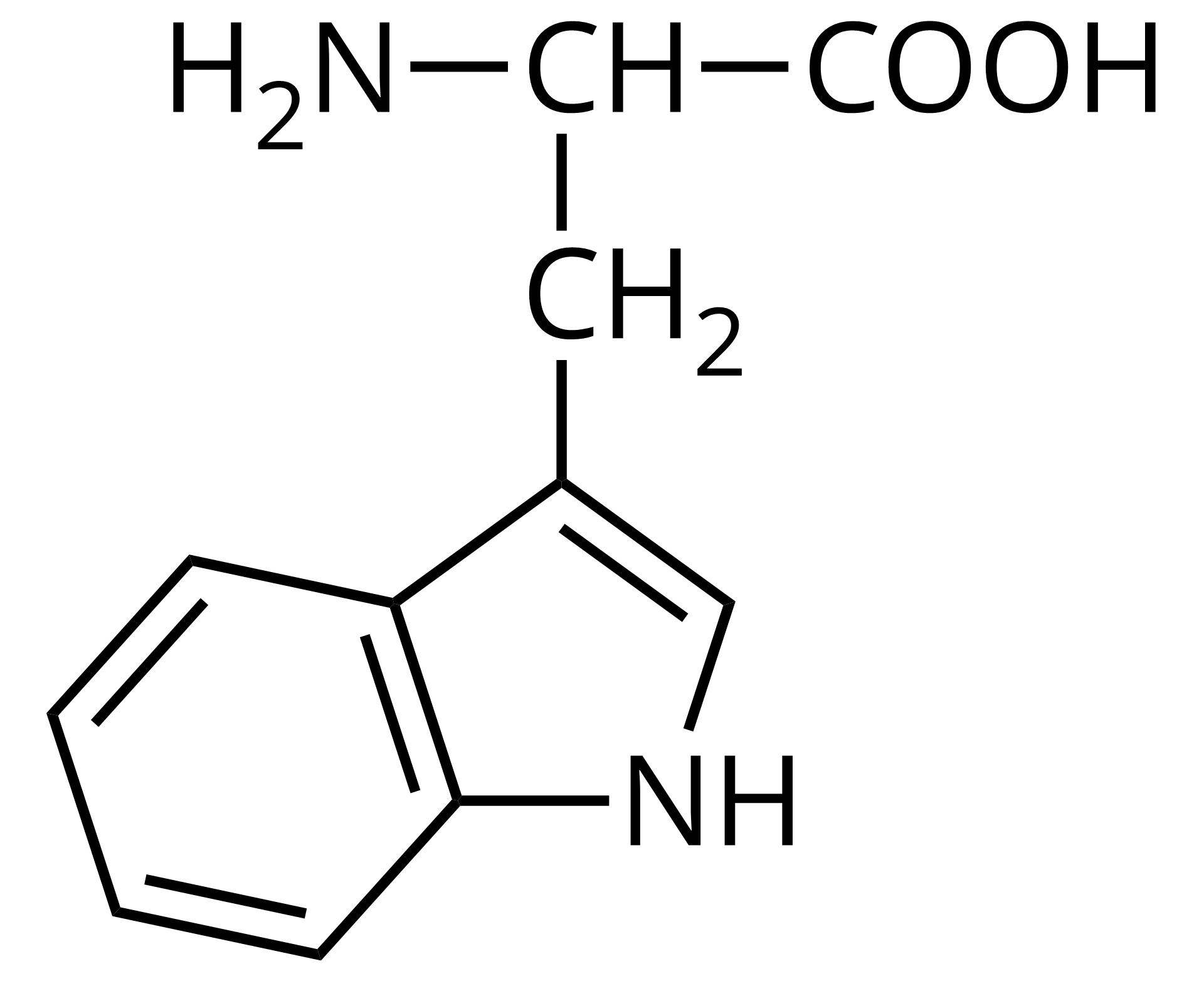
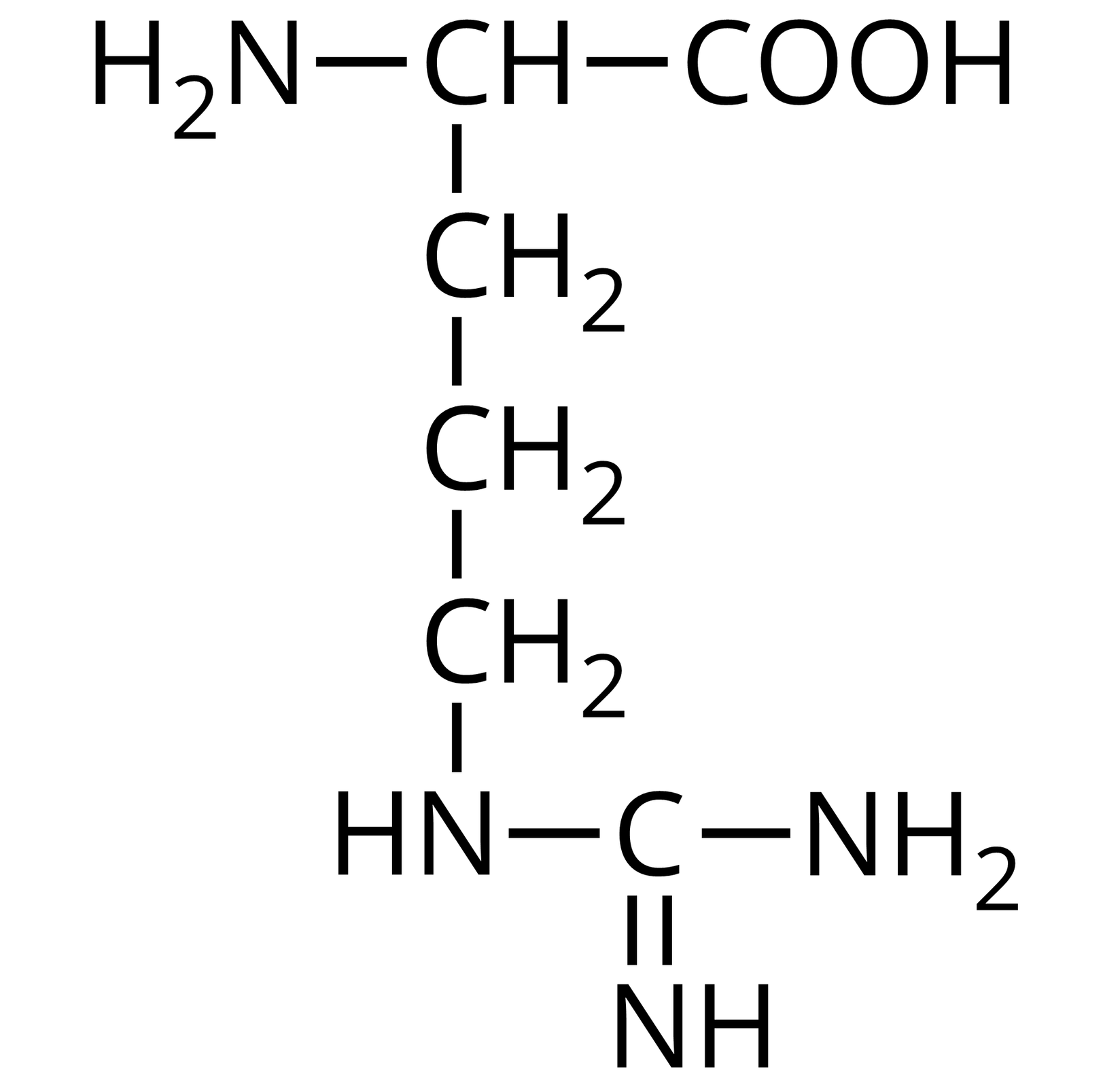
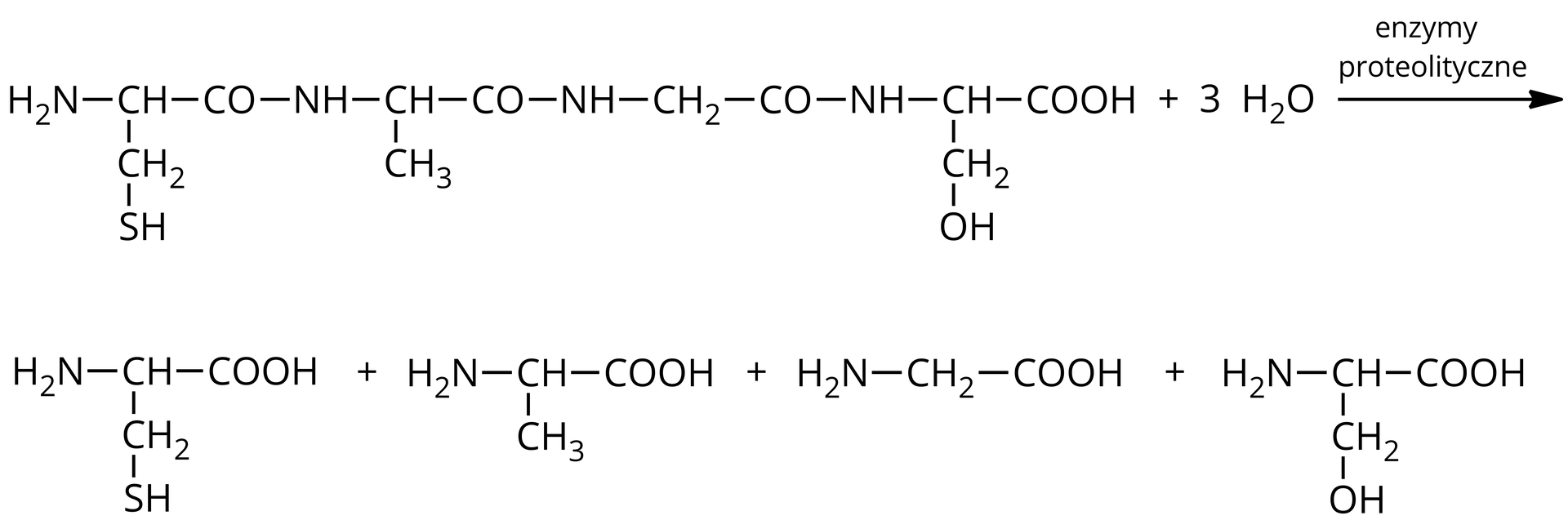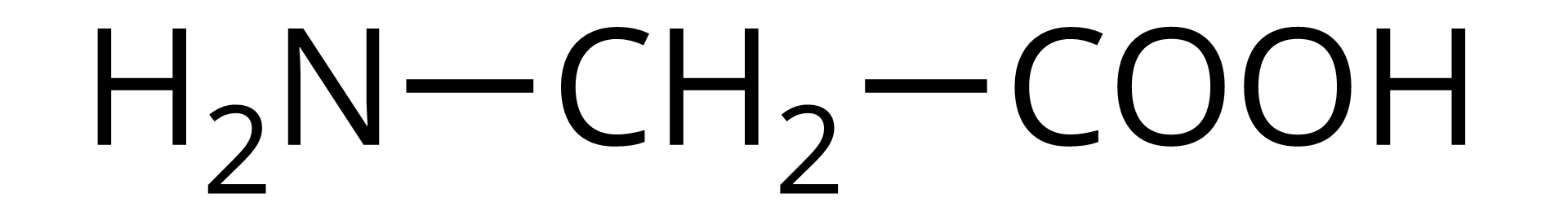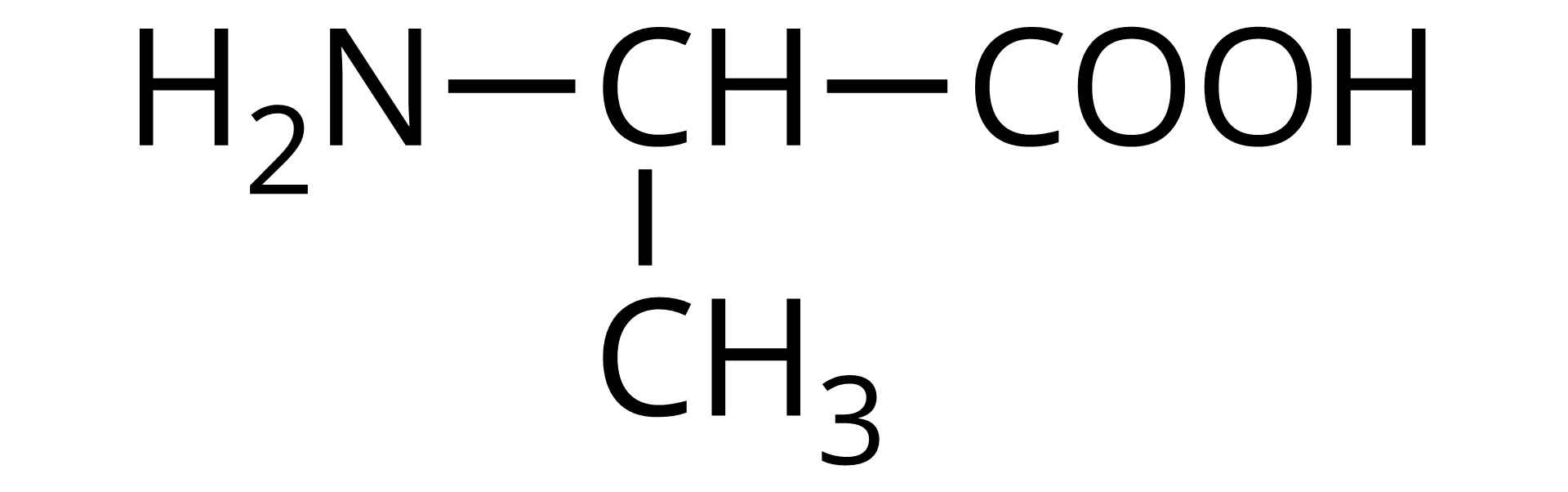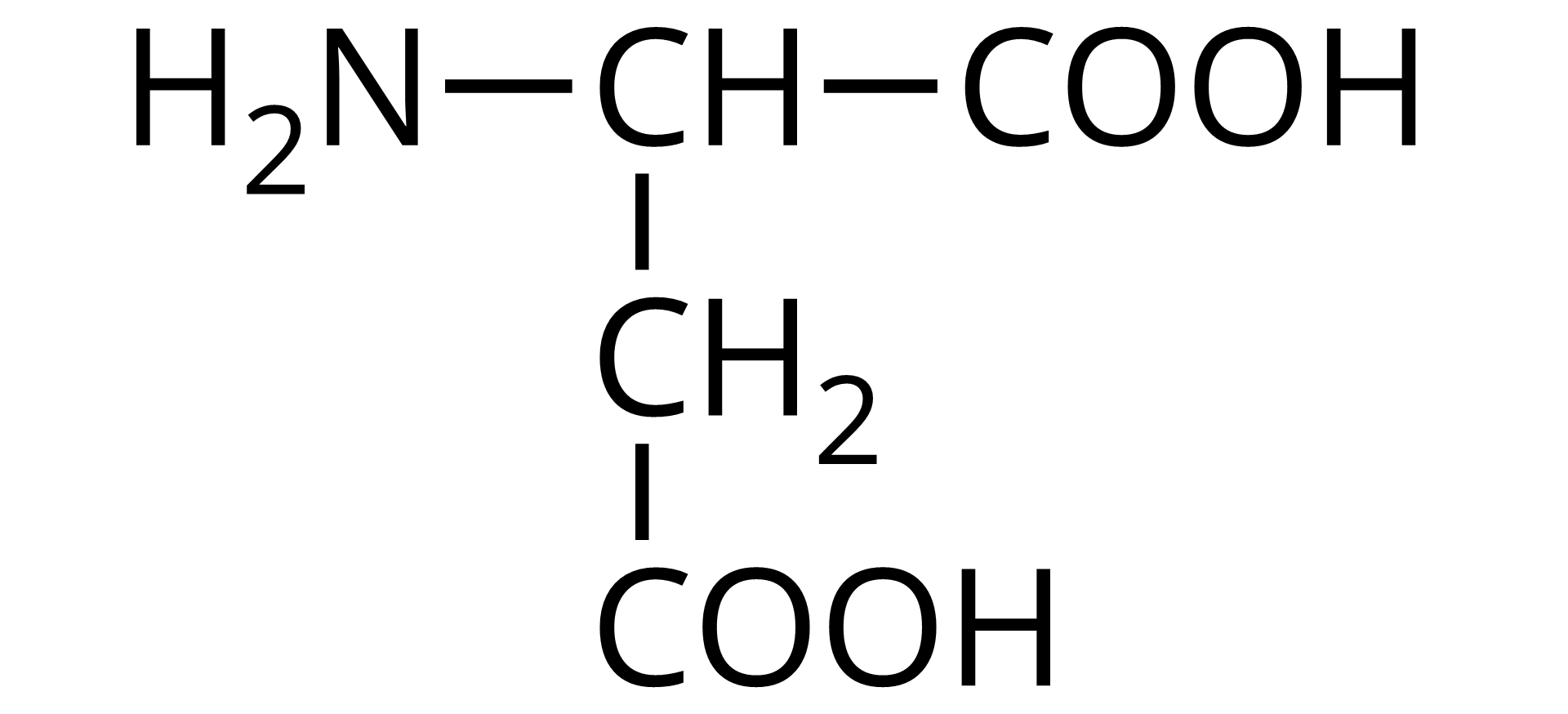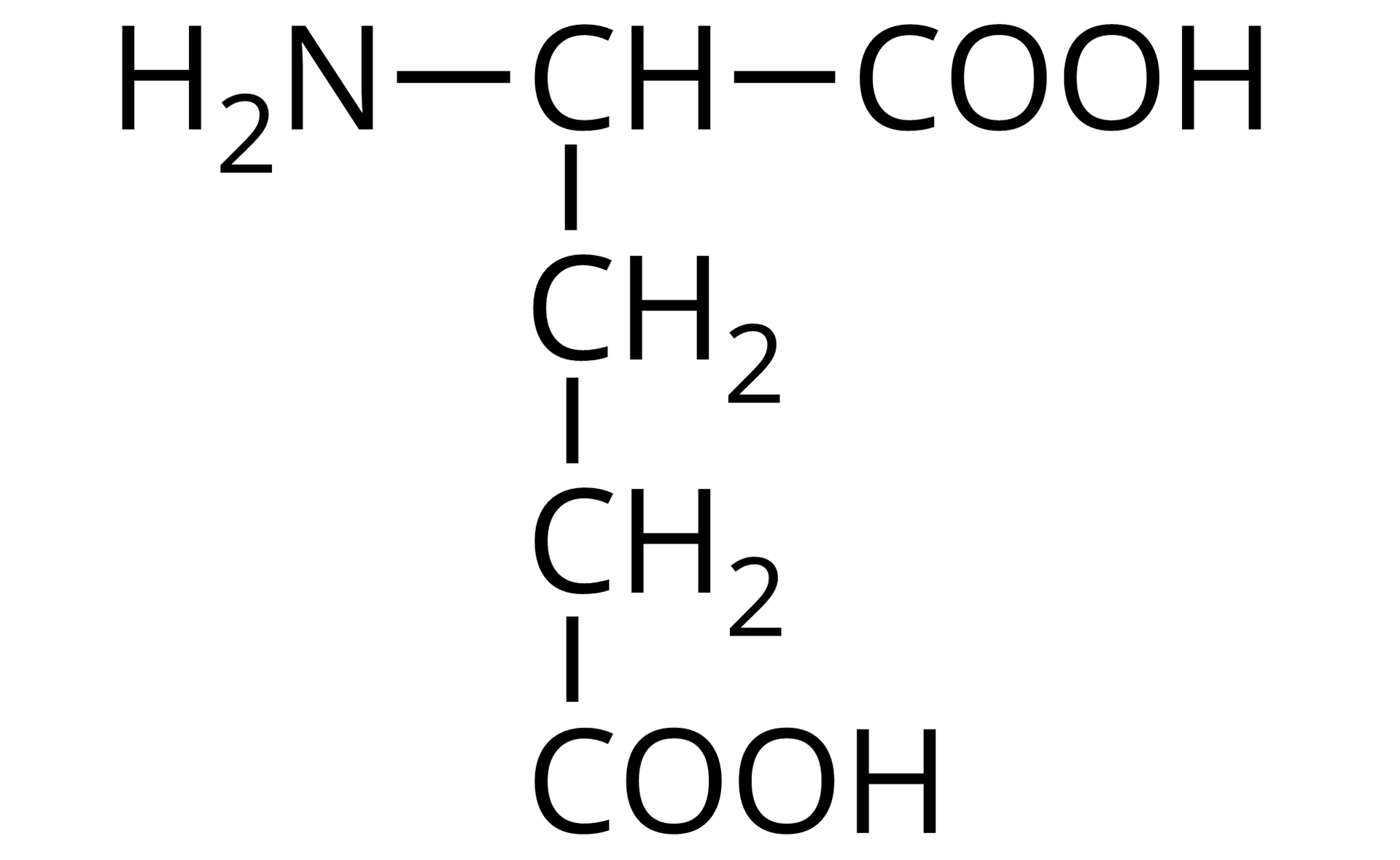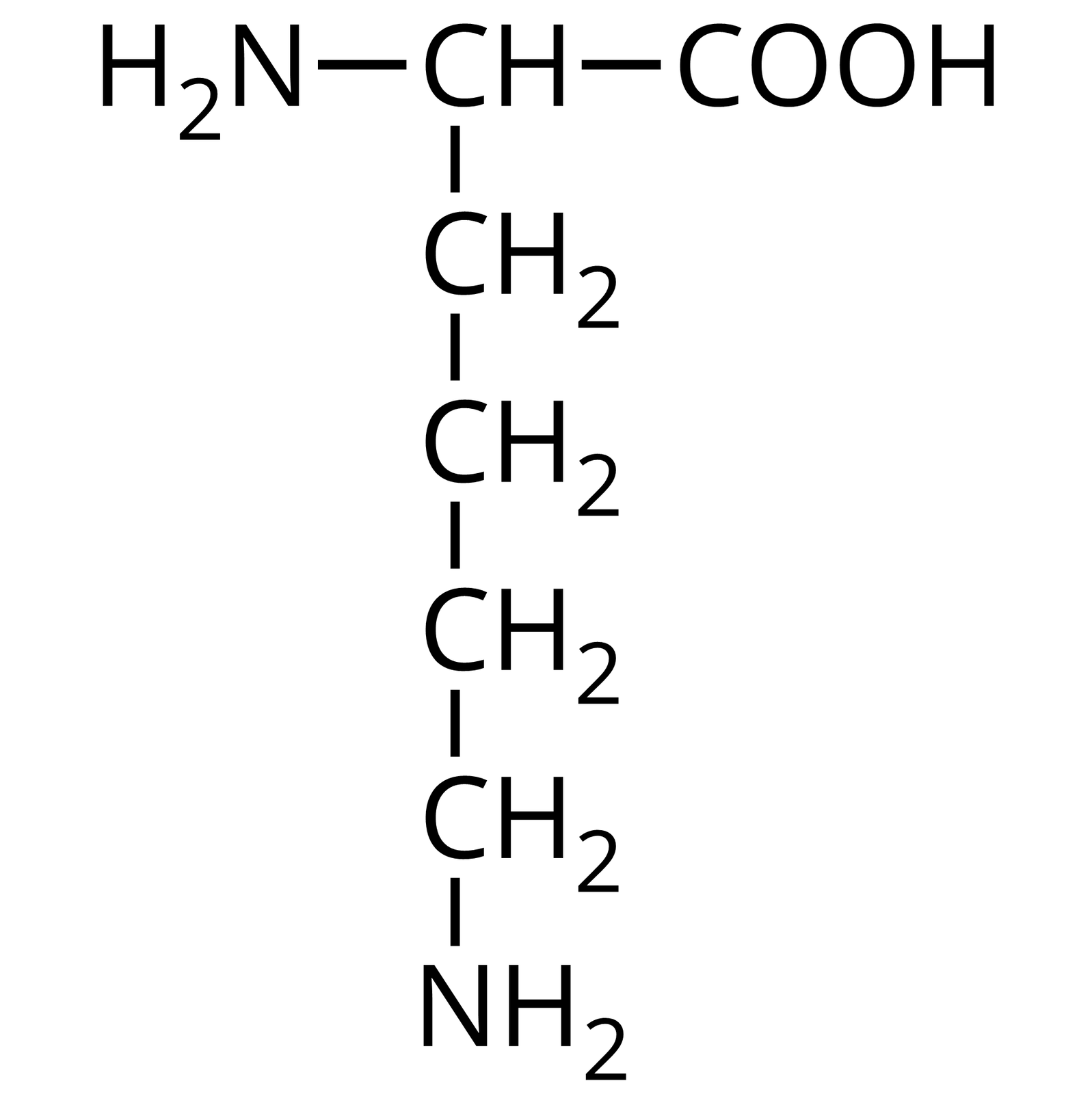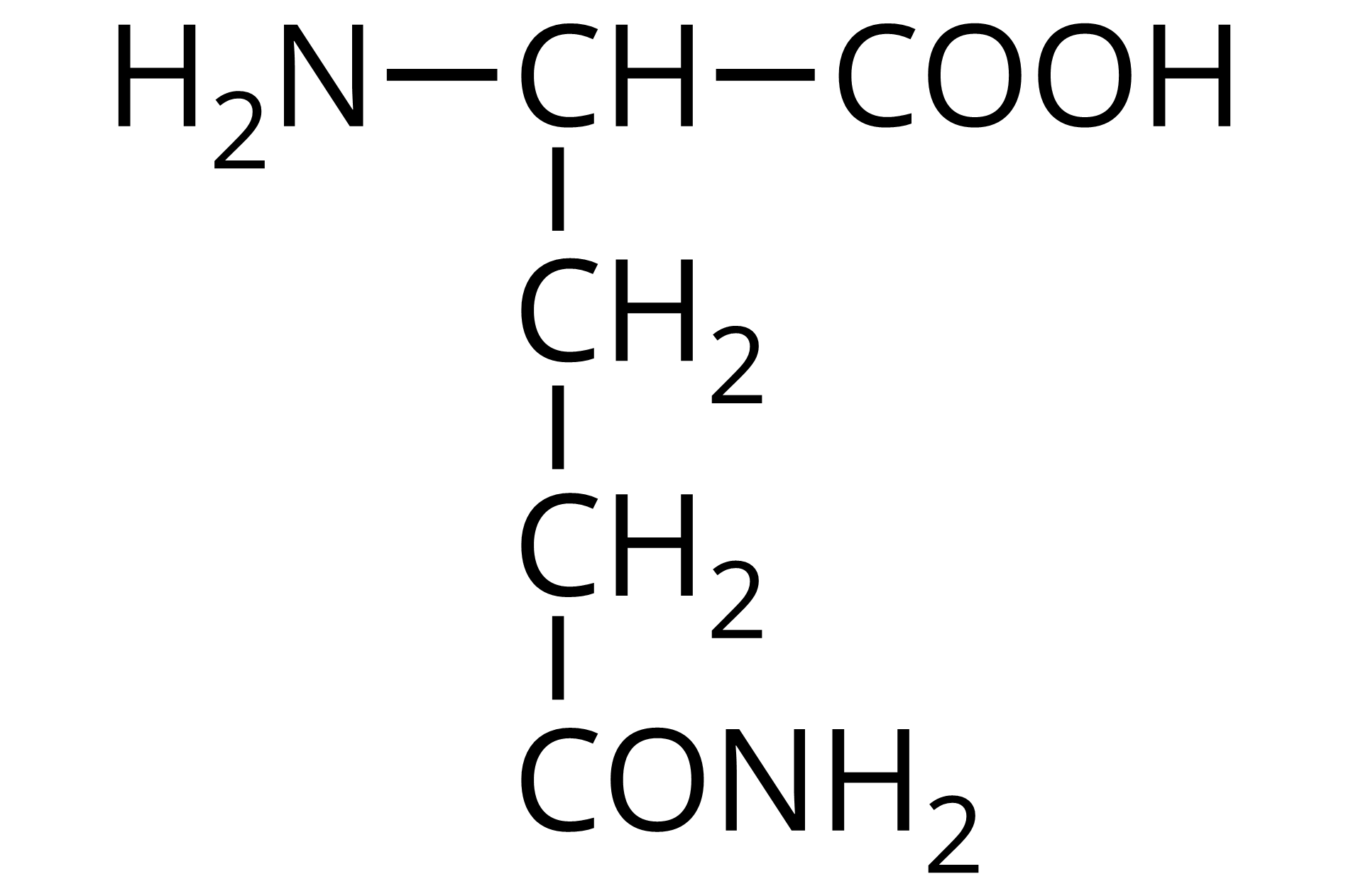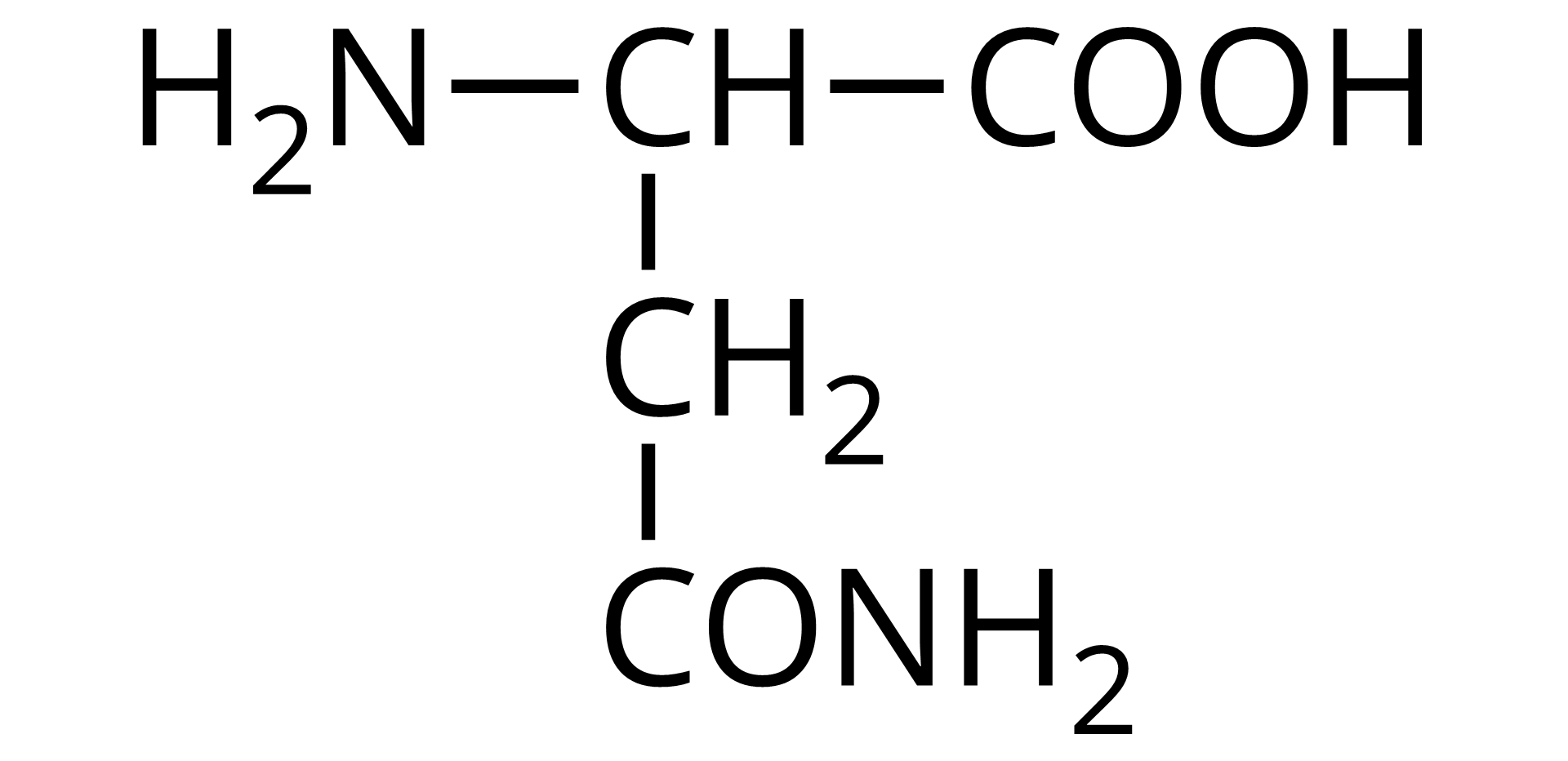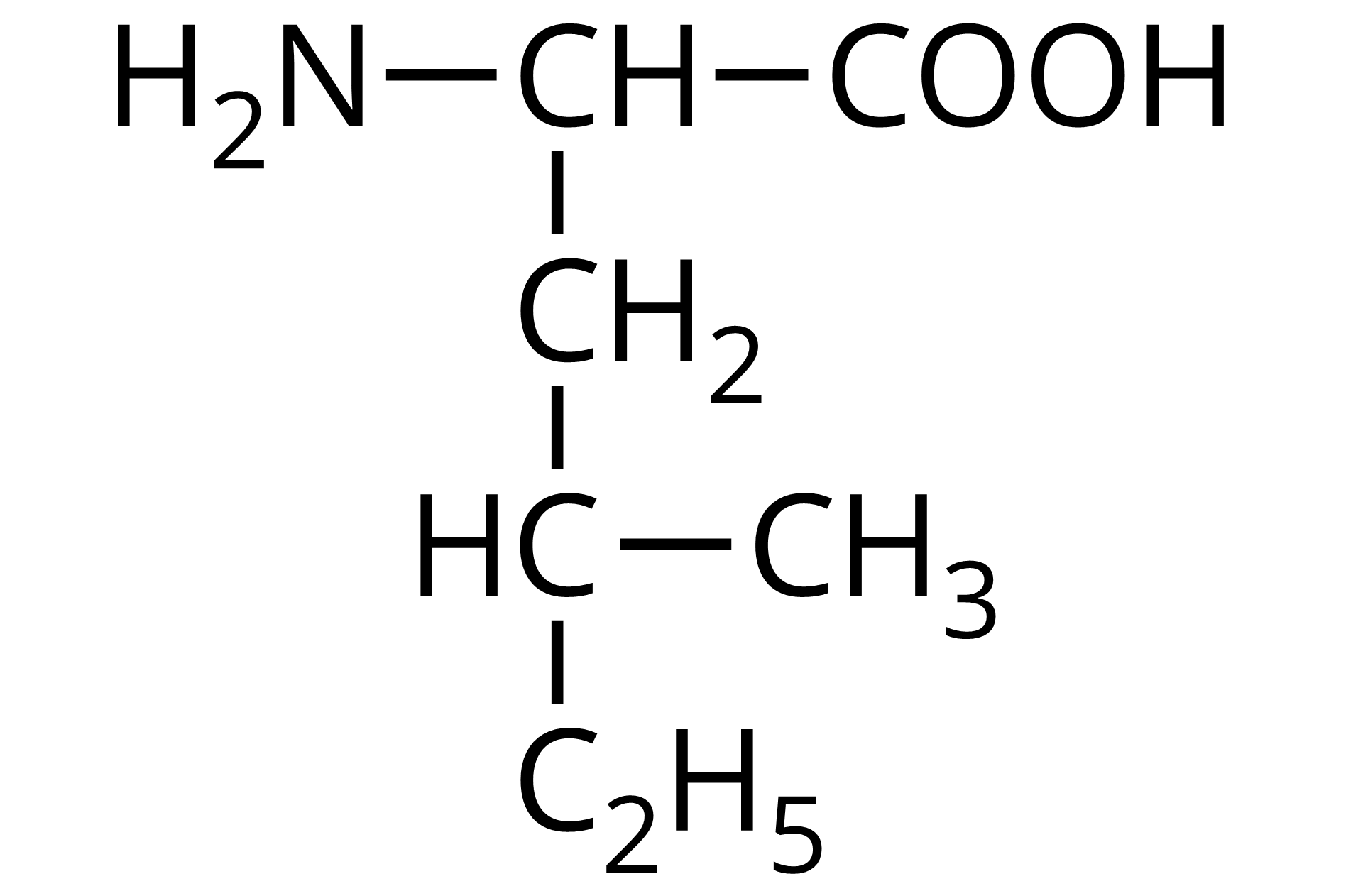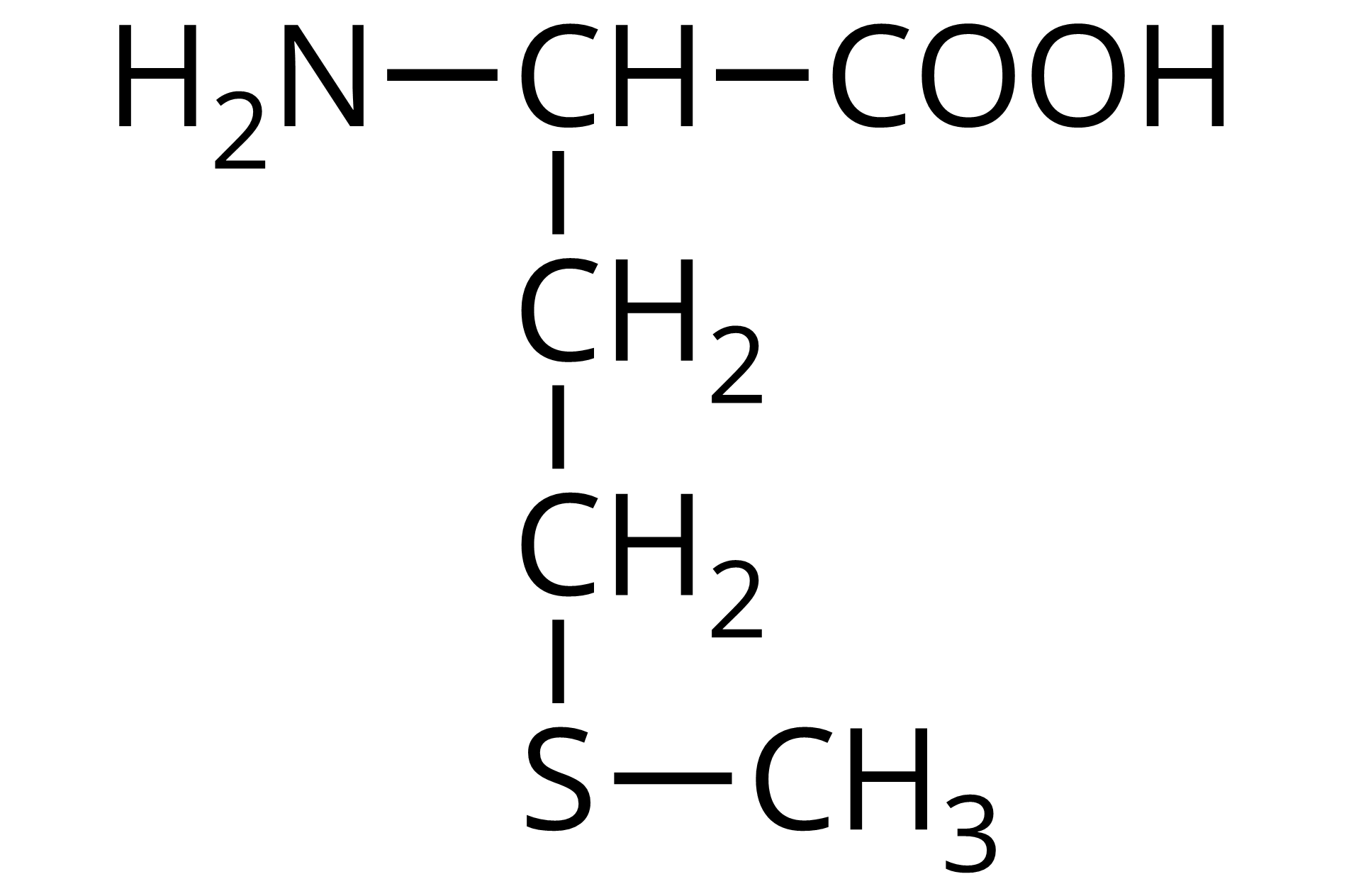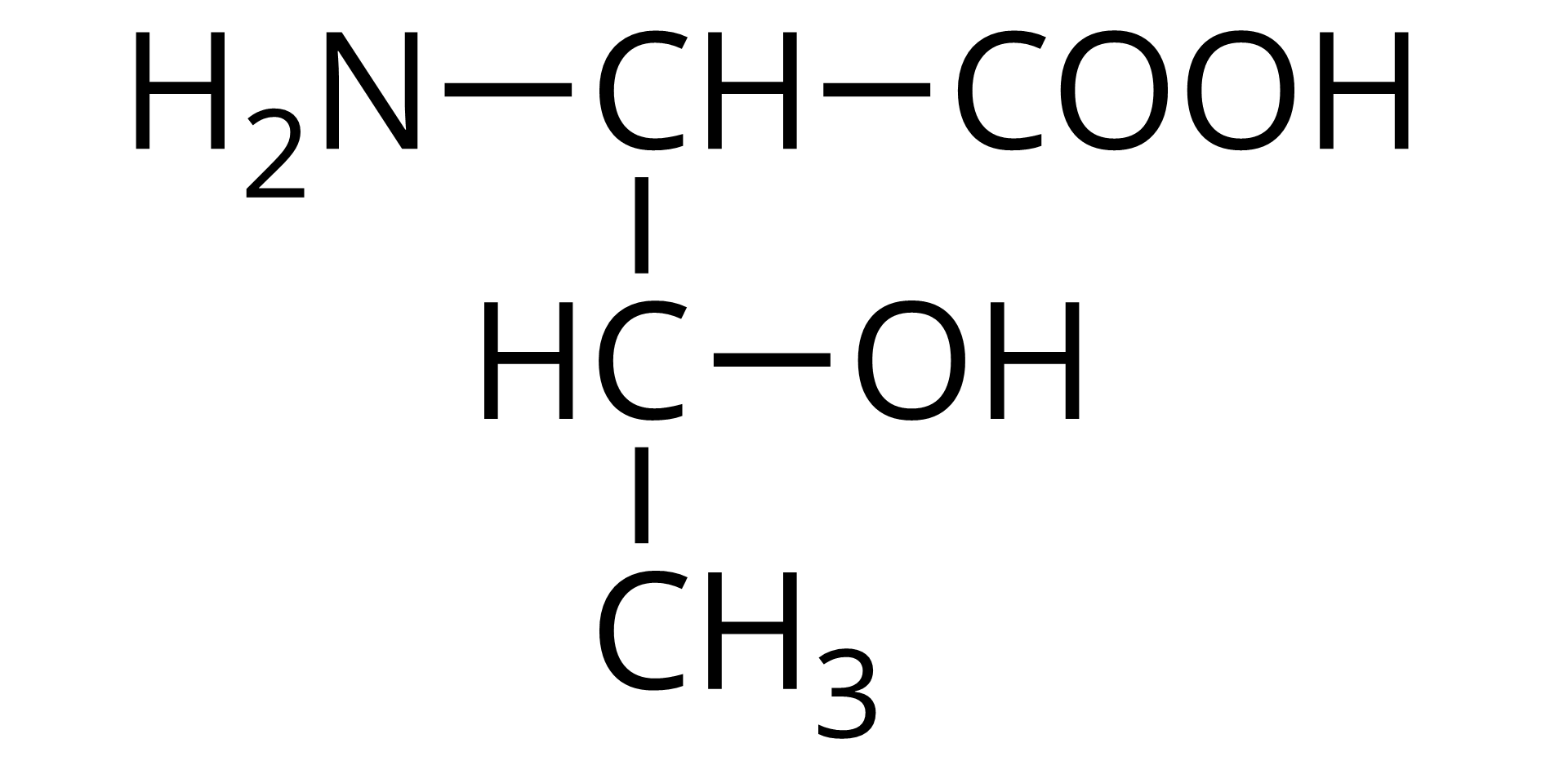Otrzymywanie peptydów i ich hydroliza
Peptydy
Peptydy zbudowane są z reszt aminokwasów, połączonych wiązaniem peptydowym. Ze względów praktycznych peptydy o cząsteczkach zawierających mniej niż 10 reszt aminokwasowych są określane jako oligopeptydy, a zawierające do ok. 100 reszt — jako polipeptydy. Związki, których cząsteczki są zbudowane z ponad 100 reszt są określane jako białka.
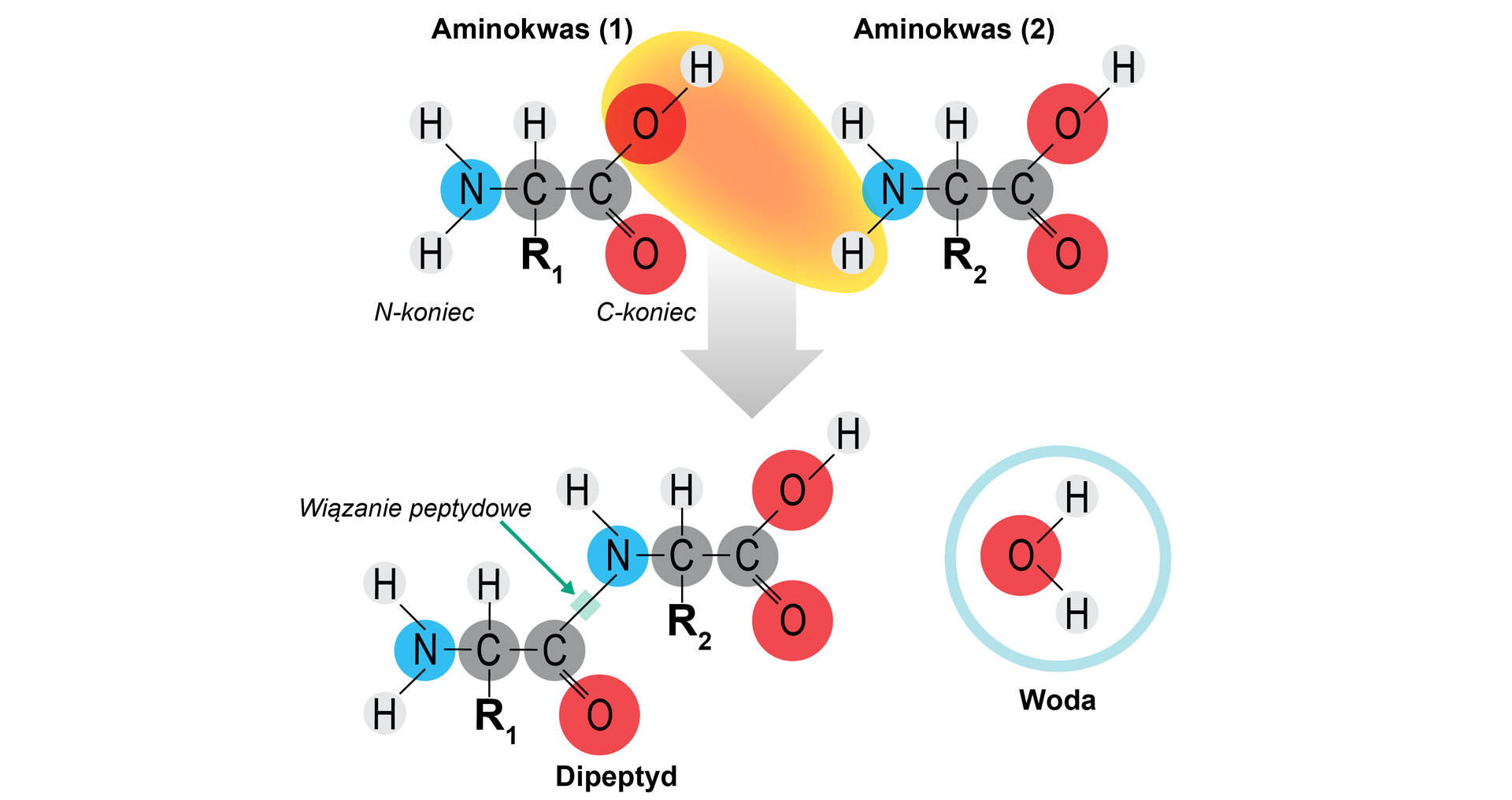
Peptydy powstają na drodze kondensacji aminokwasów. Aminokwasy, ze względu na obecność w cząsteczkach grupy karboksylowej i grupy aminowej, mogą się ze sobą łączyć w reakcji kondensacji aminokwasów. W reakcji kondensacji dwóch różnych aminokwasów można uzyskać cztery różne dipeptydy, które zawierają wolną grupę aminową oraz wolną grupę karboksylową.
W czasie reakcji kondensacji glicyny i alaniny można uzyskać cztery peptydy:

By lepiej zrozumieć kondensację aminokwasów zapoznaj się z samouczkiem i wykonaj zawarte poniżej ćwiczenia.
Czy wiesz, w jaki sposób cząsteczki aminokwasów mogą łączyć się ze sobą? Zapoznaj się z poniższym filmem, a następnie rozwiąż zadania.
Film dostępny pod adresem /preview/resource/R1P1JN2T0RK7J
Film dotyczy reakcji kondensacji aminokwasów. Przedstawiono reakcje kondensacji glicyny i fenyloalaniny tworzących dłuższe łańcuchy polipeptydowe.
Zaznacz poprawną odpowiedź.
Jak nazywa się związek, którego wzór przedstawiono poniżej?
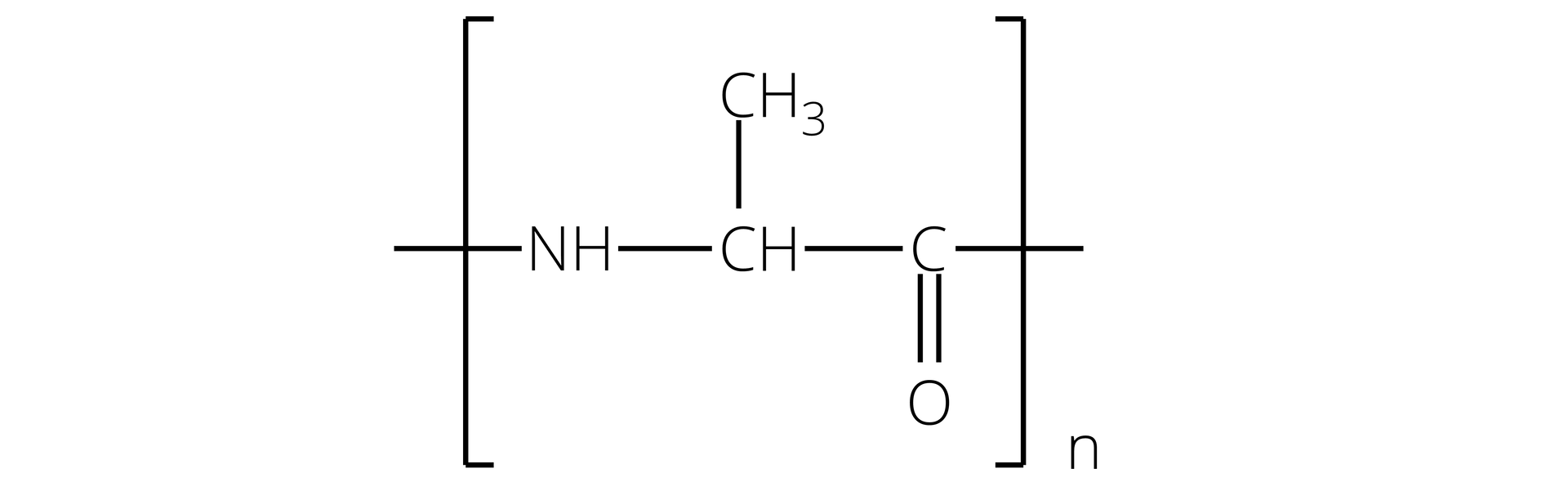
Zaznaczony w poprzednich równaniach układ atomów, nosi nazwę wiązania peptydowegowiązania peptydowego. Układ atomów tworzących wiązanie peptydowe jest płaski, sztywny i prawie zawsze występuje w formie trans.
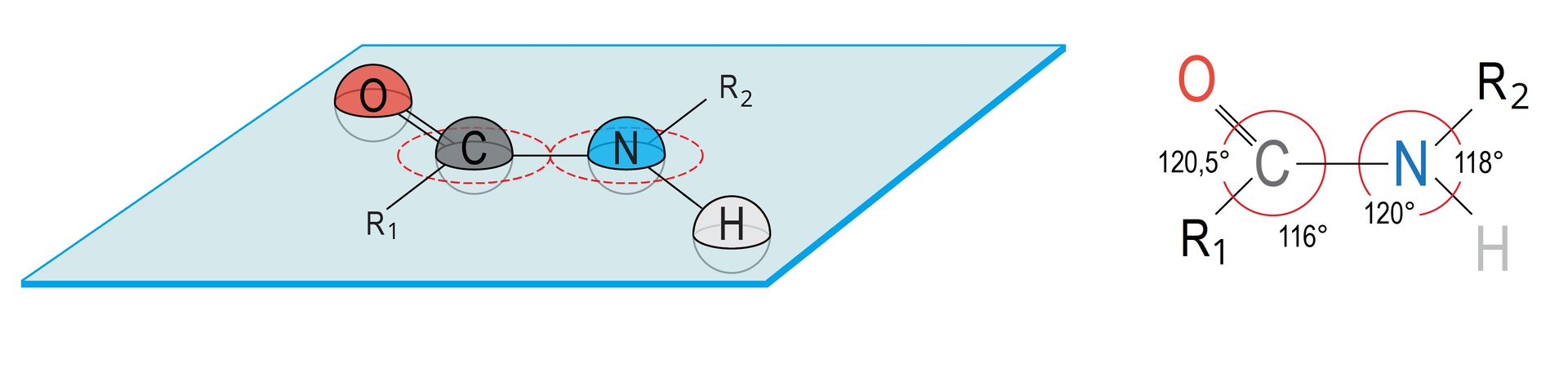
Zgodnie z ogólnie przyjętą umową wzory strukturalne peptydów przedstawia się, umieszczając wzór aminokwasu z wolną grupą aminową po lewej stronie (grupa N–terminalna lub N–końcowa), a aminokwasu z wolną grupą karboksylową na końcu szeregu po prawej stronie (grupa C–terminalna lub C–końcowa).
Reakcje cyklizacji
– i –aminokwasy ulegają podczas ogrzewania cyklizacji, tworząc laktamy, czyli cykliczne amidy:
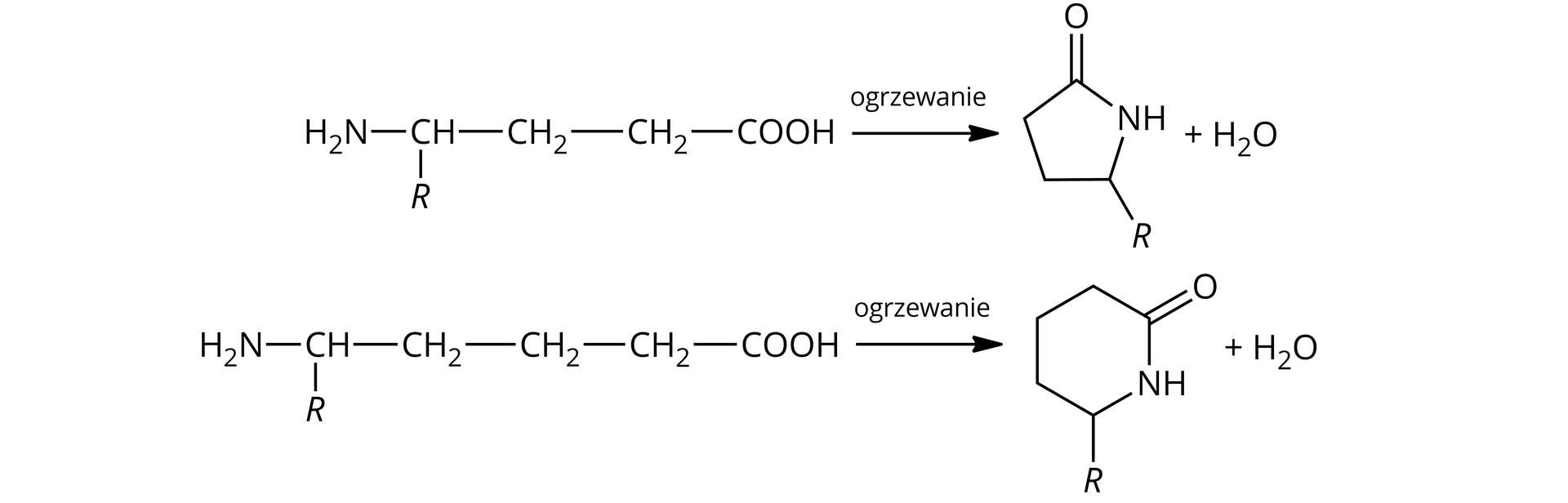
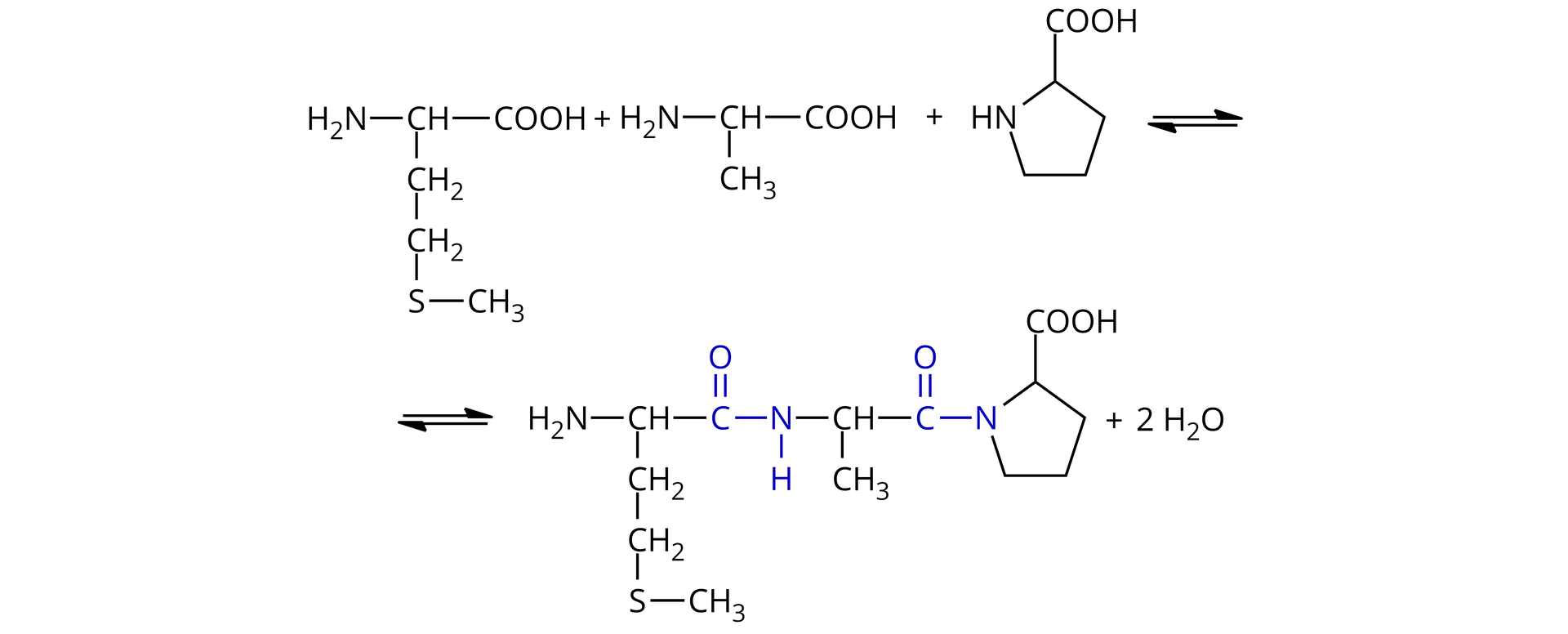
Poznaj proces tworzenia polipeptydów. Sprawdź swoją wiedzę, rozwiązując quiz dotyczący etapów syntezy polipeptydów.
Produkujemy polipeptydy
Zagraj w quiz sprawdzający Twoją wiedzę na temat produkcji polipeptydów. Gra składa się z trzech następujących po sobie etapów. Żeby przejść do kolejnego, konieczne jest ukończenie poprzedniego z pozytywnym wynikiem. W odpowiedzi na pytania może okazać się przydatna tabela aminokwasów zamieszczona poniżej. Powodzenia!
Indeks dolny Autor: Krzysztof Błaszczak Indeks dolny koniecAutor: Krzysztof Błaszczak
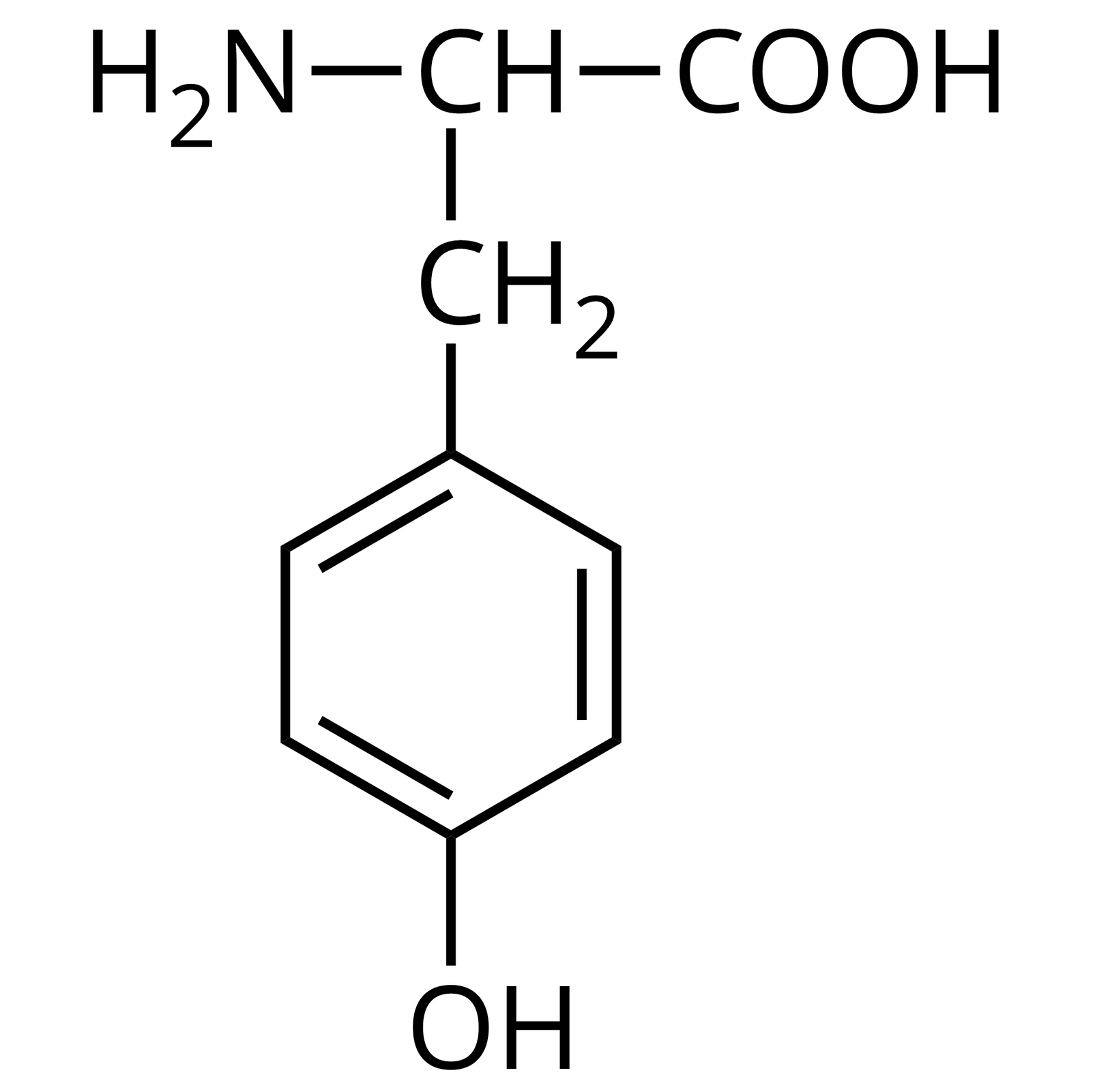
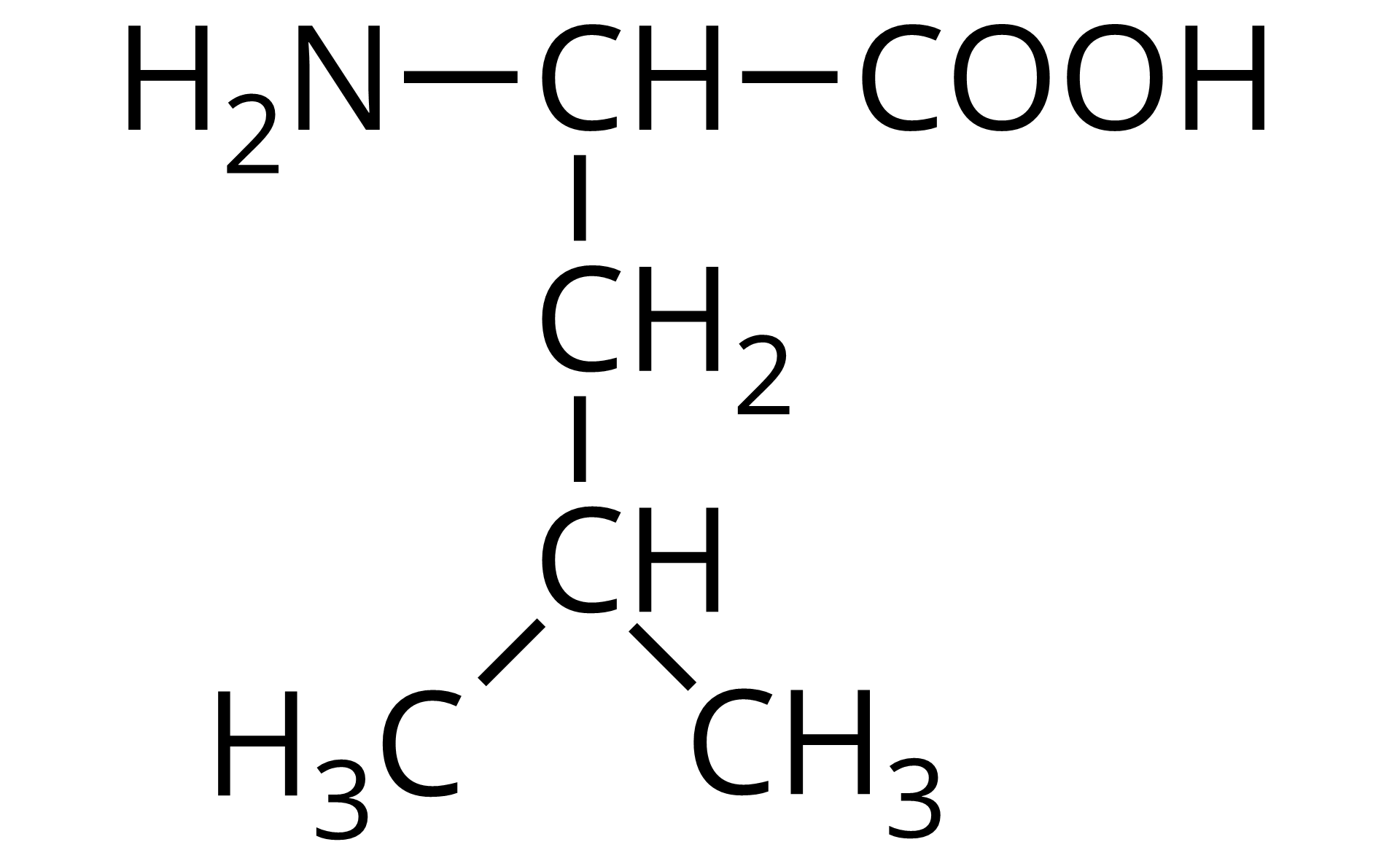
Wzór półstrukturalny | Nazwa zwyczajowa | Trzyliterowy kod |
|---|---|---|
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | glicyna | Gly |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | alanina | Ala |
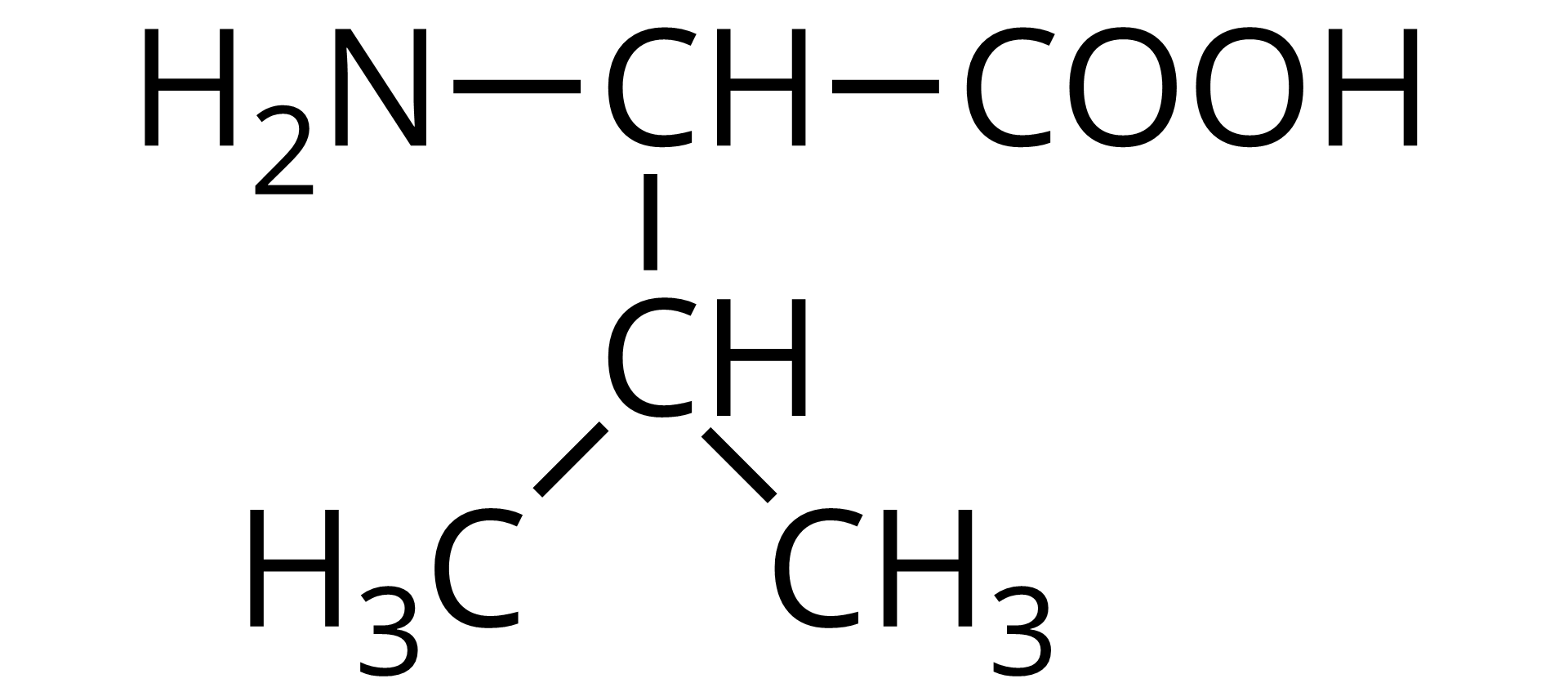
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | walina | Val |
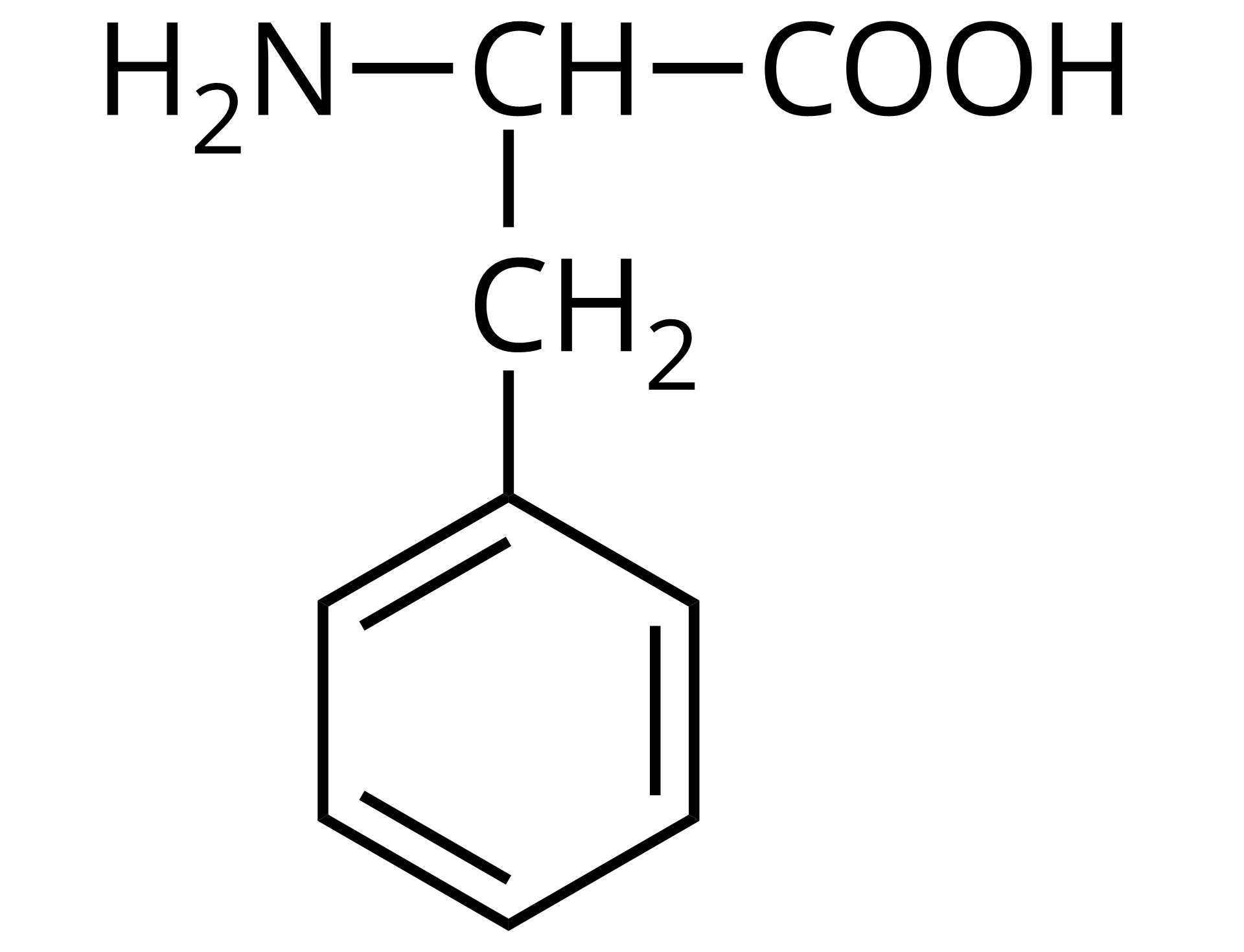
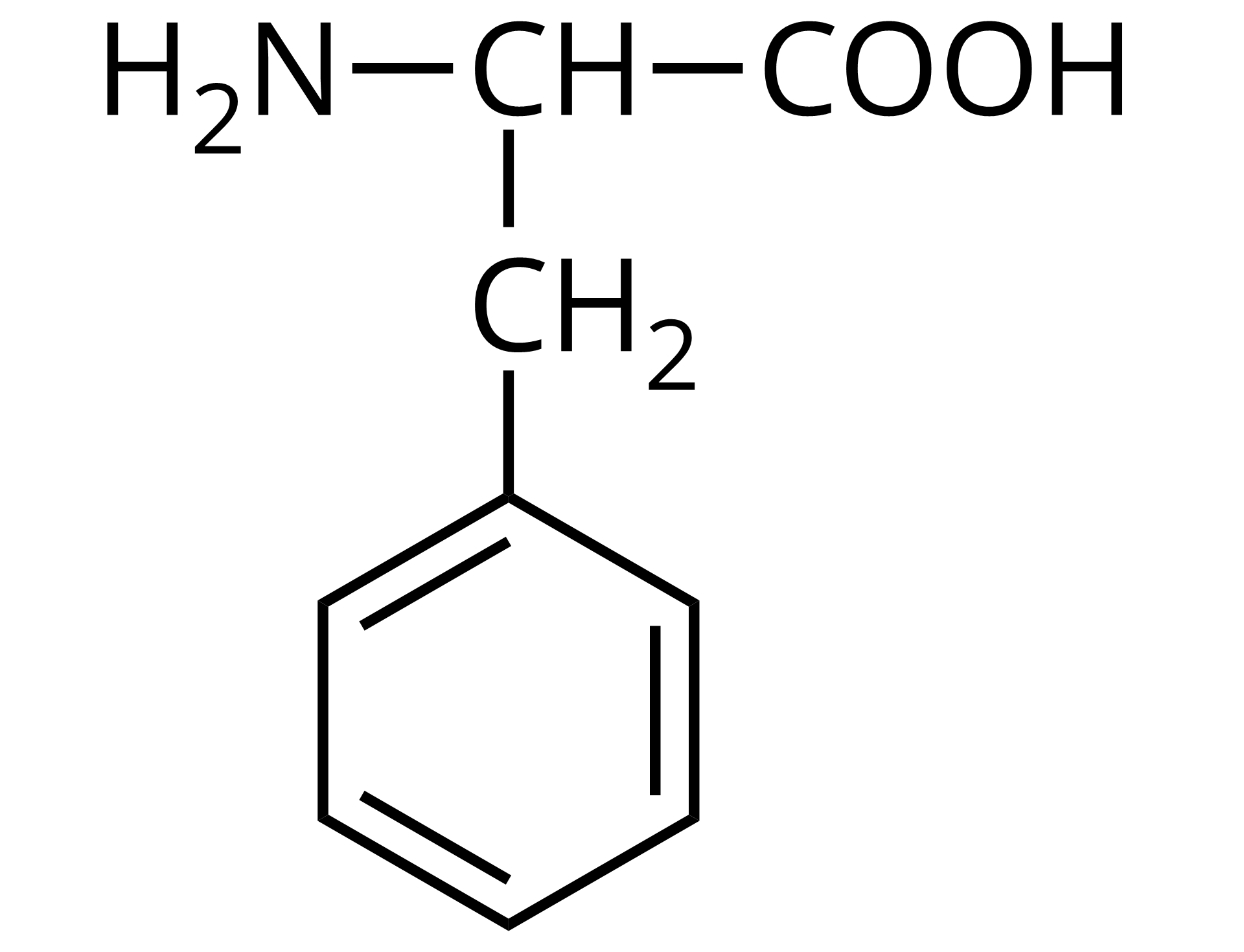 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | fenyloalanina | Phe |
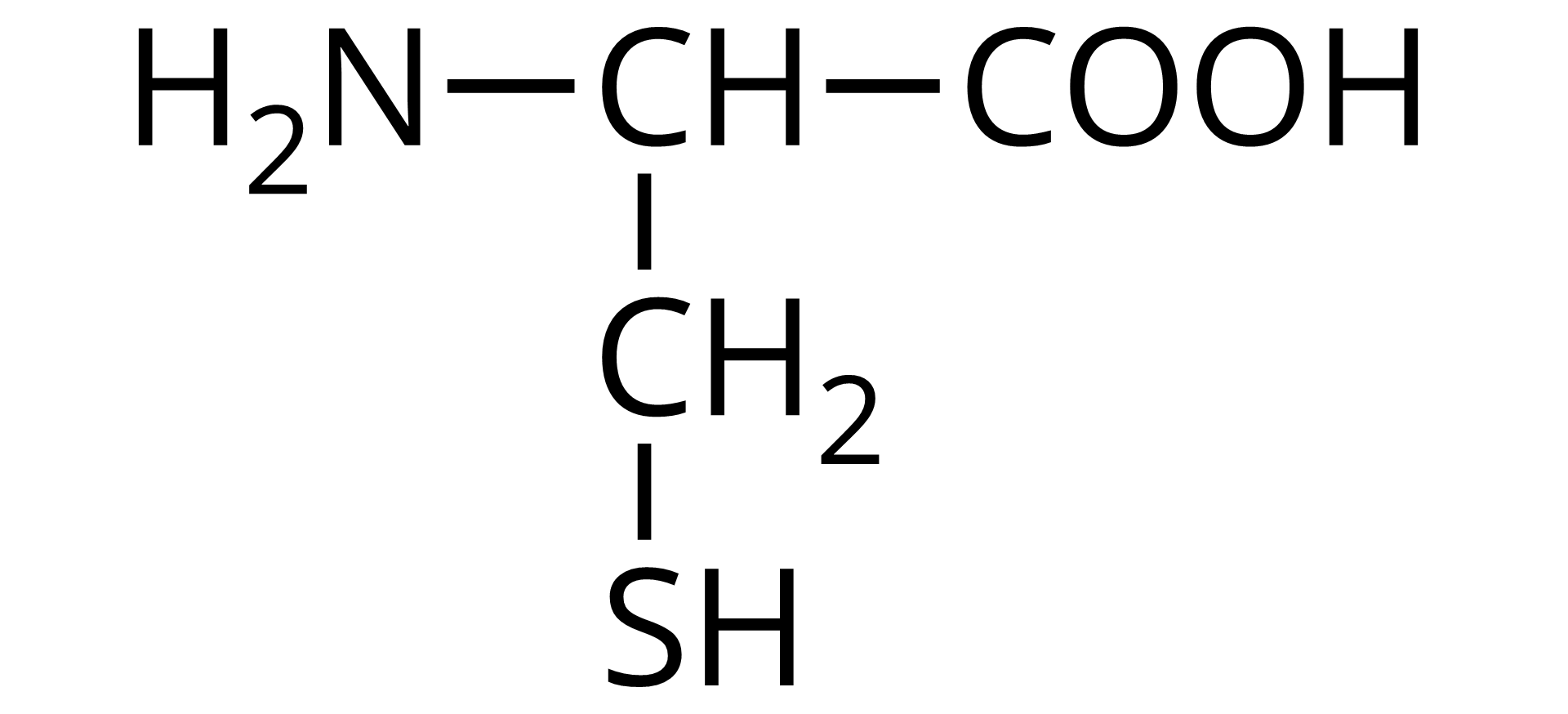
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | cysteina | Cys |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas glutaminowy | Glu |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | lizyna | Lys |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas asparaginowy | Asp |
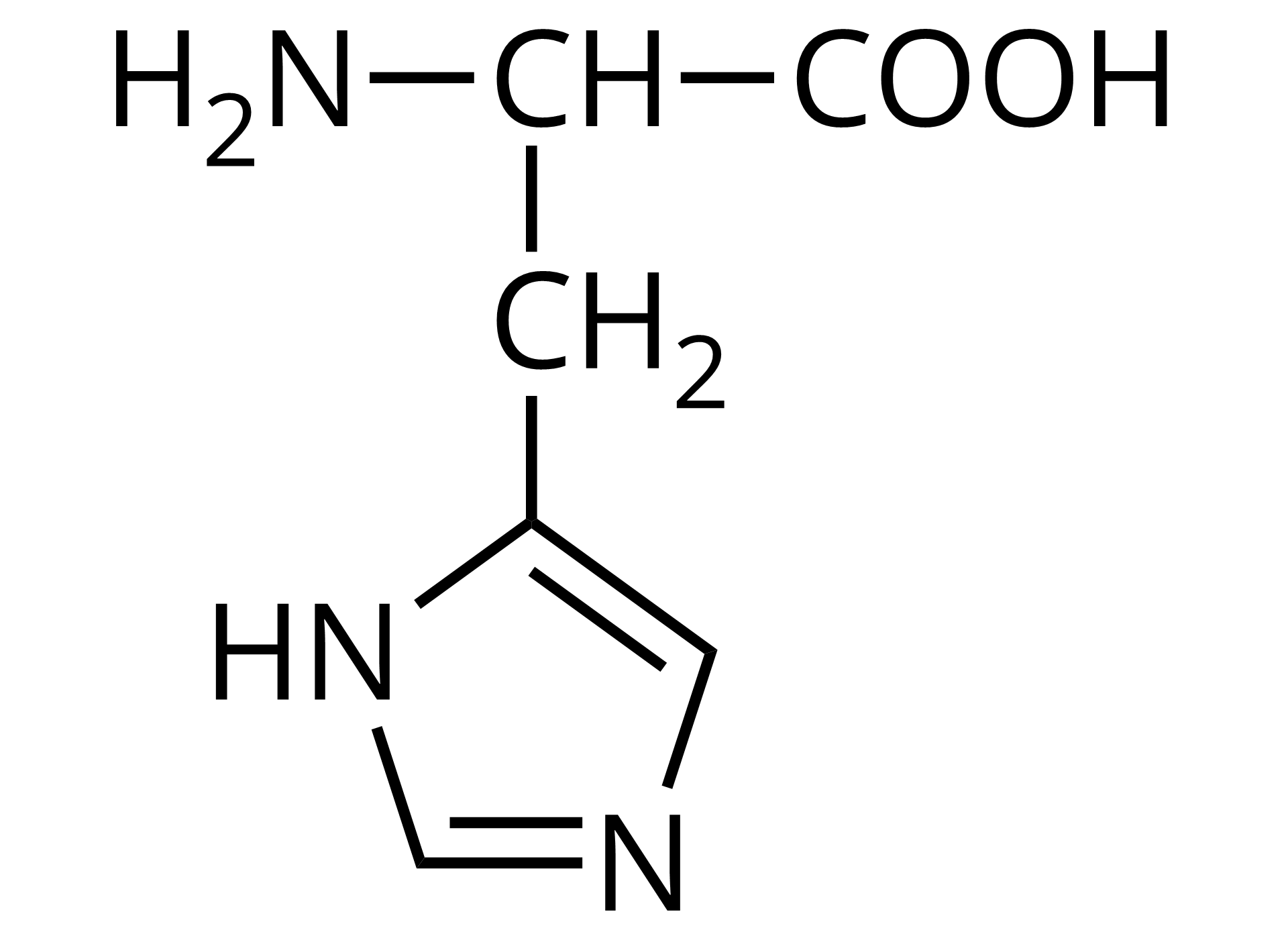
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | histydyna | His |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | izoleucyna | Ile |
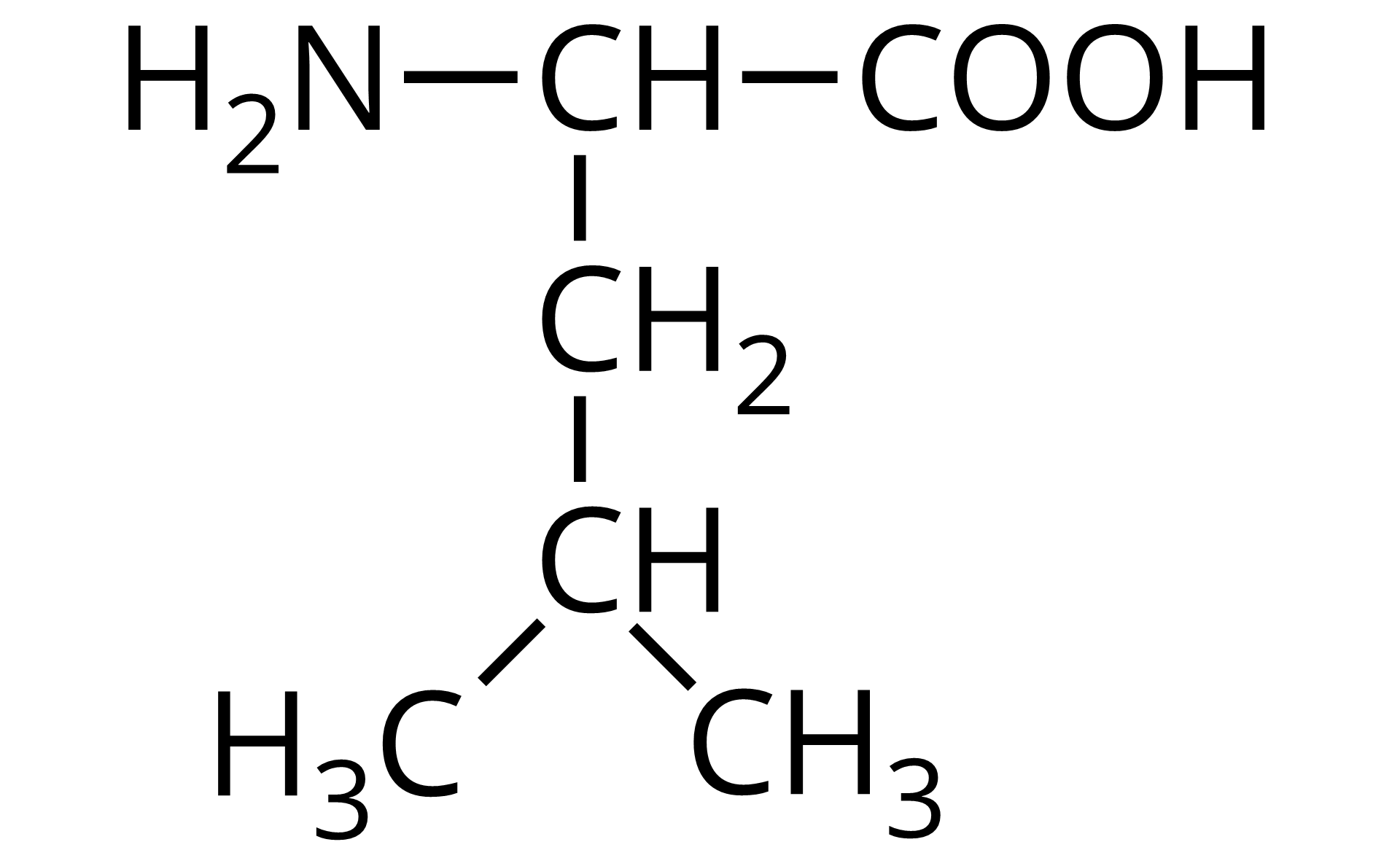 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | leucyna | Leu |
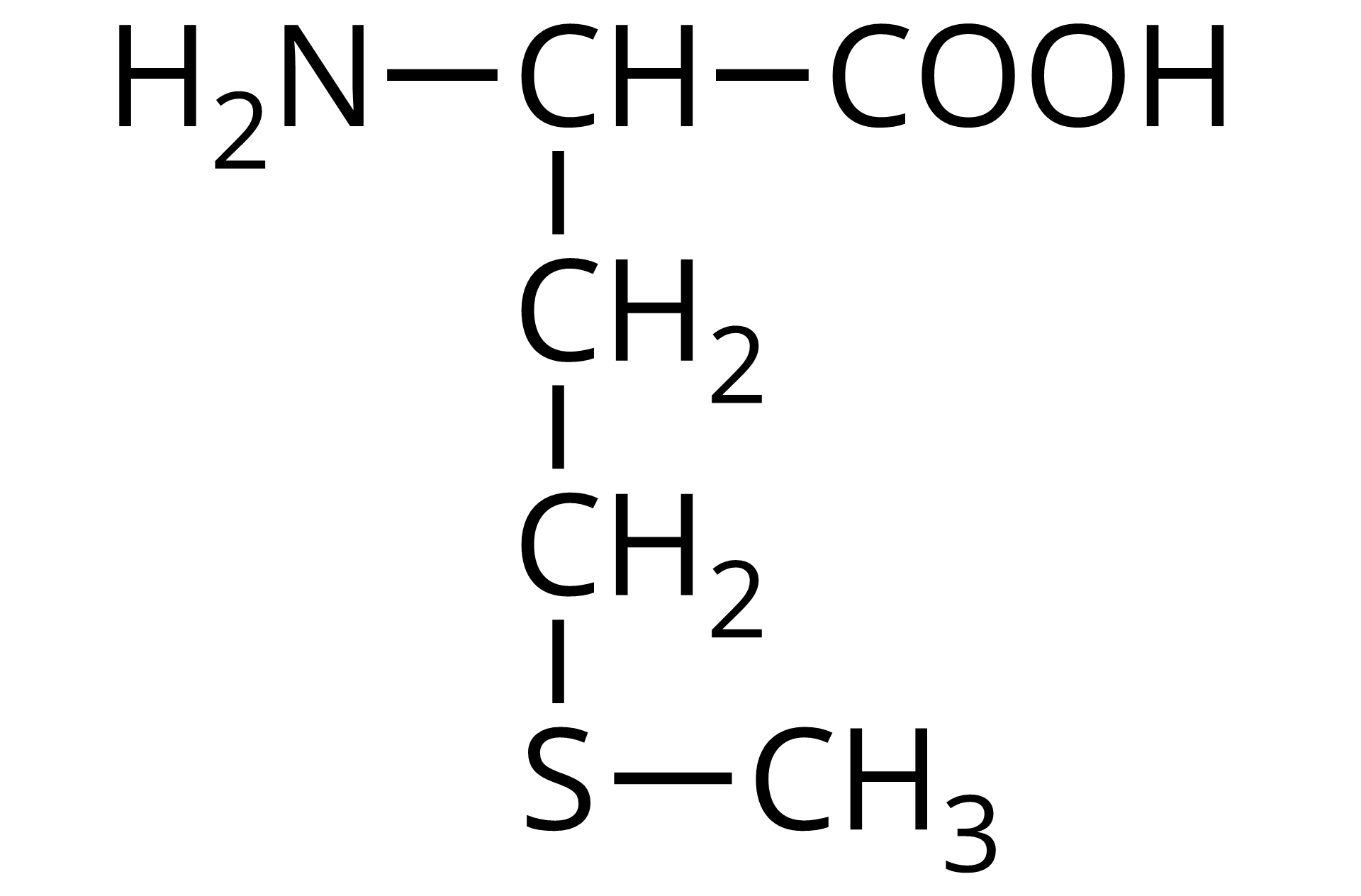 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | metionina | Met |
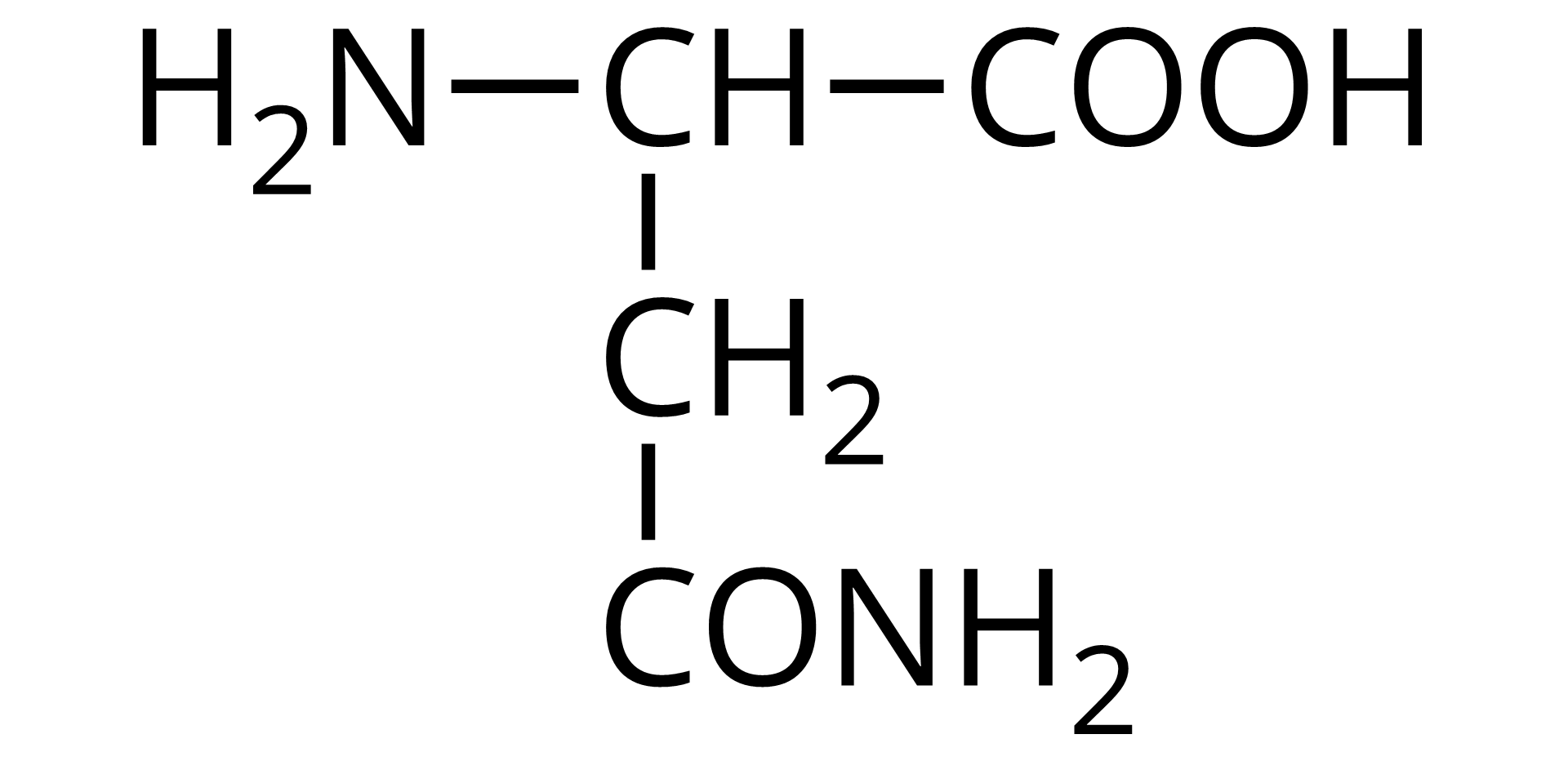 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | asparagina | Asn |
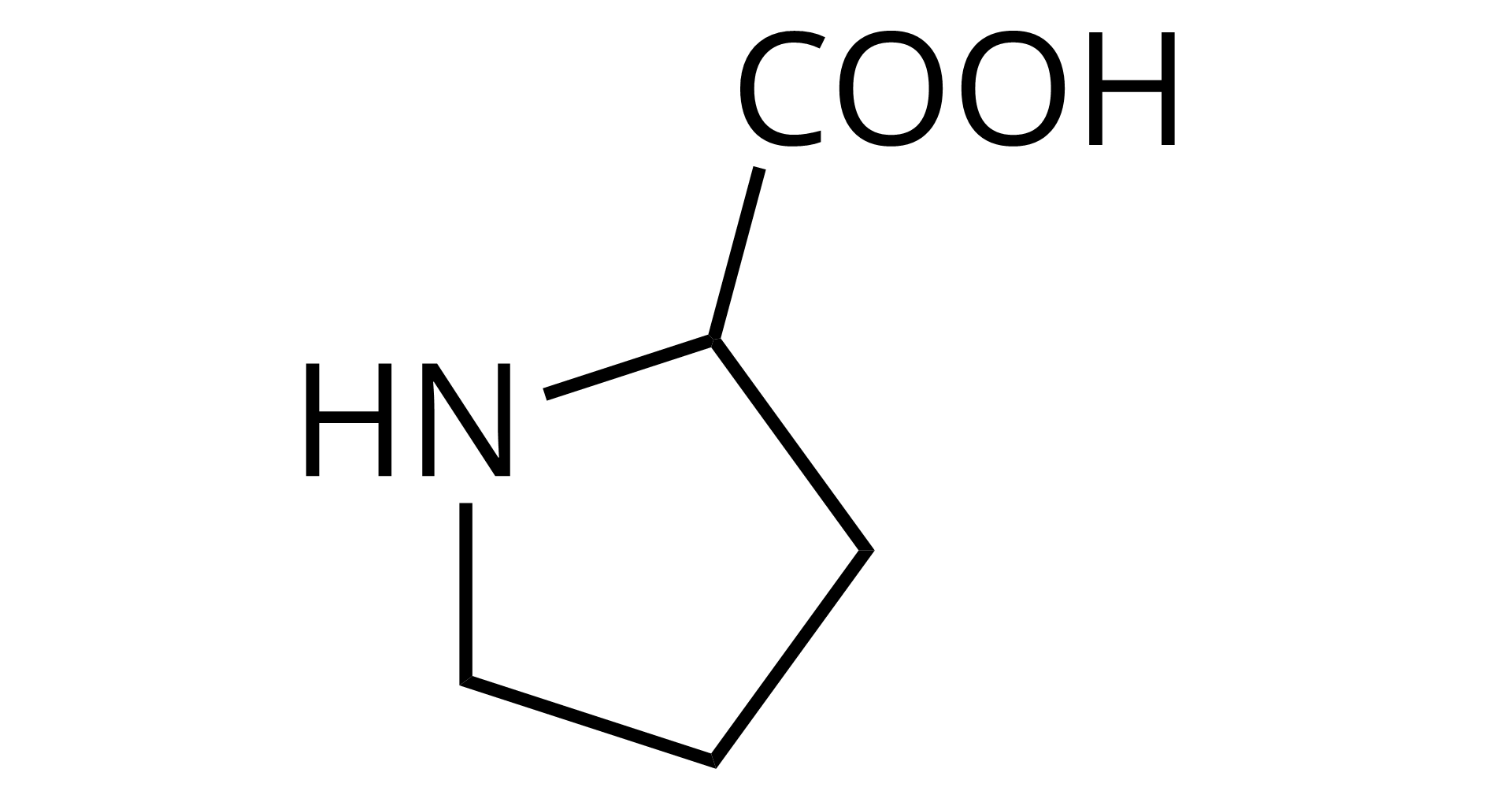
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | prolina | Pro |
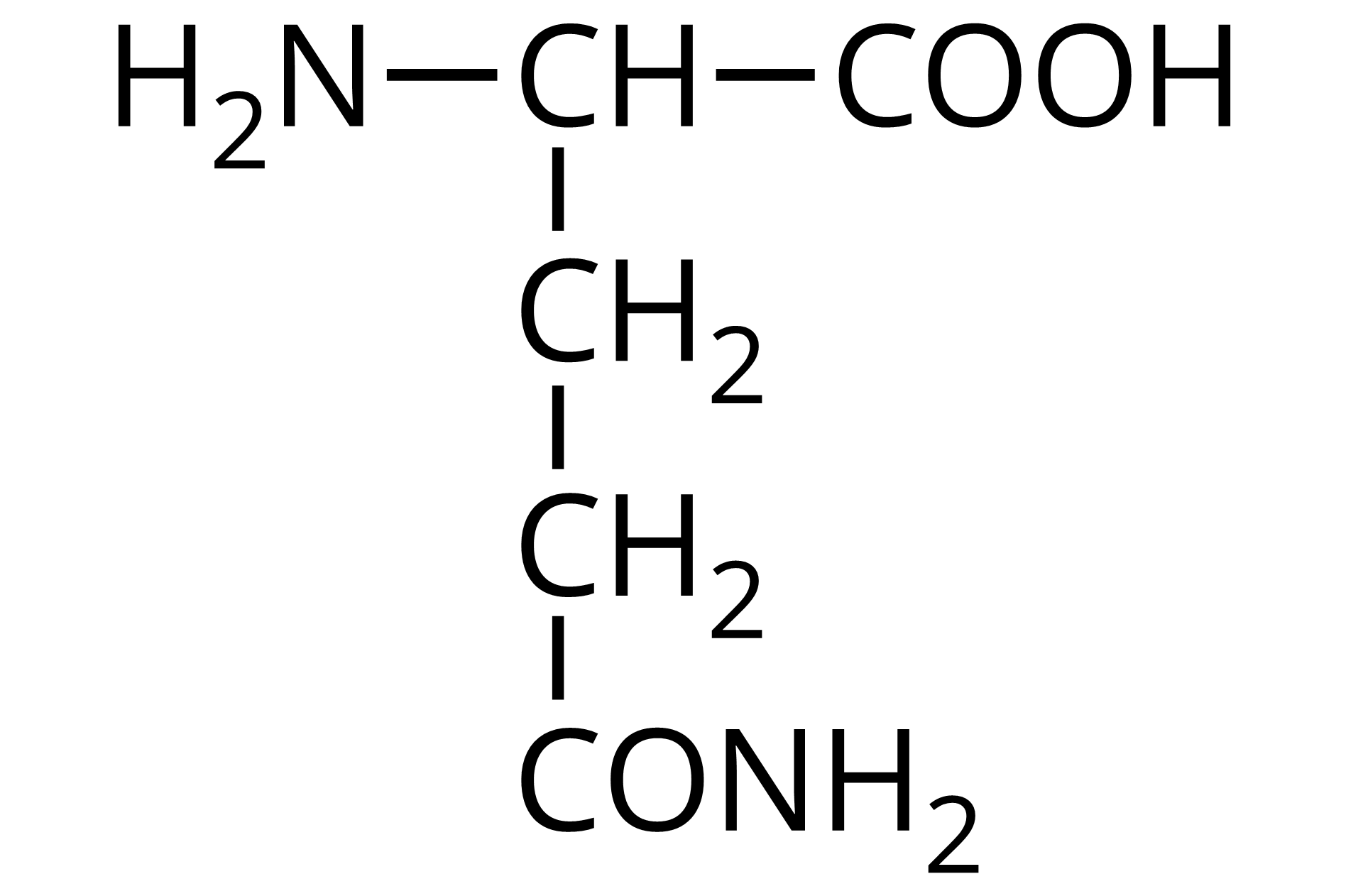 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | glutamina | Gln |
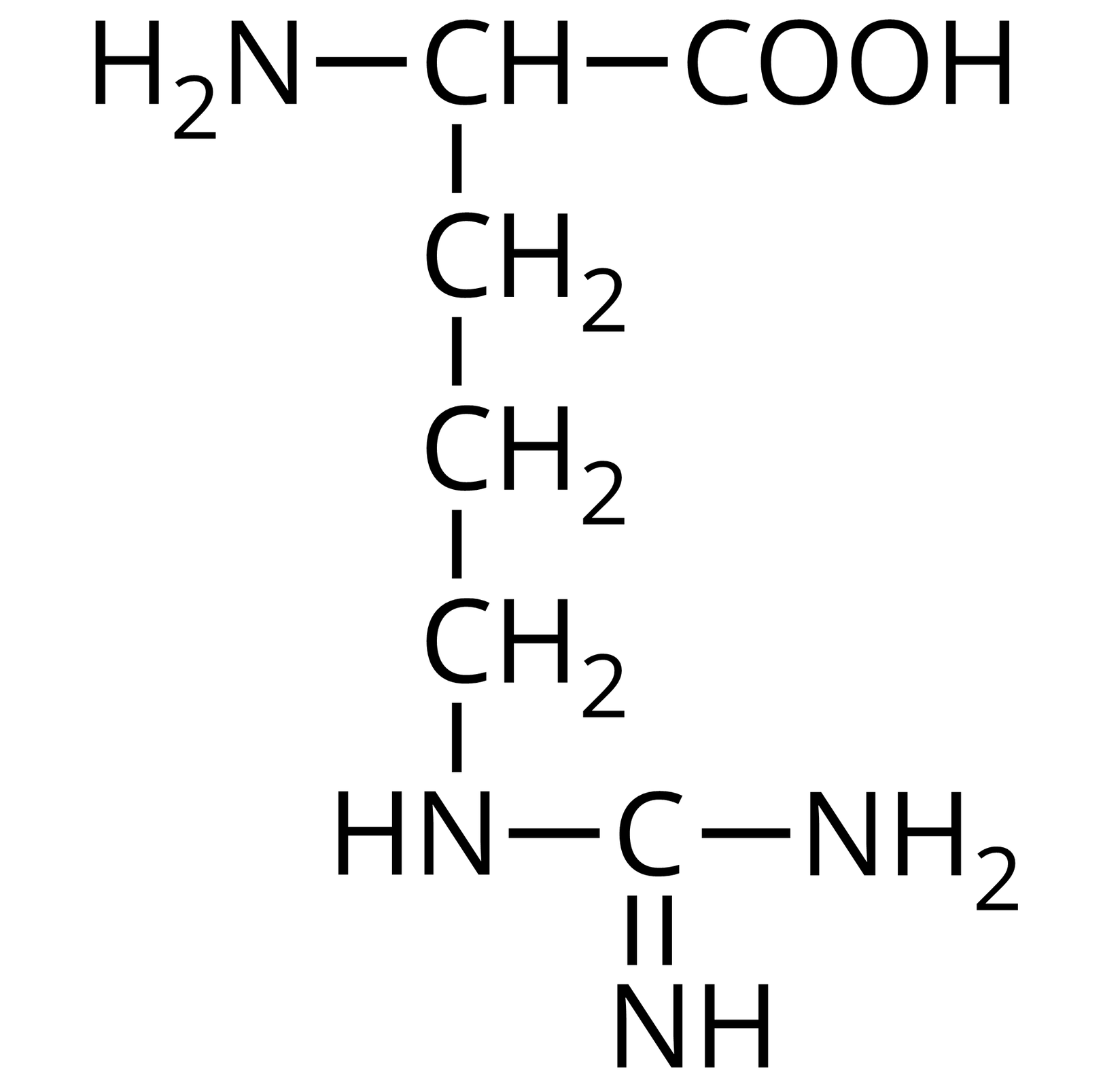 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | arginina | Arg |
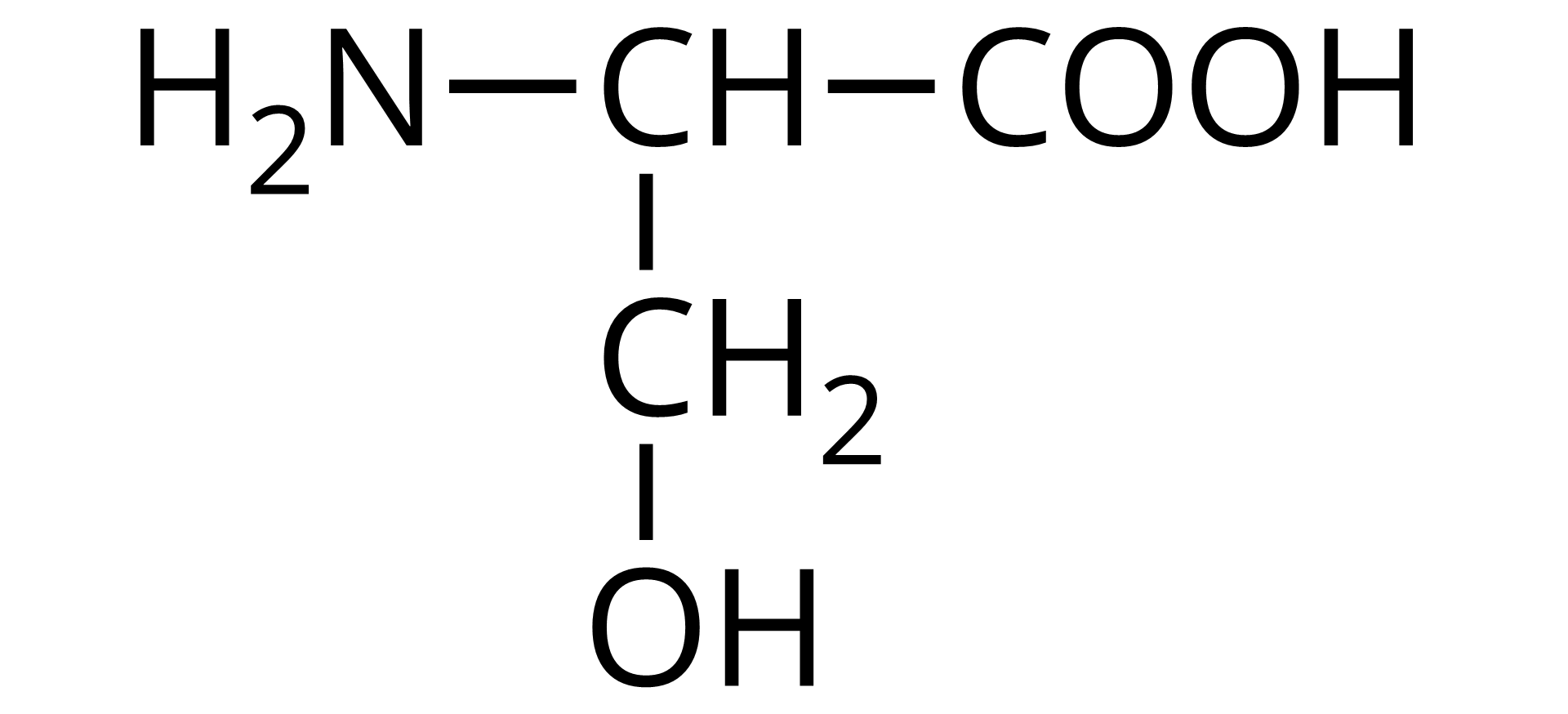
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | seryna | Ser |
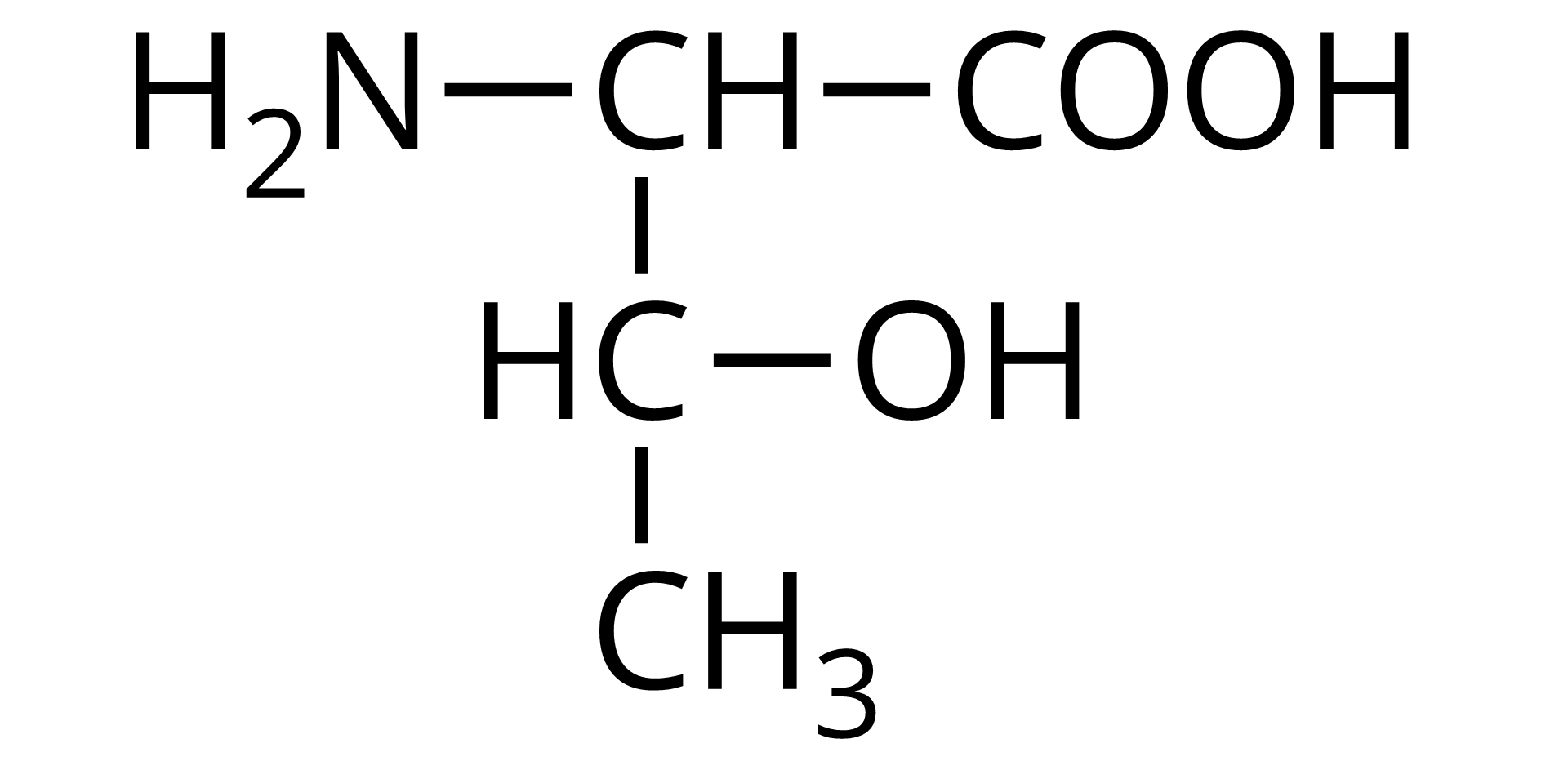 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | treonina | Thr |
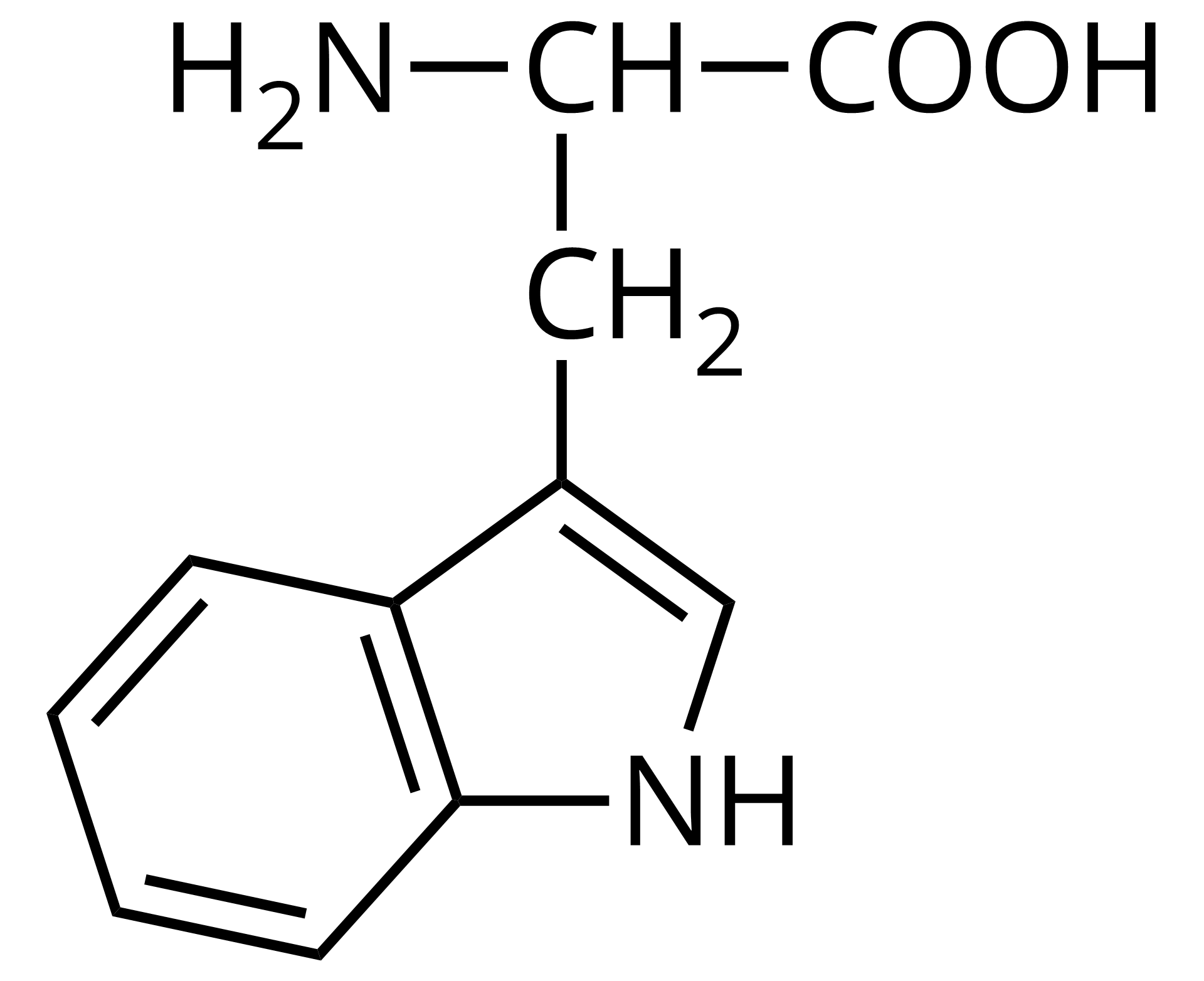 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | tryptofan | Trp |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | tyrozyna | Tyr |
Produkujemy polipeptydy
Hydroliza peptydów
Hydroliza jest reakcją odwrotną do reakcji kondensacji, czyli polega na rozerwaniu utworzonych wiązań peptydowych i odtworzeniu poszczególnych aminokwasów. Bierze w niej udział woda, której cząsteczki rozpadają się na jony hydroksylowe i jony hydroniowe , a następnie łączą się z uwolnionymi wiązaniami substancji wielkocząsteczkowej. Przemiany te można przedstawić uproszczonym schematem:
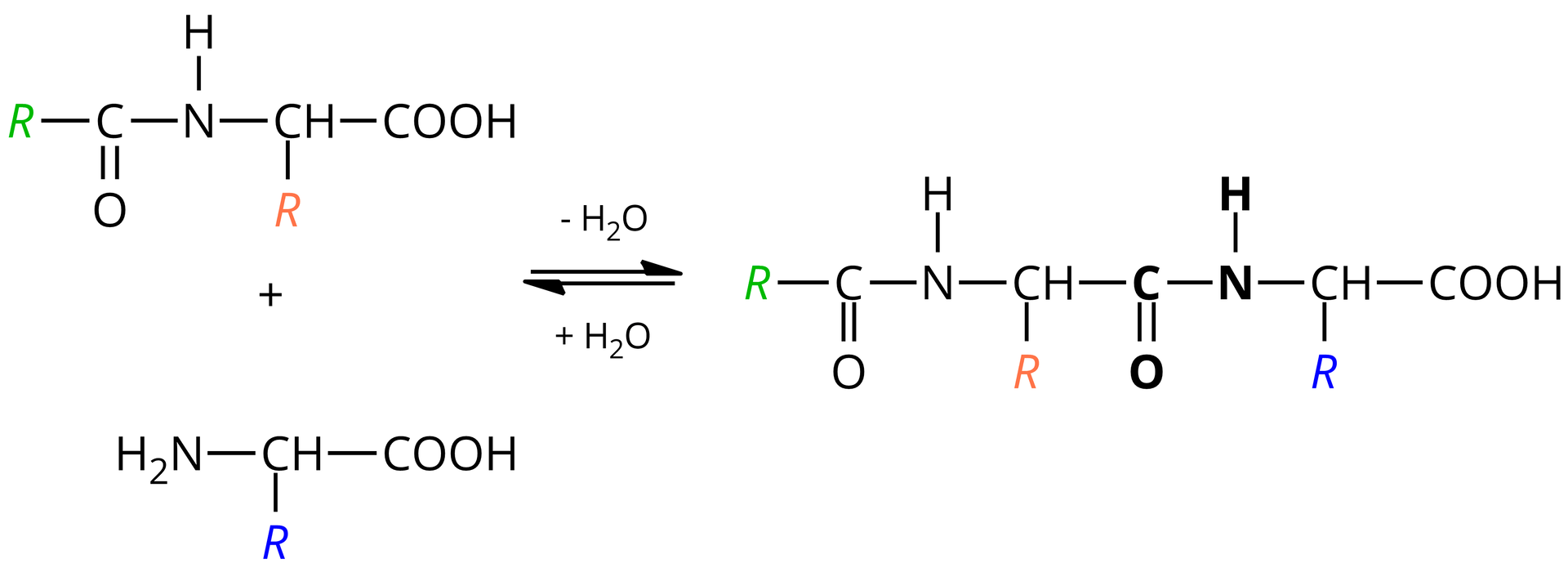
Peptydy, jak i białka, ulegają hydrolizie w środowisku wodnym i w podwyższonej temperaturze oraz w obecności stężonych kwasów nieorganicznych lub stężonych zasad.
W reakcji tej powstają odpowiednie aminokwasy. Analizując skład otrzymanych produktów hydrolizy, można ustalić, z jakich reszt aminokwasowych składał się dany peptyd.
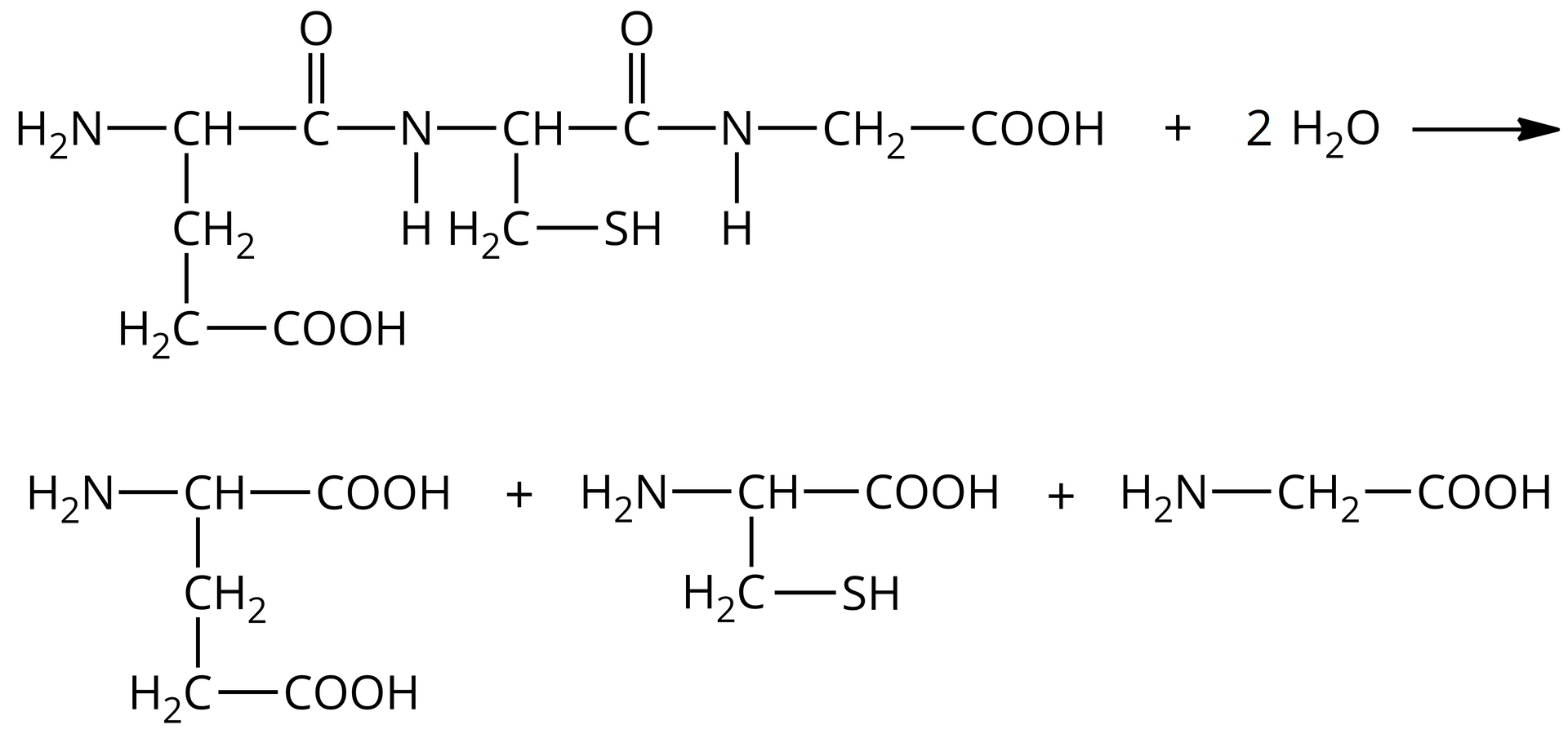
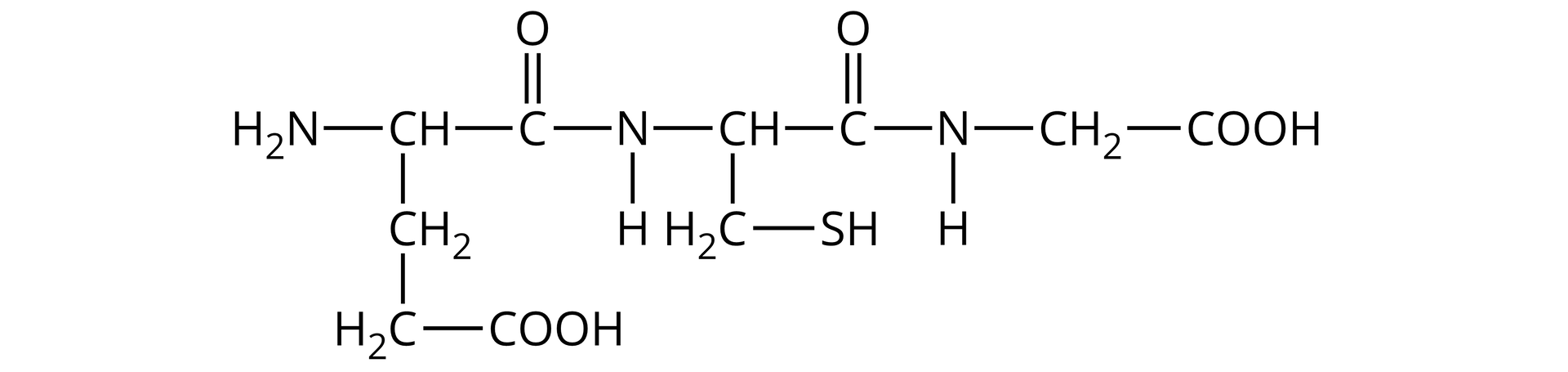
Przykładem peptydu, którego obecność stwierdzono w większości żywych komórek, jest glutation.
Ile i jakie aminokwasy powstaną w wyniku hydrolizy glutationu? Czy potrafisz zapisać tę reakcję?
**Sposoby przeprowadzania hydrolizy peptydów i białek zostały omówione w poniższym audiobooku. Po jego wysłuchaniu zapoznaj się z interaktywną grafiką i wykonaj ćwiczenia.
Zapoznaj się z audiobookiem oraz odpowiedz na pytania.
P. Brodalka, K. Felisiak, M. Szymczak, Hydrolizaty białkowe jako źródło biologicznie aktywnych peptydów – otrzymywanie i zastosowanie w przemyśle spożywczym, “Kosmos” 2018, nr 4, t.67, 889-894, GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Poniżej przedstawiono wzór pewnego peptydu.
Zapoznaj się z opisem wzoru pewnego peptydu.
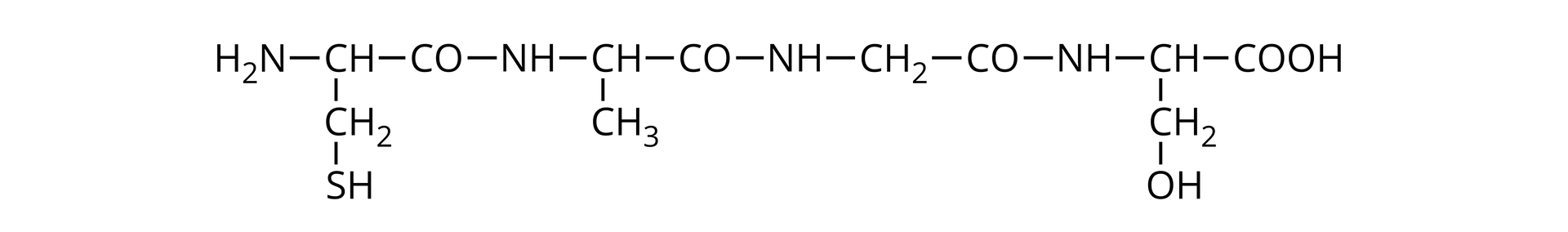
Pewien tripeptyd, którego wzór można zapisać z użyciem symboli trzyliterowych jako Phe‑Ala‑Gly, poddano całkowitej hydrolizie enzymatycznej w celu wydzielenia z układu fenyloalaniny.
Oblicz, ile gramów fenyloalaniny powstanie w wyniku całkowitej hydrolizy 1 kg opisanego tripeptydu. Wynik podaj w gramach z dokładnością do jedności.