Alotropowe odmiany węgla
Budowa odmian alotropowych węgla
AlotropiaAlotropia to zjawisko polegające na występowaniu różnych odmian tego samego pierwiastka, różniących się między sobą strukturą krystaliczną. Wszystkie odmiany składają się wyłącznie z atomów jednego pierwiastka, a zatem wszelkie różnice fizyczne i chemiczne muszą wynikać z połączeń atomów w strukturach.
W przypadku węgla w różnych jego odmianach alotropowych atomy wiążą się ze sobą na różne sposoby. Odmianami alotropowymi węgla są: grafit, diament, grafen, nanorurki węglowe oraz fullereny.
Grafit posiada strukturę zbudowaną z dwuwymiarowej jednostki heksagonalnej, w której każdy atom węgla jest połączony z trzema innymi atomami węgla wiązaniami kowalencyjnymi w tej samej warstwie. Między sobą warstwy układają się równolegle i związane są przez słabe siły Van der Waalsa. Dlatego grafit jest bardzo miękką odmianą węgla i potrafi pozostawić smugę na papierze.
W diamentach wszystkie atomy węgla w strukturze, o regularnej sieci przestrzennej o kształcie czworościanu foremnego (tetraedru), są połączone z czterema innymi atomami węgla za pomocą wiązań kowalencyjnych. Równomiernie rozłożone, krótkie i mocne wiązania kowalencyjne wpływają na bardzo dużą twardość, dlatego diament jest najtwardszą odmianą alotropową węgla.
Grafen jest to pojedyncza warstwa grafitu o hybrydyzacji orbitali walencyjnych atomów węgla . Jest to pierwszy materiał dwuwymiarowy jaki odkryto oraz jest to jeden z najtrwalszych materiałów na świecie (wytrzymałość na rozciąganie – gigapaskali).
Fullereny to jednowarstwowe cząsteczki o strukturze przypominającej kształt kuli, zbudowane z od do atomów węgla. Nanorurki węglowe to cylindryczne cząsteczki składające się ze zwiniętych arkuszy jednowarstwowych atomów węgla (grafenu), których orbitalom walencyjnym przypisujemy hybrydyzację .
Diament

Diament to minerał, naturalnie występujący w postaci przezroczystych (mogą mieć kolory w zależności od zanieczyszczeń), silnie załamujących światło kryształów, które charakteryzują się bardzo dużą twardością. Ma on dobre właściwości optyczne – przepuszcza promieniowanie od podczerwieni do nadfioletu. Na jego twardość ma wpływ wysoka energia wiązań , która wynosi . Ponadto diament ma właściwości izolatora elektrycznego. Jest bardzo dobrym przewodnikiem ciepła, odpornym na działanie stężonych zasad i nieutleniających kwasów. Diament ulega spaleniu w temperaturze wyższej od . Te właściwości czynią go niezwykle ważnym i drogim surowcem w wielu branżach.
Grafit

Grafit ma strukturę zbudowaną z regularnych sześciokątów o wspólnych bokach. Atomy węgla w strukturze grafitu połączone są silnymi wiązaniami kowalencyjnymi w obrębie każdej warstwy z trzema sąsiednimi atomami tego pierwiastka, natomiast słabe siły van der Waalsa pomiędzy jego warstwami ułatwiają poślizg w płaszczyznach. Grafit charakteryzuje się wysoką przewodnością elektryczną (dzięki zdelokalizowanym elektronom) i cieplną, większą niż żelazo i stal, lecz mniejszą niż miedź i aluminium. Dzięki temu zyskuje zastosowanie jako element uszczelniający czy ślizgowy (służący do ruchomego połączenia elementów). Ma on niską reaktywność, jest ogniotrwały (topi się w temperaturze około ) i odporny chemicznie (jest odporny na działanie wielu kwasów i zasad).

Fullereny
Fullereny to cząsteczki zbudowane z parzystej liczby atomów węgla (od do około atomów węgla). Mają one metaliczny połysk, własności nadprzewodzącenadprzewodzące i półprzewodnikowe. Pod względem chemicznym mają właściwości zbliżone do sprzężonych węglowodorów aromatycznych, ponieważ składają się z układu sprzężonych pierścieni o pięciu i sześciu atomach węgla.
Zostały odkryte w roku przez Roberta Curla, Richarda Smalleya oraz Harolda Kroto. Eksperyment prowadzący do odkrycia kolejnej odmiany alotropowej węgla polegał na zastosowaniu laserowego naddźwiękowego generatora klastrów.

Promień laseralasera kierowany był na wolno obracającą się tarczę grafitową w obecności helu. Następnie węgiel w postaci gazowej kierowany był na spektrometr masowy (urządzenie pozwalające analizować masy jonów), który pozwalał zarejestrować masę nowo powstałych cząsteczek fullerenów.
Kolejne lata dostarczyły wielu innych technik syntezy fullerenów jednak najbardziej standardową metodą ich otrzymywania jest metoda płomieniowa. Polega ona na spalaniu acetylenu lub benzenu w tlenie. Wydajność tej metody jest niska () jednak ma istotne zalety jak ciągłość procesu, łatwość kontroli oraz możliwość zwiększenia skali produkcji.
Fullereny i nanorurki węglowe to jedyny przykład czystej węglowej odmiany alotropowej węgla, ponieważ wiązania brzegowe w diamencie i graficie są „wysycone” innymi pierwiastkami.
Nanorurki
Nanorurki węglowe to szczególny przykład izomerówizomerów fullerenów, mający doskonałe właściwości mechaniczne i elektryczne. Są to bardzo sprężyste i elastyczne materiały (moduł Youngamoduł Younga ), mają dobrą wytrzymałość przy rozciąganiu oraz zginaniu. Co ciekawe mają –krotnie większą wytrzymałość na rozciąganie od stali i razy większą gęstość prądu od miedzi. Są odporne na działanie wysokiej temperatury sięgającej nawet do .
Nanorurki otrzymuje się na skutek powolnej kondensacji gorących par atomów węgla. Struktura zamknięta nanorurek powstaje na skutek łączenia się niestabilnych, płaskich warstw węglowych (na brzegach płaskich płaszczyzn występują nienasycone wiązania o wysokiej energii).
Ze względu na swoje właściwości chemiczne, mechaniczne i elektryczne nanorurki znajdują zastosowanie w różnych gałęziach gospodarki jako bioczujniki, tranzystory, akumulatory litowo‑jonowe oraz materiały magazynujące wodór.
Grafen

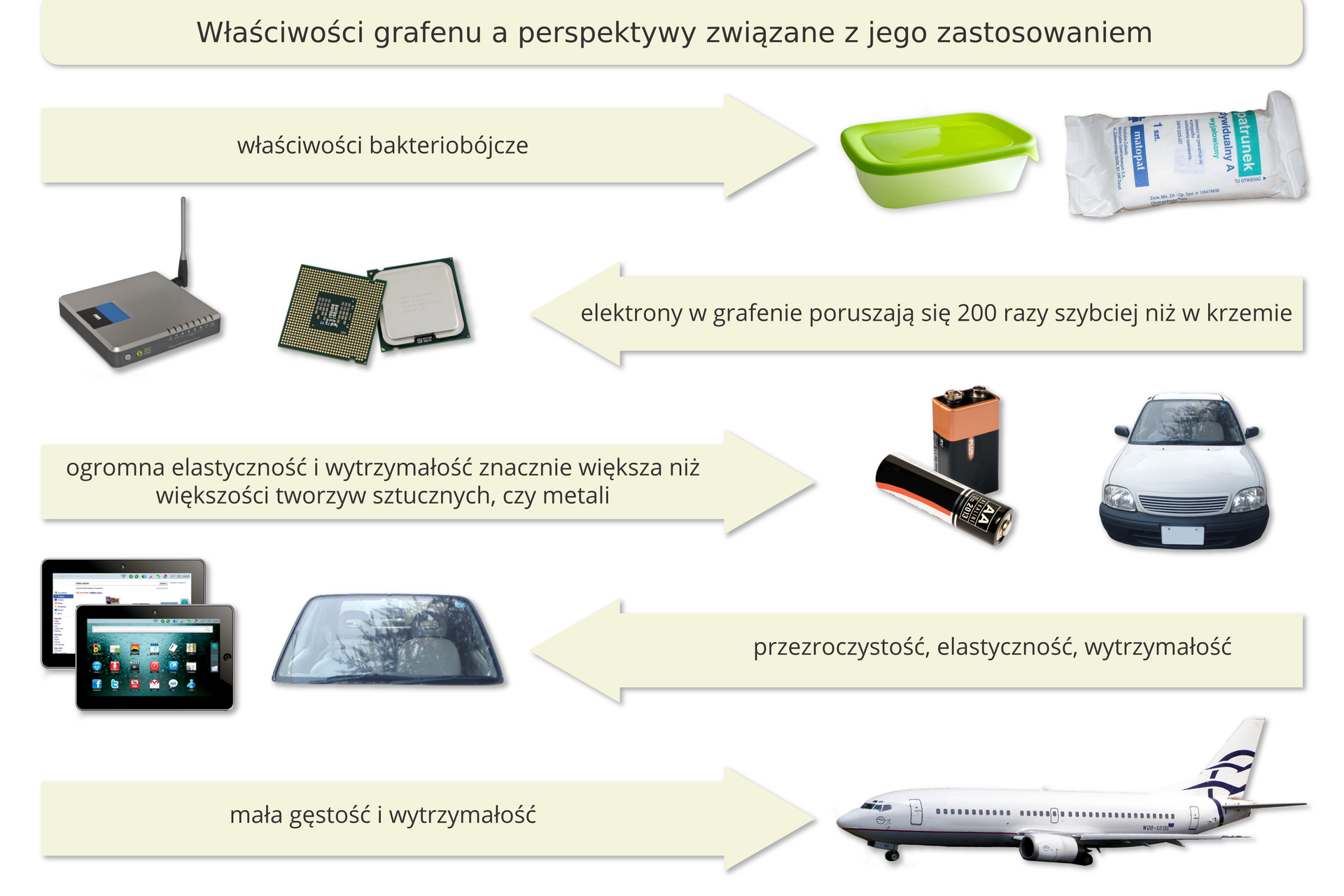
Grafen to przezroczysty materiał i dobry przewodnik prądu. Elektrony poruszają się w nim razy szybciej niż w krzemie. Jest również dobrym przewodnikiem ciepła i bardzo wytrzymałym materiałem ( razy bardziej wytrzymały od stali).
Grafen można otrzymać w wyniku metody taśmy klejącej. Metoda ta polega na odrywaniu kolejnych warstw grafenu od grafitu, do momentu uzyskania pojedynczej warstwy grafenu. Obecnie do otrzymywania grafenu stosowana jest metoda osadzania chemicznego z fazy gazowej. Jest to metoda obróbki cieplno–chemicznej materiałów, która pozwala na nanoszenie cienkich powłok materiału.
Badania odmian alotropowych węgla
Jakość i czystość alotropów węgla można badać przy użyciu spektroskopii ramanowskiej. Jest to technika spektroskopowa, polegająca na pomiarze promieniowania nieelastycznego rozpraszania fotonówfotonów. Zastosowanie jej i analiza otrzymanych pasm na widmie, pozwala sprawdzić np. czy grafen jest zanieczyszczony lub czy występują w nim nieuporządkowania sieci krystalicznej, które mogą mieć istotny wpływ na uzyskanie przerwy energetycznej w jego strukturze.
Właściwości wynikające ze specyficznej budowy związków można badać i obserwować poprzez wykorzystanie transmisyjnego mikroskopu elektronowego (TEM).

Inną znaną metodą pozwalającą potwierdzić identyfikację fullerenów w materiale doświadczalnym jest spektroskopia magnetycznego rezonansu jądrowego (NMR). Jest to metoda, która wyczuwa zmiany struktury elektronowej wokół jądra atomowego i obecność innych jąder, dlatego NMR jest bardzo ważnym narzędziem analizy strukturalnej. Widma węglowe otrzymane w wyniku tej metody pozwalają potwierdzić symetryczną i złożoną budowę tych form alotropowych węgla.
Węgiel występuje w różnych odmianach alotropowych, które różnią się określonymi właściwościami fizycznymi. Na podstawie poniższej symulacji dokonaj analizy wybranych właściwości grafitu, diamentu, grafenu, fullerenu i nanorurek węglowych, zwróć uwagę na poszczególne różnice i rozwiąż zadania.
Węgiel występuje w różnych odmianach alotropowych, które różnią się określonymi właściwościami fizycznymi. Na podstawie opisu poniższej symulacji zapoznaj się z analizą wybranych właściwości grafitu, diamentu, grafenu, fullerenu i nanorurek węglowych, zwróć uwagę na poszczególne różnice i rozwiąż zadania.
- Pierwszą odmianą jest grafit. Struktura grafitu składa się z warstw, w których występują sześcioczłonowe aromatyczne układy cykliczne. Na ilustracji są dwie warstwy. Każdy atom węgla w danej warstwie łączy się trzema innymi atomami węgla w tej samej warstwie. Zastosowania grafitu:
- klocki hamulcowe w samochodach,
- suchy smar,
- materiały konstrukcyjne (kompozyty).
- Drugą odmianą jest diament. Struktura diamentu: każdy atom węgla połączony jest wiązaniami kowalencyjnymi z czterema innymi atomami węgla, atomy węgla w diamencie tworzą regularną sieć przestrzenną, a każdy atom węgla ma hybrydyzację typu . Zastosowania diamentu:
- jubilerstwo,
- wyrób ostrych narzędzi.
- Trzecią odmianą jest grafen. Struktura grafenu jest płaska, złożona z atomów węgla tworzących sześcioczłonowe pierścienie. Struktura przypomina plaster miodu. Każdy atom węgla łączy się z trzema innymi atomami węgla w warstwie. W przeciwieństwie do grafitu, grafen zbudowany jest z pojedynczej warstwy, zatem warstwa grafenu ma grubość jednego atomu węgla. Zastosowania grafenu:
- czujniki,
- wyświetlacze dotykowe.
- Czwartą odmianą są fullereny. Ilustracja przedstawia strukturę fullerenu, który tworzą połączone ze sobą sześcio- i pięcioczłonowe pierścienie zbudowane z atomów węgla. Tworzą kulistą formę. Każdy atom węgla w strukturze łączy się z trzema innymi atomami węgla w warstwie. Zastosowanie fullerenów:
- medycyna,
- lotnictwo,
- optyka,
- elektrochemia.
- Piątą odmianą są nanorurki węglowe. Mają postać pustych w środku walcowatych tworów, których ściany zbudowane są z warstwy utworzonej przez sześcioczłonowe pierścienie węglowe. Każdy atom węgla w warstwie łączy się z trzema innymi również należącymi do tejże warstwy. Zastosowanie nanorurek węglowych:
- układy elektroniczne,
- jako materiał konstrukcyjny.
- Pierwszą właściwością jest przewodnictwo elektryczne. Kolejno włączano do obwodu elektrycznego z żarówką odmiany alotropowe węgla. Grafit, grafen oraz nanorurki węglowe po zamknięciu obwodu przewodziły prąd elektryczny, czego dowodziło zaświecenie się żarówki. W przypadku diamentu i fullerenów żarówka nie zapalała się. Na wyświetlaczu pojawiała się wartość przewodnictwa elektrycznego. Dla grafitu 1200 wat na milikelwin. Dla diamentu 2250 wat na milikelwin. Dla grafenu 5000 wat na milikelwin. Dla fullerenów 0,4 wat na milikelwin. Dla nanorurek węglowych 3500 wat na milikelwin.
- Kolejną właściwością jest przewodnictwo cieplne. Ogrzewano wybraną odmianę alotropową węgla ciepłem płomienia świecy. Dla grafitu wyświetlacz miernika wskazał delta T równe , dla diamentu , dla grafenu , dla fullerenów , dla nanorurek węglowych 4.
- Kolejną właściwością jest twardość oceniania w skali Mohsa. Dla grafitu, przedstawionego jako szaroczarna połyskliwa bryła, twardość wynosi , dla diamentu, przedstawionego jako przezroczysty, świetlisty kryształ, twardość wynosi , dla fullerenów, przedstawionych jako szaroczarna połyskliwa sztabka, twardość wynosi , dla grafenu i nanorurek węglowych brak danych. Dla porównania twardość szkła wynosi .
- Kolejną właściwością jest połysk. Do badań wykorzystano lupę i światło żarówki. Grafit, fullereny oraz nanorurki węglowe są lekko połyskliwe, a diament i grafen bardziej połyskliwe od uprzednio wspomnianych.
- Kolejną właściwością jest gęstość. Do pomiarów wykorzystano piknometr, wagę laboratoryjną oraz cylinder z wodą. Aby wyliczyć gęstość, najpierw zmierzono następujące masy:
- piknometru,
- piknometru z wodą,
- piknometru z badanym ciałem stałym
- piknometru z badanym ciałem stałym i wodą.
- dla grafitu: grama na centymetr sześcienny;
- dla diamentu: grama na centymetr sześcienny;
- dla grafenu: grama na centymetr sześcienny;
- dla fullerenów: grama na centymetr sześcienny;
- dla nanorurek węglowych: grama na centymetr sześcienny.
- Ostatnia badana właściwość to rozpuszczalność w wodzie. Wszystkie badane odmiany alotropowe są nierozpuszczalne w wodzie.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D6EMF24GK
Wyjaśnij, co oznacza, że diamentowi przypisuje się twardość równą w skali Mohsa.
Wymień alotropowe odmiany węgla, które przewodzą prąd elektryczny.
Wiedząc, że w graficie orbitale walencyjne atomów węgla znajdują się w stanie hybrydyzacji , a w diamencie w stanie hybrydyzacji , wyjaśnij dlaczego:
Podsumowanie
Różnice w budowie wewnętrznej poszczególnych odmian alotropowych węgla skutkują zróżnicowanymi właściwościami tych odmian – m.in. właściwościami elektrycznymi, termicznymi oraz fizycznymi.
Nazwa | Grafit | Diament | Grafen | Fullereny | Nanorurki węglowe |
|---|---|---|---|---|---|
Struktura | 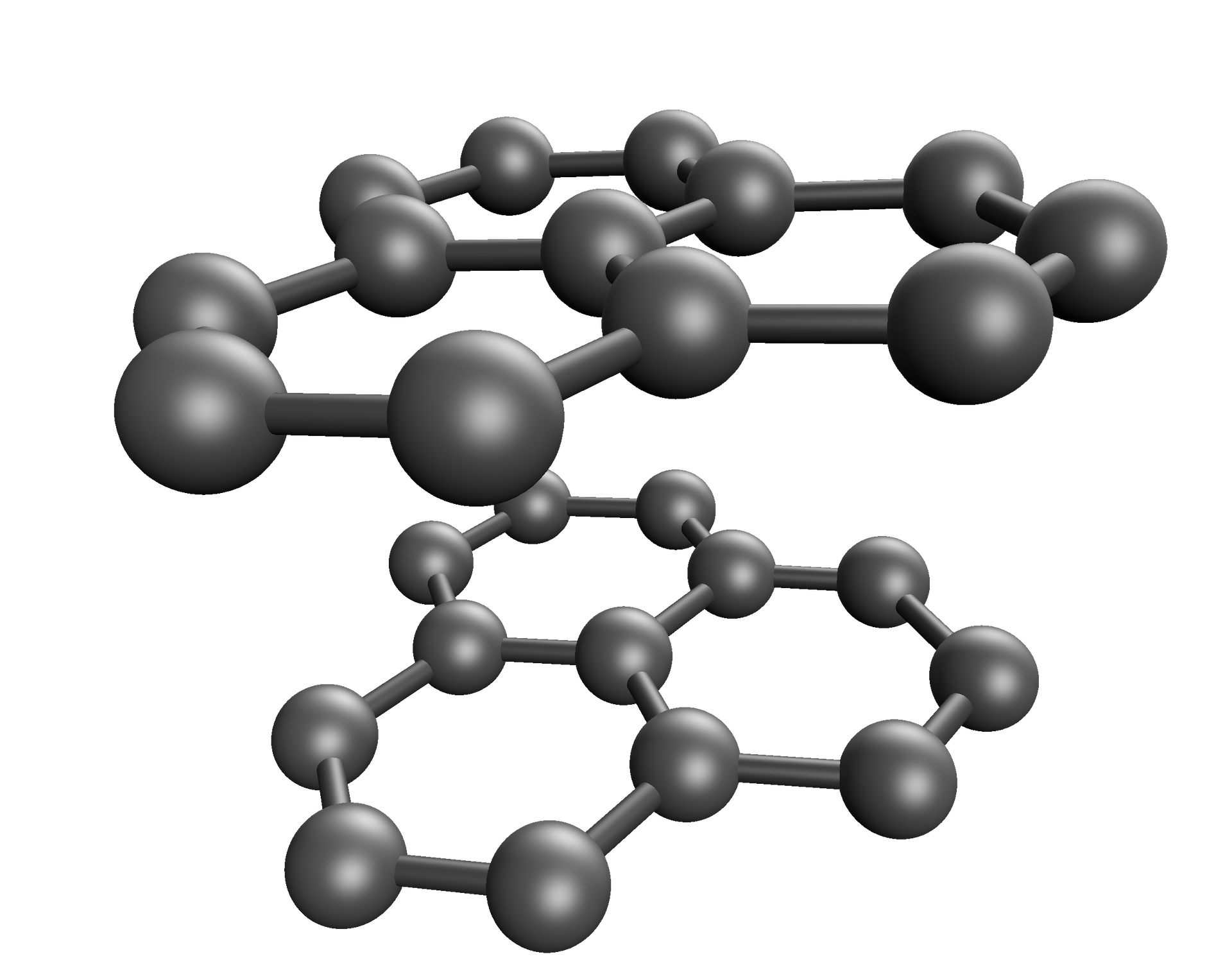 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |  Źródło: GroMar Sp. z o.o., licencja: CC BY 3.0. |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Przewodność elektrycznaPrzewodność elektryczna | tak | nie | tak | nie | tak |
Przewodność cieplnaPrzewodność cieplna | stosunkowo niska | wysoka | wysoka | wysoka | wysoka |
Typ hybrydyzacji orbitali walencyjnych atomów węgla | i | ||||
Wygląd | ciemnoszary z metalicznym połyskiem | bezbarwny lub barwny (zanieczyszczony) | bezbarwny | czarne ciało stałe | czarne ciało stałe |
Właściwości | nierozpuszczalny w wodzie i miękki | nierozpuszczalny w wodzie, kruchy | elastyczny | nierozpuszczalne w wodzie, rozpuszczalne w niektórych niepolarnych rozpuszczalnikach np. w benzenie | nierozpuszczalne w wodzie i rozpuszczalnikach organicznych, elastyczne i sprężyste |
Zastosowanie | wkład do ołówków, smar i materiał ogniotrwały | w jubilerstwie, półprzewodnikach i jako narzędzie do cięcia | elektronika, półprzewodniki i filtracja wody | w fotooptyce i w elektronice, nośniki leków | w produkcji sprzętu sportowego, |
