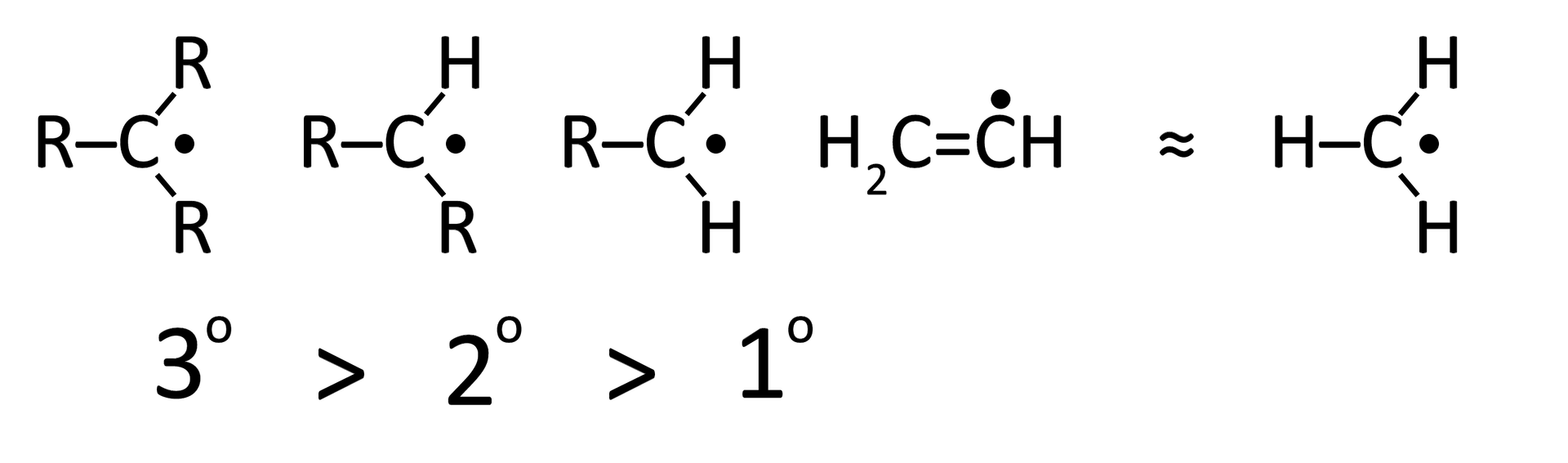O właściwościach i zastosowaniu alkanów
Właściwości fizyczne alkanów
Aby dokładnie poznać właściwości fizyczne alkanów, zapoznaj się z treścią i wykonaj Polecenie 1.
Otrzymywanie metanu oraz sposób jego zbierania.
Problem badawczy
W jaki sposób można zbierać metan powstający w reakcji chemicznej?
Hipoteza
Metan można otrzymać w wyniku reakcji octanu sodu z wodorotlenkiem sodu pod wpływem tlenku wapnia. To gaz o mniejszej gęstości od powietrza i słabo rozpuszczalny w wodzie, dlatego należy go zbierać do probówki lub zlewki napełnionej wodą i odwróconej do góry dnem w naczyniu napełnionym wodą.
Co będzie potrzebne
octanu sodu;
tlenku wapnia;
wodorotlenku sodu;
moździerz;
krystalizator;
dwie probówki;
korek z rurką odprowadzającą;
korek;
statyw;
łapa;
palnik gazowy.
Instrukcja
W moździerzu zmieszano octan sodu, tlenek wapnia i wodorotlenek sodu. Powstałą mieszaninę umieszczono w probówce, zamknięto korkiem z rurką odprowadzającą i umocowano ukośnie w statywie. Drugą probówkę napełniono wodą i umieszczono, odwróconą do góry dnem, w krystalizatorze napełnionym wodą do objętości. Zaczęto ogrzewać probówkę z mieszaniną. Wydzielający gaz zbierano pod wodą do probówki (po ukończeniu zbierania zamknięto probówkę korkiem). Zaobserwowano zachodzące zmiany.
Obserwacje
W wyniku reakcji powstaje bezbarwny, bezwonny gaz, który wypiera wodę z probówki.
Wybrana hipoteza
Metan można otrzymać w wyniku reakcji octanu sodu w wodorotlenkiem sodu, pod wpływem tlenku wapnia. Jest gazem o mniejszej gęstości od powietrza i słabo rozpuszczalny w wodzie, dlatego należy go zbierać do probówki lub zlewki napełnionej wodą i odwróconej do góry dnem w naczyniu napełnionym wodą.
Wnioski
Zebranym gazem jest metan.

Jakie związki chemiczne są potrzebne, aby otrzymać metan?

. Przedstaw dane z tabeli nr 1 w postaci wykresu punktowego, uwzględniając zależność temperatury wrzenia i topnienia alkanów od liczby atomów węgla w ich cząsteczkach. Następnie uzupełnij zdanie.
. Odczytaj w tablicach chemicznych gęstość pierwszych pięciu węglowodorów z szeregu homologicznego alkanów. Następnie uzupełnij zdanie.
Zastanów się i napisz, jaka jest zależność pomiędzy temperaturą wrzenia oraz topnienia i stanem skupienia względem liczby atomów węgla cząsteczkach alkanów.
Podsumowanie właściwości fizycznych alkanów
1. Właściwości fizyczne alkanów o prostych łańcuchach węglowych zmieniają się wraz ze wzrostem liczby atomów węgla w ich cząsteczkach.
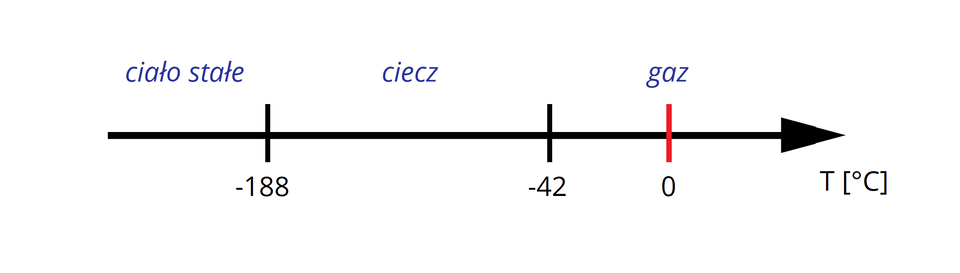
W temperaturze pokojowej alkany o prostych łańcuchach węglowych od metanu do butanu to gazy, od pentanu do heksadekanu to ciecze, natomiast od heptadekanu wszystkie alkany charakteryzują się stałym stanem skupienia.
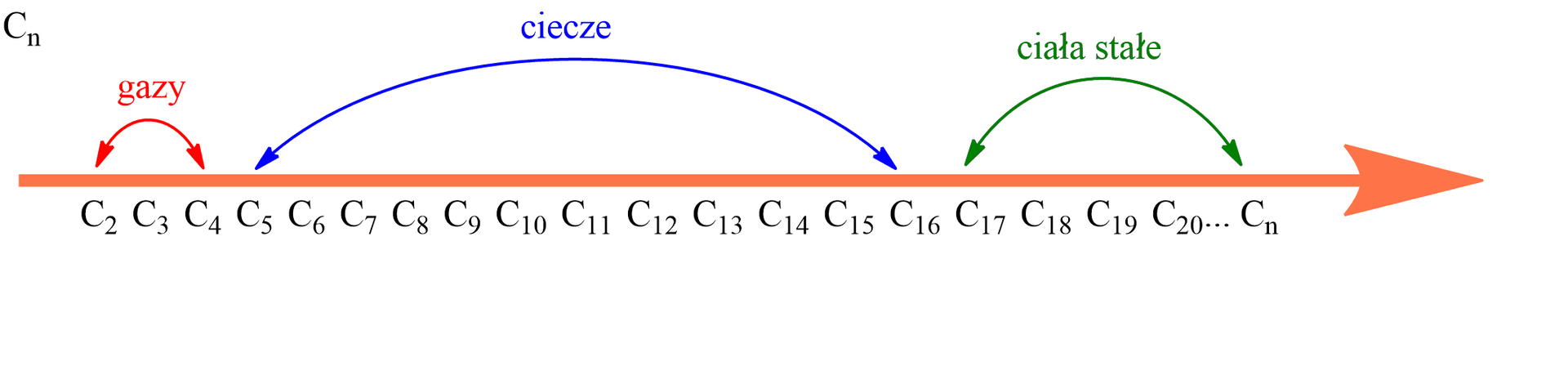
Wraz ze wzrostem liczby atomów węgla rosną zarówno temperatury wrzenia, jak i topnienia alkanów.

Wraz z długością łańcucha węglowego zwiększa się również gęstość alkanów, jednak pozostaje mniejsza od gęstości wody wynoszącej .

2. Alkany są związkami bezbarwnymi, nie rozpuszczają się w wodzie.

Alkany charakteryzują się różnymi wartościami temperatur wrzenia. Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym polegające na zbadaniu temperatur wrzenia wybranych alkanów. Czy długość łańcucha węglowego alkanu ma wpływ na jego temperaturę wrzenia? Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje, a następnie sformułuj wnioski.
Zapoznaj się z opisem doświadczenia zamieszczonym poniżej, a następnie wykonaj polecenia.
Hipoteza:
Im dłuższy łańcuch węglowy alkanu, tym wyższa temperatura wrzenia.
Sprzęt laboratoryjny:
mieszadło magnetyczne z funkcją grzania;
kamyczki wrzenne;
termometr;
kolba okrągłodenna;
chłodnica;
kolba płaskodenna;
cylinder miarowy;
łyżeczka.
statyw.
Odczynniki chemiczne:
pentan;
heksan;
heptan;
oktan;
nonan;
dekan.
Przebieg eksperymentu:
Do kolby okrągłodennej odmierzono za pomocą cylindra miarowego pięćdziesiąt wybranego alkanu. Następnie dodano do kolby kamyczki wrzenne. W kolejnym kroku umieszczono kolbę w płaszczu grzejnym znajdującym się w zamontowanym zestawie. Następnie odkręcono wodę i włączono ogrzewanie kolby. Dalej obserwowano moment, w którym ciecz zaczęła parować, a następnie pary zaczęły się skraplać. Odczytano temperaturę na wyświetlaczu i zanotowano ją.
Obserwacje:
Pentan zaczął wrzeć w temperaturze .
Heksan zaczął wrzeć w temperaturze .
Heptan zaczął wrzeć w temperaturze .
Oktan zaczął wrzeć w temperaturze .
Nonan zaczął wrzeć w temperaturze .
Dekan zaczął wrzeć w temperaturze .
Wyniki:
Im dłuższy łańcuch węglowy alkanu, tym wyższa temperatura wrzenia.
Wnioski:
Hipoteza została potwierdzona.
Właściwości chemiczne alkanów
Reakcją wspólną dla wszystkich alkanów jest reakcja spalania, której najszybciej ulegają, w podwyższonej temperaturze, alkany gazowe. Spalanie może być całkowite lub niecałkowite, co determinuje stężenie tlenu w reakcji.
Do właściwości chemicznych alkanów zaliczamy przede wszystkim ich palność. Wszystkie alkany są palne, a produkty ich spalania zależą od dostępności tlenu. Przy nieograniczonym dostępie powietrza (tlenu) następuje spalanie alkanów do tlenku węgla(). Jest to spalanie całkowite.
Przy ograniczonym dostępie powietrza (tlenu) następuje spalanie węglowodorów do węgla, czyli sadzy. Jest to jeden z typów spalania niecałkowitego.
Możliwe jest również spalanie węglowodorów do tlenku węgla(), czyli czadu. Jest to drugi rodzaj spalania niecałkowitego.
Sprawdź, w jaki sposób metan zachowuje się wobec wody bromowej.
W tym celu wykonaj doświadczenie. Wybierz hipotezę, napisz obserwacje oraz sformułuj odpowiedni wniosek.
Jeśli nie masz możliwości samodzielnego przeprowadzenia doświadczenia, zapoznaj się z poniższym materiałem filmowym obrazującym jego przebieg.
Sprawdzono, w jaki sposób metan zachowuje się wobec wody bromowej.
W tym celu wykonano doświadczenie. Wybierz hipotezę, zapoznaj się z obserwacjami oraz sformułuj odpowiedni wniosek.
Możesz zapoznać się z filmem ukazującym to doświadczenie.
Problem badawczy:
Czy metan powoduje odbarwienie wody bromowej?
Hipoteza:
Metan nie powoduje odbarwienia wody bromowej.
Co będzie potrzebne:
dwie probówki;
korek;
woda bromowa (roztwór bromu);
metan (np. z małej butli).
Instrukcja:
Doświadczenie przeprowadzono pod dygestorium. Do obu probówek wlano do objętości roztwór bromu (wodę bromową). Do jednej z probówek włożono wężyk z metanem i przepuszczono gaz przez roztwór. Zaobserwowano zachodzące zmiany i porównano obie probówki.
Obserwacje:
Brak objawów reakcji./Brak zmian świadczących o przebiegu reakcji./Brunatny (lub pomarańczowy lub żółty) roztwór nie zmienia swojego zabarwienia.
Wniosek:
Metan nie powoduje odbarwienia wody bromowej./Metan nie reaguje z bromem.

Film dostępny pod adresem /preview/resource/R1Pmw7FoxTWhn
W filmie zaprezentowano przebieg doświadczenia, w którym zbadano reaktywność metanu względem wody bromowej. W filmie przedstawiono niezbędne szkło i sprzęt laboratoryjny do przeprowadzenia doświadczenia.
Napisz obserwacje oraz wniosek do przeprowadzonego doświadczenia.
Zastanów się i napisz, w jakiej postaci metan wprowadzany jest do probówki.
Zapoznaj się z mechanizmem substytucji rodnikowej. Zwróć uwagę na nazwy poszczególnych etapów i sposób powstawania rodników.
Czym jest substytucja?
Węglowodory nasycone, w tym alkany, mają zdolność do reakcji substytucji, czyli podstawiania. Reakcja ta polega na wymianie fragmentów cząsteczek, czyli na zastąpieniu atomu w cząsteczce związku chemicznego innym atomem lub grupą atomów, w wyniku czego powstają dwa nowe produkty. Jednym z rodzajów reakcji substytucji, w której biorą udział alkany, jest reakcja halogenowania.
Czy wszystkie halogeny reagują z alkanami?
Fluor z alkanami reaguje wybuchowo bez naświetlania lub ogrzewania. Kontrolowanie procesu jest możliwe po rozcieńczeniu fluoru gazem obojętnym, przez co zmniejsza się ilość reaktywnych rodników.
Najczęściej alkany poddaje się chlorowaniu i bromowaniu (przy czym bromowanie zachodzi wolniej niż chlorowanie).
Reakcja z jodem jest niemożliwa ze względów energetycznych, zatem w praktyce przeprowadza się tylko chlorowanie bądź bromowanie alkanów.
Reaktywność fluorowców w reakcjach z alkanami zmienia się zatem w kolejności: .
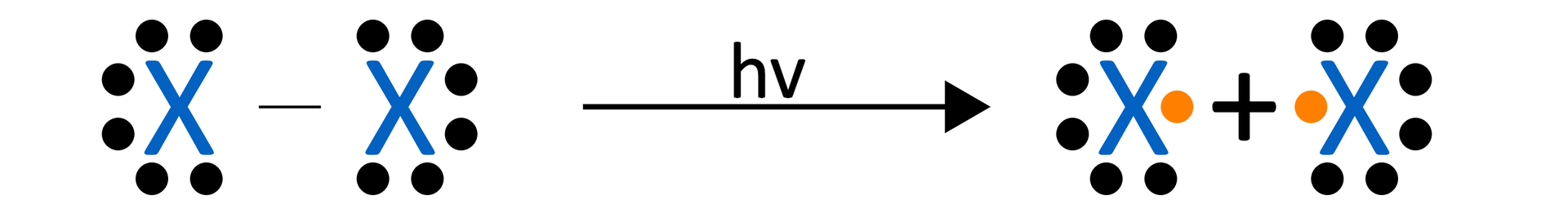
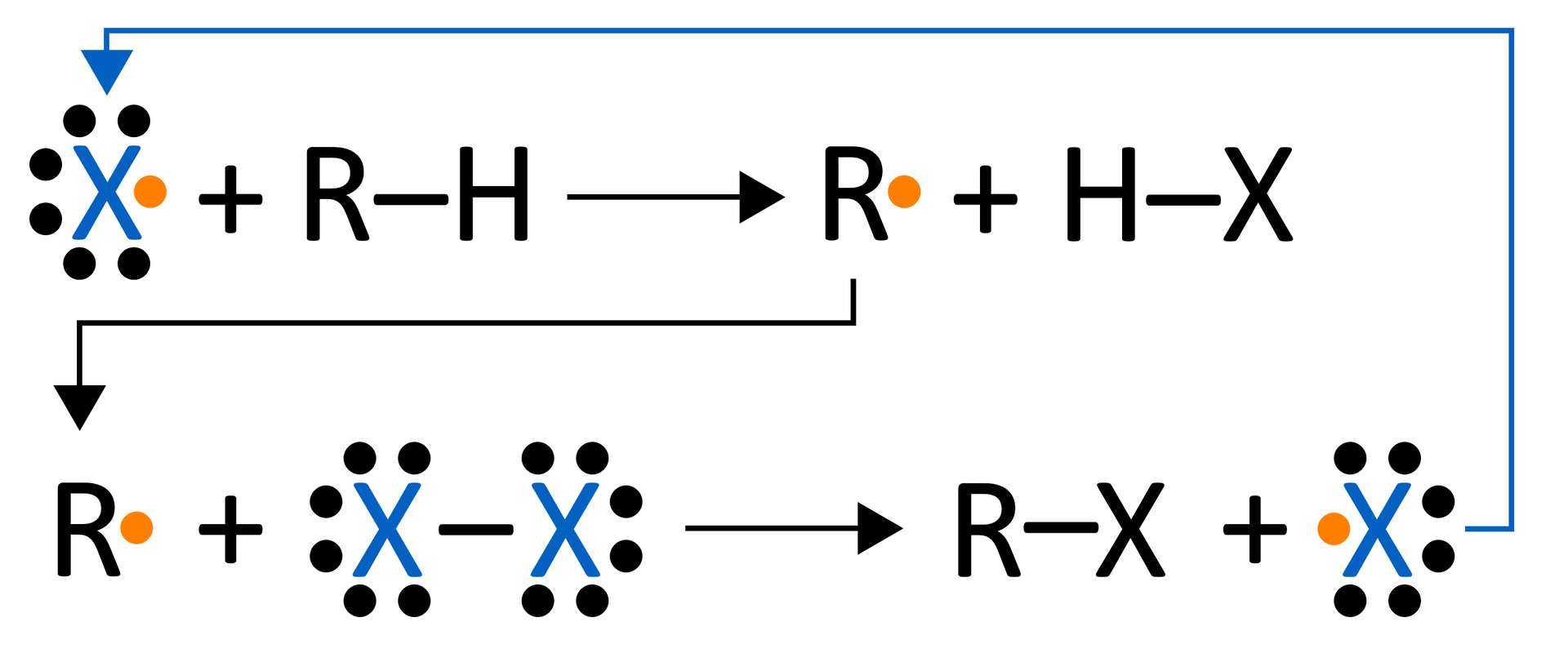
Reakcja halogenowania alkanów przebiega łańcuchowo i składa się z kilku etapów:
Za pomocą symulacji sprawdź, w jaki sposób alkany mogą reagować z chlorowcami. Zwróć uwagę, jakie etapy towarzyszą temu typowi reakcji chemicznej, a następnie rozwiąż ćwiczenia sprawdzające.
Zapoznaj się z opisem symulacji. Dowiesz się, w jaki sposób alkany mogą reagować z chlorowcami. Zwróć uwagę, jakie etapy towarzyszą temu typowi reakcji chemicznej, a następnie rozwiąż ćwiczenia sprawdzające.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DA75SLVB3
Zastosowanie alkanów
Przy pomocy poniższej symulacji interaktywnej sprawdź, gdzie w przemyśle wykorzystuje się alkany. Następnie dopasuj odpowiednie produkty do węglowodorów, z których zostały wyprodukowane. Aby dodatkowo sprawdzić swoją wiedzę dotyczącą wykorzystania alkanów, rozwiąż poniższe ćwiczenia.
Zapoznaj się z poniższą symulacją, z której dowiesz się, gdzie w przemyśle wykorzystuje się alkany. Aby dodatkowo sprawdzić swoją wiedzę dotyczącą wykorzystania alkanów, rozwiąż poniższe ćwiczenia.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DA75SLVB3
Alkany zawierające od pięciu do szesnastu atomów węgla w cząsteczce zaliczane są do węglowodorów ciekłych. Większość z nich stosowana jest jako: Możliwe odpowiedzi: 1. paliwa do pojazdów samochodowych., 2. pasty do podłóg., 3. specjalistyczne smary.
Alkany są ważnymi surowcami w przemyśle chemicznym i głównym składnikiem benzyny i olejów smarowych. Alkany od butanu/etanu/pentanu do oktanu są wysoce lotnymi cieczami i dobrymi rozpuszczalnikami dla substancji niepolarnych. Stosowane są jako sprężony gaz ziemny CNG/smar/paliwo w silnikach spalinowych tzw. benzyna.