Węglowodory nienasycone – alkeny - inne właściwości chemiczne (KMnO4)
Właściwości chemiczne alkenów
Alkeny ulegają także reakcji spalania. Spalanie alkenów zachodzi przy udziale tlenu, a produktami tego procesu, w zależności od ilości dostarczonego tlenu, mogą być:
węgiel (w postaci sadzy) – spalanie niecałkowite;
tlenek węgla() – spalanie niecałkowite;
tlenek węgla() – spalanie całkowite.
Schematycznie proces spalania alkenów można zapisać w postaci równania:
Praktycznym przykładem tego procesu jest spawanie metali, do którego, jako gazu paliwowego, używa się czasami etenu.
Jakie efekty energetyczne towarzyszą reakcji spalania całkowitego etenu?
Na podstawie wartości energii wiązań, można przeprowadzić dla powyższej reakcji obliczenia standardowej entalpii reakcji ().
Typ wiązania | Energia wiązania |
|---|---|
Ponieważ wszystkie wiązania kowalencyjne w cząsteczkach reagentów są zerwane, ilość ciepła wydzielanego w tej reakcji jest związana z siłą tych wiązań (i, oczywiście, siłą wiązań utworzonych w produktach).

Standardowa entalpia reakcji:
Wniosek:
Spalanie alkenów jest procesem egzotermicznym, ponieważ zmiana entalpii reakcji przyjmuje wartość ujemną. Oznacza to, że w trakcie reakcji wydzielają się ogromne ilości energii.
Zapoznaj się z filmem dotyczącym spalania alkenów. Zwróć uwagę na ilość moli tlenu używaną w reakcjach i na rodzaj powstających produktów. Następnie rozwiąż ćwiczenia dołączone do filmu.

Film dostępny pod adresem /preview/resource/R15WTYlXHLqO2
Film nawiązujący do treści materiału dotyczącej spalania alkenów.
Alkeny ulegają także reakcji uwodornienia. Proces ten został opracowany w filmie poniżej.
Czy wiesz, w jaki sposób zachodzi addycja wodoru w obecności katalizatorów? Zapoznaj się z poniższym filmem, a następnie rozwiąż zadania.
Film dostępny pod adresem /preview/resource/R1Wb5Ga8IoxY7
Film nawiązujący do treści materiału
Uzasadnij, w jakim celu stosuje się katalizatory chiralne podczas reakcji addycji wodoru i gdzie mają one zastosowanie.
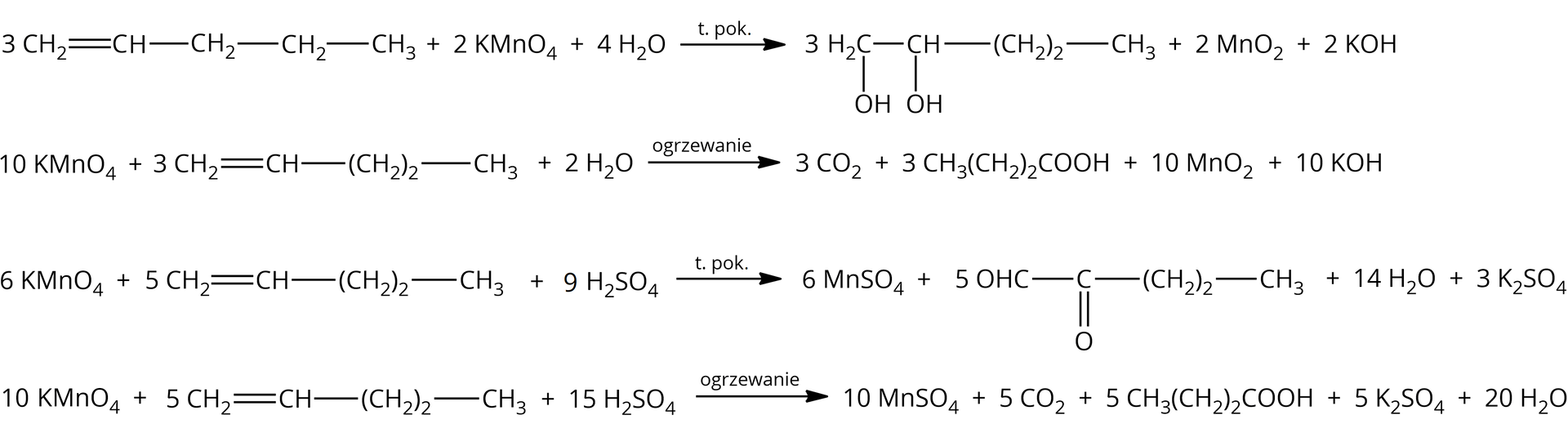
Alkeny wyróżnia również to, iż będą ulegać reakcji utleniania w obecności manganianu(VII) potasu.
„Utlenianie alkenów manganianem() potasu () prowadzi do otrzymania różnych produktów organicznych, co jest zdeterminowane środowiskiem i temperaturą, w której prowadzi się reakcję.”
Indeks górny źródło: Krzeczkowska M., Loch J., Mizera A., Chemia. Repetytorium. Liceum – poziom podstawowy i rozszerzony, Warszawa – Bielsko‑Biała 2010. Indeks górny koniecźródło: Krzeczkowska M., Loch J., Mizera A., Chemia. Repetytorium. Liceum – poziom podstawowy i rozszerzony, Warszawa – Bielsko‑Biała 2010.

Utlenianie alkenów za pomocą w środowisku obojętnym w temperaturze pokojowej i w podwyższonej temperaturze.
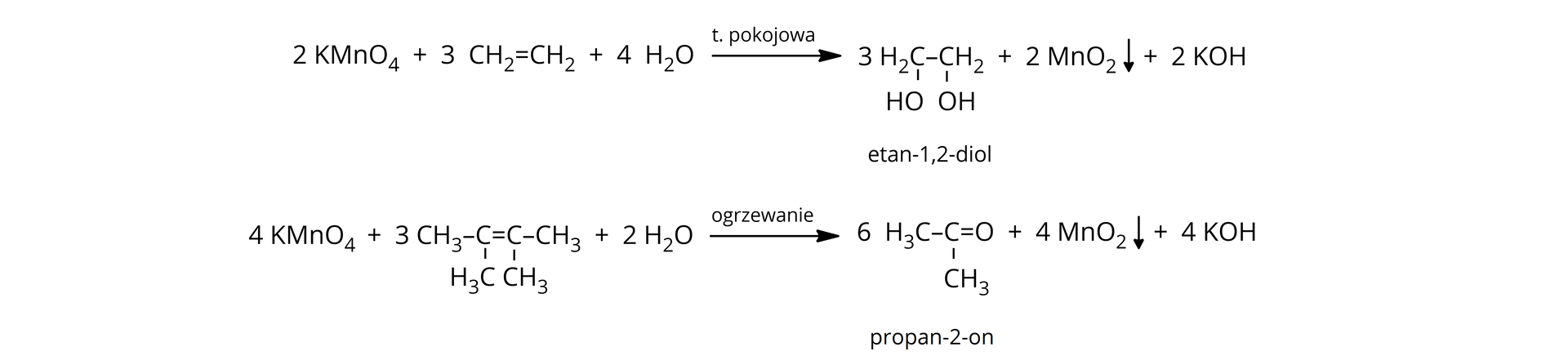
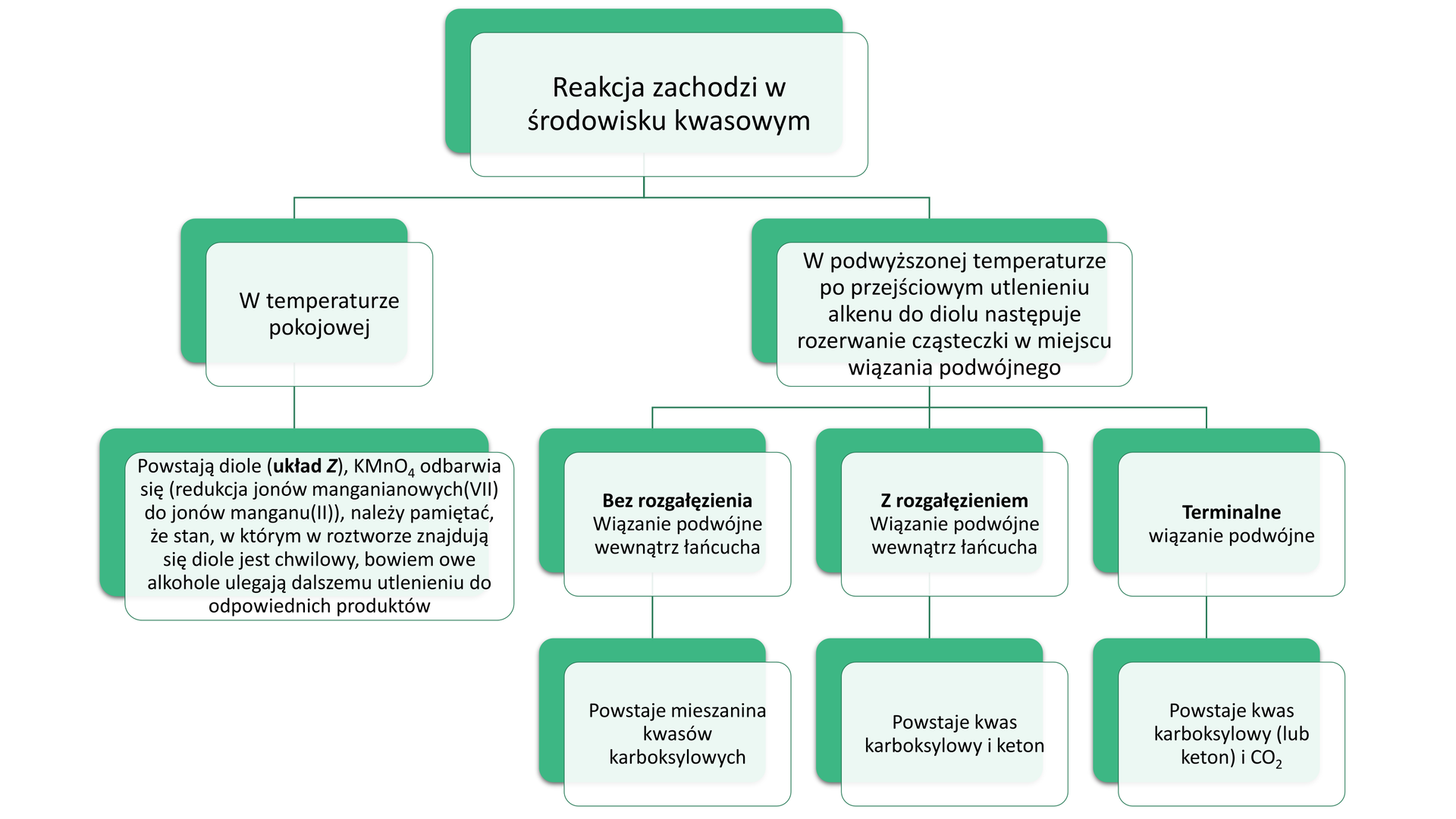
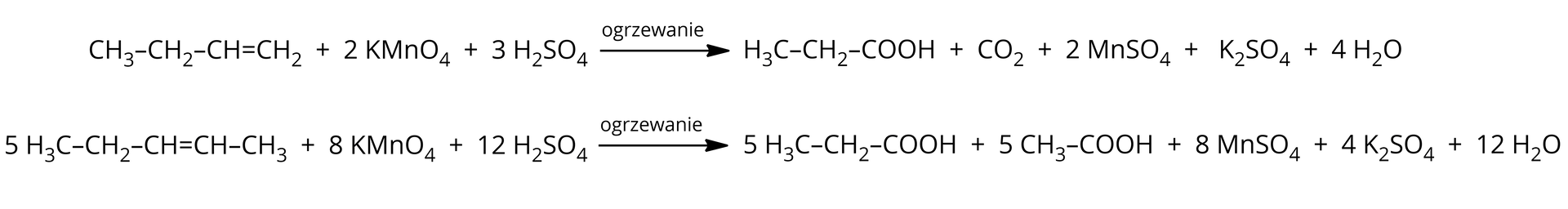
Utlenianie alkenów za pomocą w środowisku kwasowym w podwyższonej temperaturze.
Aby utrwalić zdobytą wiedzę, przeprowadź omówione reakcje utleniania w poniższym laboratorium.
Czy wiesz, jak zachowują się alkeny w obecności wodnego roztworu manganianu() potasu ?
Przeprowadź doświadczenie w laboratorium chemicznym. Sformułuj problem badawczy i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie zapisz wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DEBUXOLBM
Czy wiesz, jak zachowują się alkeny w obecności wodnego roztworu ? Zapoznaj się z poniższym opisem doświadczenia, w którym sformułowano problem badawczy i zweryfikowano hipotezę. W formularzu zanotowano obserwacje i wyniki, a następnie zapisano wnioski. Na podstawie opisu spróbuj przedstawić równania reakcji zachodzących w doświadczeniu.