Budowa i nomenklatura aminokwasów
Budowa aminokwasów
Aminokwasy to związki dwufunkcyjne, które zawierają w swych cząsteczkach grupę karboksylową -COOH oraz grupę aminową -NHIndeks dolny 22. Często są uznawane za pochodne kwasów karboksylowych, w których atom wodoru w grupie węglowodorowej został podstawiony przez grupę aminową. Do aminokwasów zalicza się związki, które zawierają także inne grupy funkcyjne, np. dodatkową grupę aminową lub karboksylową, grupę tiolową lub hydroksylową, układy heterocykliczne czy pierścienie aromatyczne.

R – alifatyczna grupa boczna aminokwasu
Ar – aromatyczna grupa boczna aminokwasu
Występująca w cząsteczce aminokwasu grupa –R, może reprezentować grupę zróżnicowaną pod względem:
kształtu;
wielkości;
ładunku elektrycznego;
reaktywności;
zdolności do tworzenia wiązań wodorowychwiązań wodorowych i oddziaływań hydrofobowych.
Często stosowaną zasadą, określającą wzajemne położenie grupy aminowej i karboksylowej, jest oznaczenie atomów węgla w łańcuchu węglowodorowym kolejnymi literami greckimi: alfa, beta, gamma i delta:
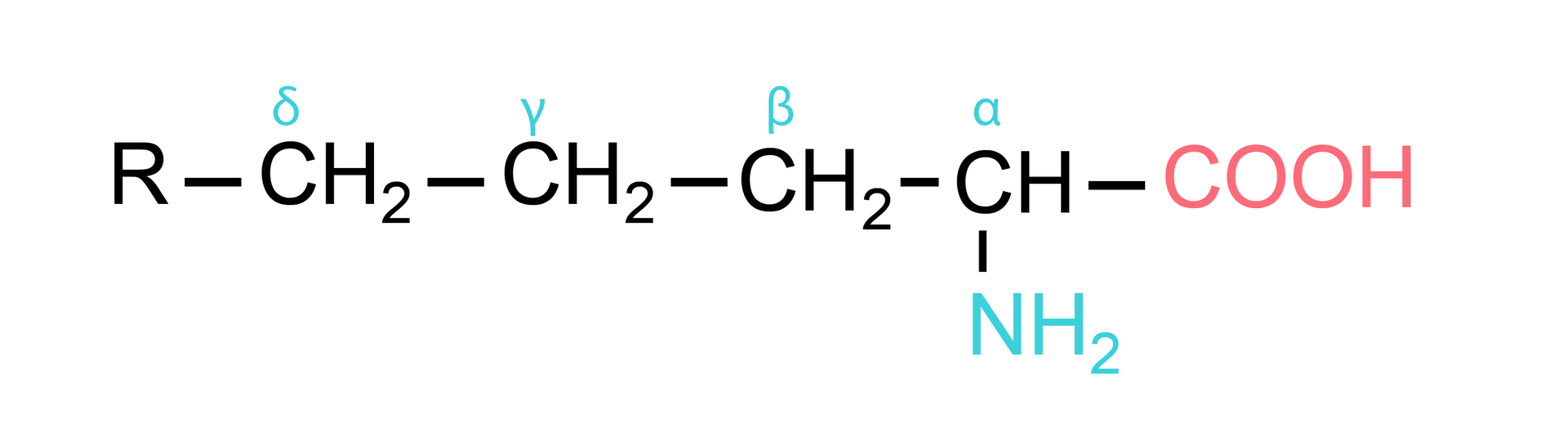
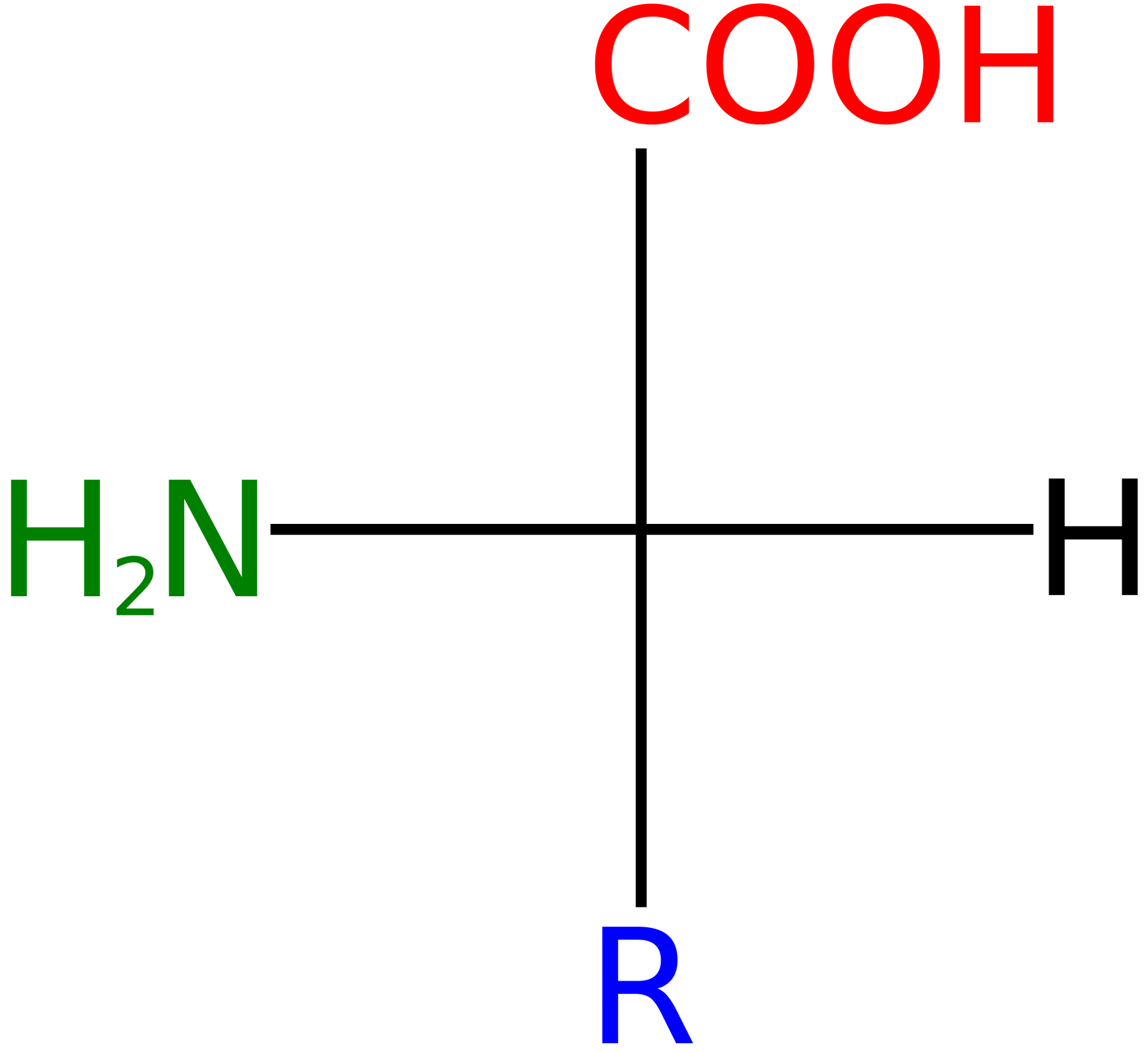
Wszystkie aminokwasy białkowe w organizmie ludzkim (z wyjątkiem glicyny) wykazują czynność optycznączynność optyczną i są alfa-L‑aminokwasami. Oznacza to, że posiadają centrum asymetrii na węglu i należą do szeregu stereochemicznego L, czyli mają grupę aminową po lewej stronie łańcucha głównego w projekcji Fischera. Do ustalenia ich przynależności do szeregu L, jako wzór wybrano L‑serynę.
Nazewnictwo systematyczne aminokwasów
Nazwę systematyczną aminokwasu tworzymy w następujący sposób:
numerujemy atomy węgla, rozpoczynając od atomu węgla grupy karboksylowej,
zapisujemy słowo „kwas”,
dodajemy lokant grupy aminowej i przedrostek „amino–”,
podajemy nazwy pozostałych grup wymienionych w kolejności alfabetycznej,
zapisujemy nazwę kwasu karboksylowego.
Przeanalizuj przedstawioną grafikę i sprawdź nazwę aminokwasu.
Przeanalizuj opis grafiki i sprawdź nazwę aminokwasu.
Poniżej przedstawiono wzory półstrukturalne innych aminokwasów oraz ich nazwy systematyczne.
Zapoznaj się z opisami wzorów półstrukturalnych innych aminokwasów oraz ich nazwami systematycznymi.

Nazewnictwo zwyczajowe aminokwasów
Dopuszcza się stosowanie nazw zwyczajowych. Nazwy alfa‑aminokwasów zgromadzono w tabeli poniżej.
Wzór półstrukturalny | Nazwa systmetyczna | Nazwa zwyczajowa | Trzyliterowy kod | Punkt izoelektryczny |
|---|---|---|---|---|
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas aminooctowy | glicyna | Gly | 5,97 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑aminopropanowy | alanina | Ala | 6,02 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑3‑metylobutanowy | walina | Val | 6,00 |
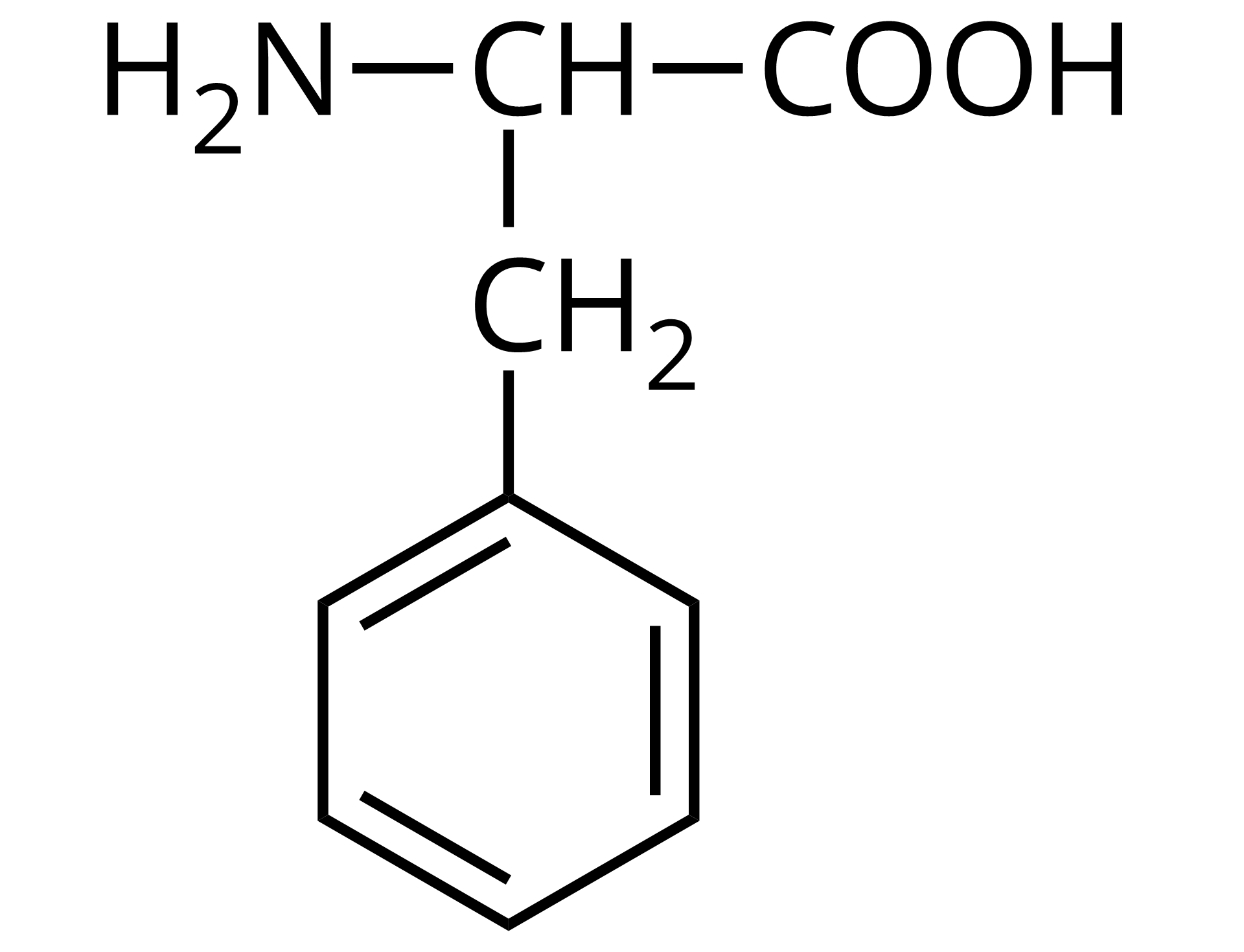 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑3‑fenylopropanowy | fenyloalanina | Phe | 5,48 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑3‑tiolopropanowy | cysteina | Cys | 5,50 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑aminopentanodiowy | kwas glutaminowy | Glu | 3,15 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas‑2,6‑diaminoheksanowy | lizyna | Lys | 9,60 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑aminobutanodiowy | kwas asparaginowy | Asp | 2,85 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑3-(1H-imidazolo‑4- ylo)propanowy | histydyna | His | 7,60 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas (2S,3S)-2‑amino‑3‑metylopentanowy | izoleucyna | Ile | 6,05 |
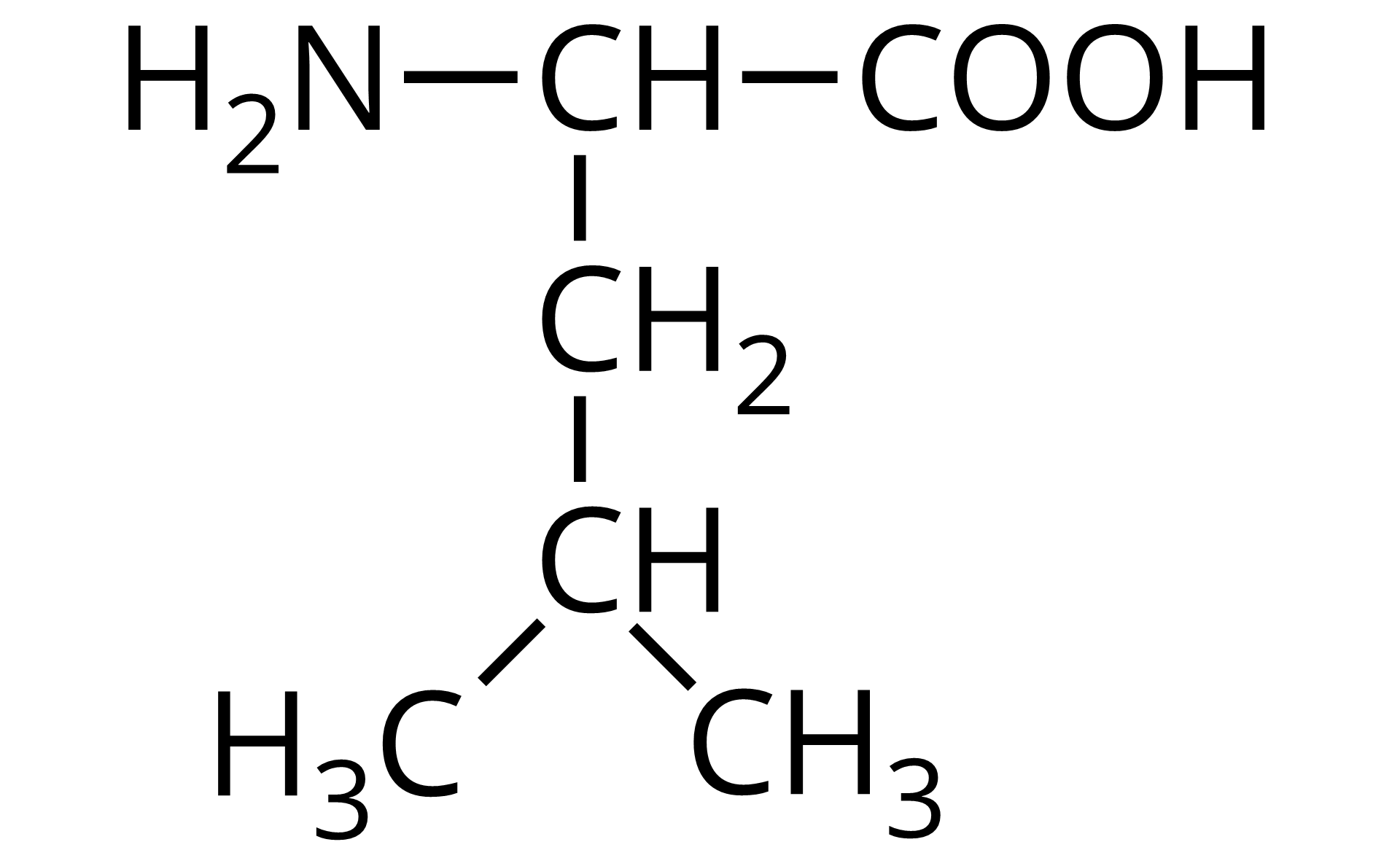 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑4‑metylopentanowy | leucyna | Leu | 6,01 |
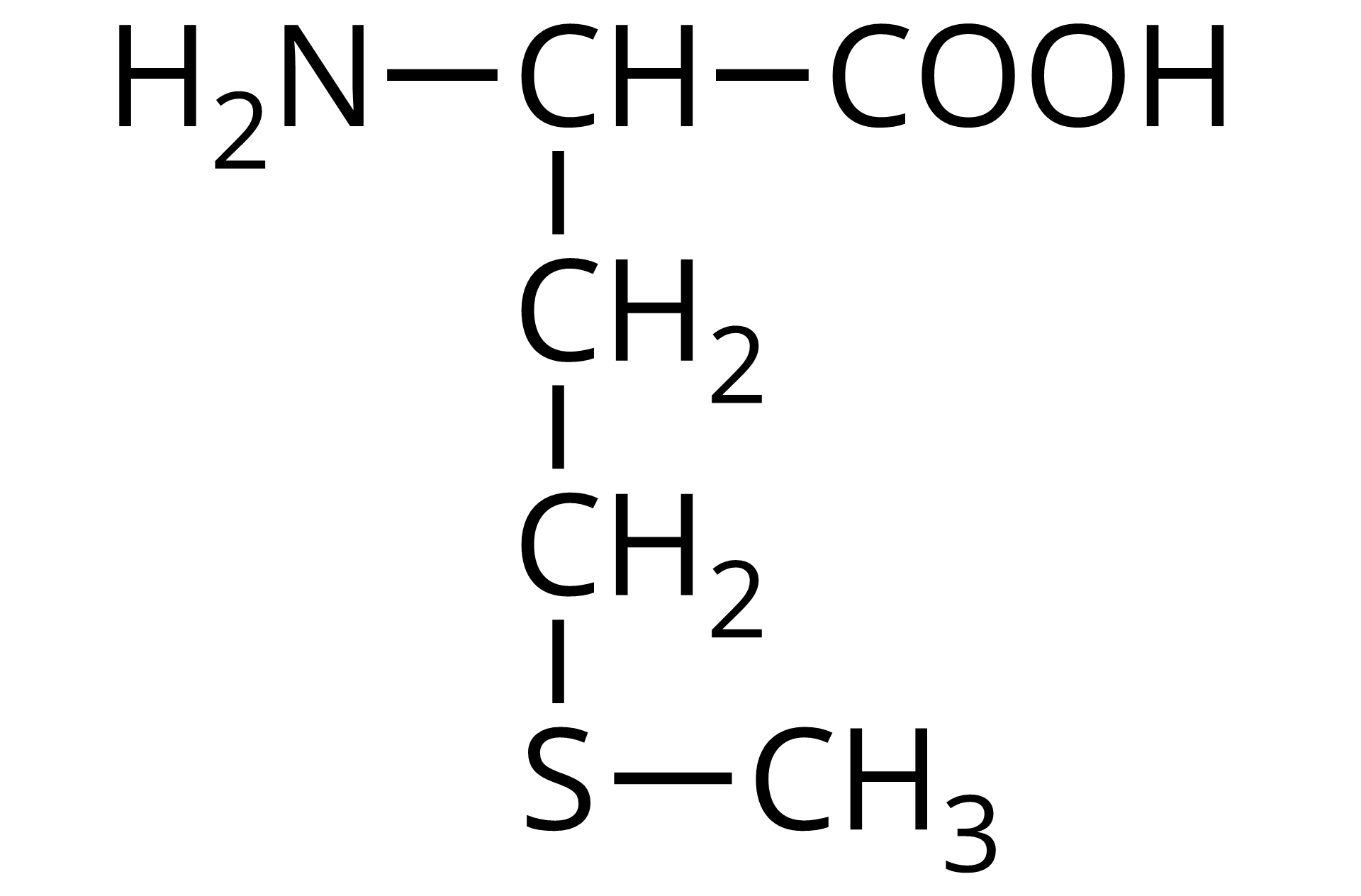 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑4-(metylotio)-butanowy | metionina | Met | 5,74 |
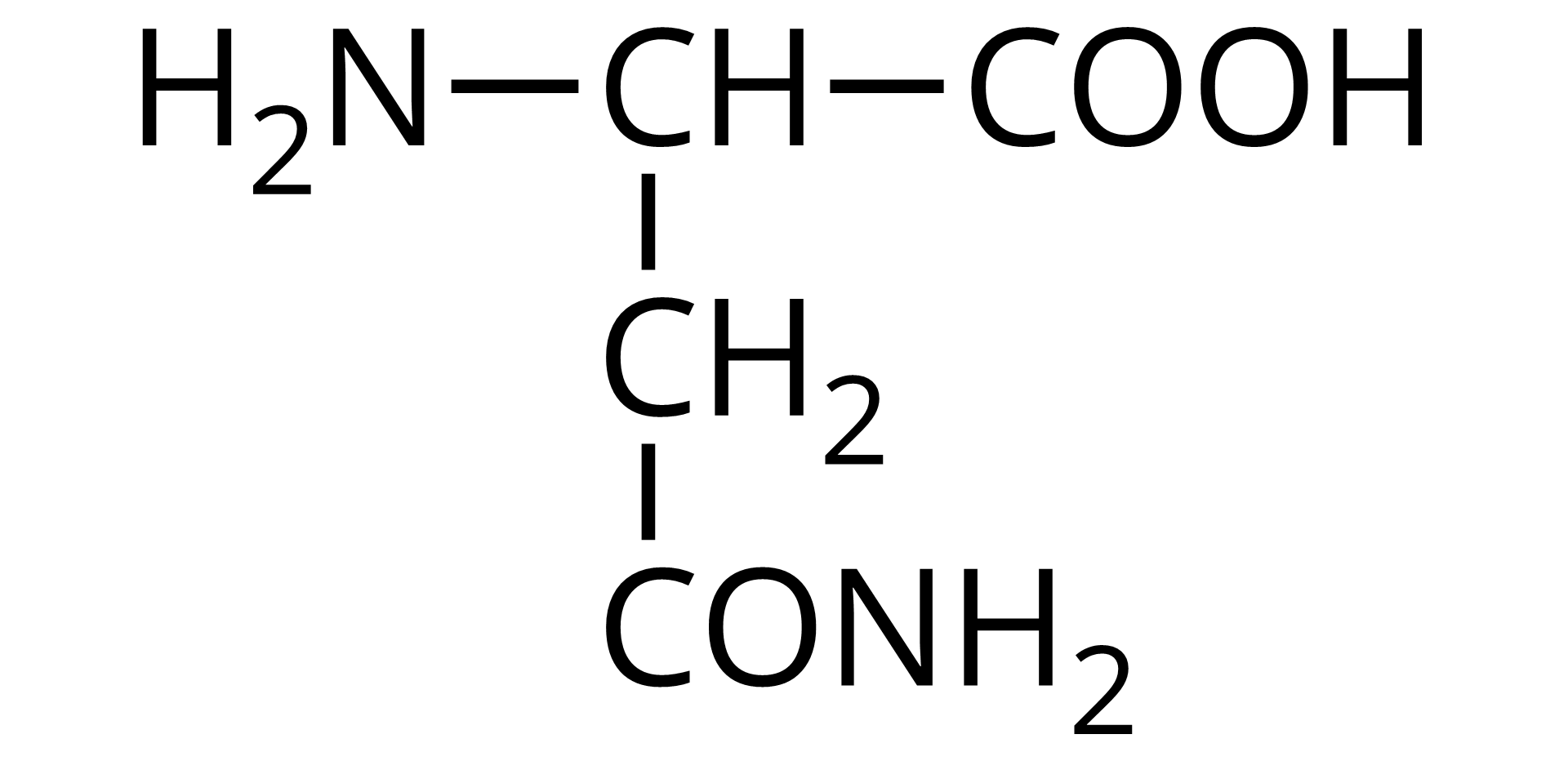 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2,4‑diamino‑4‑oksobutanowy | asparagina | Asn | 5,41 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas pirolidyno‑2‑karboksylowy | prolina | Pro | 6,30 |
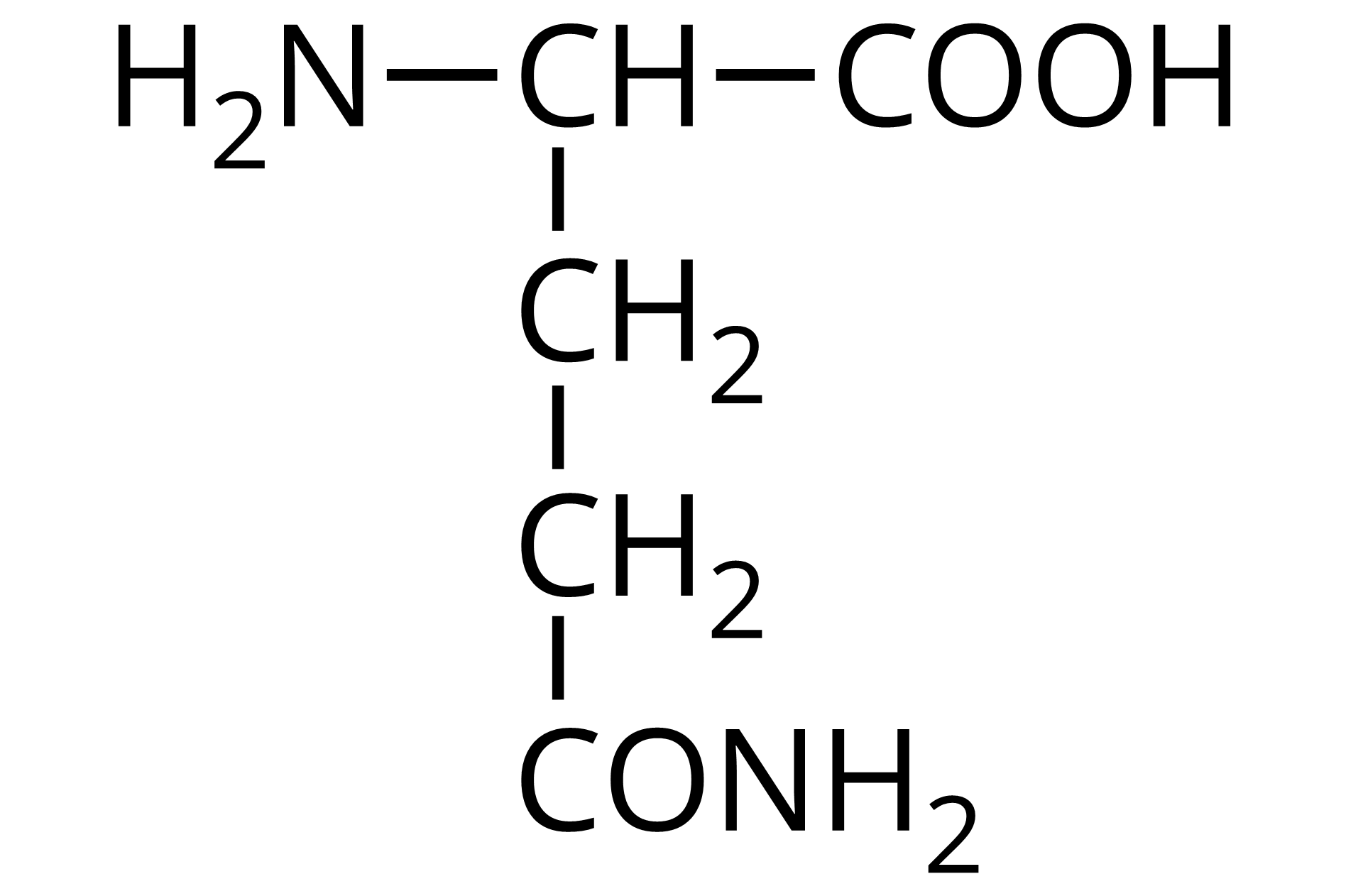 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2,5‑diamino‑5‑oksopentanowy | glutamina | Gln | 5,65 |
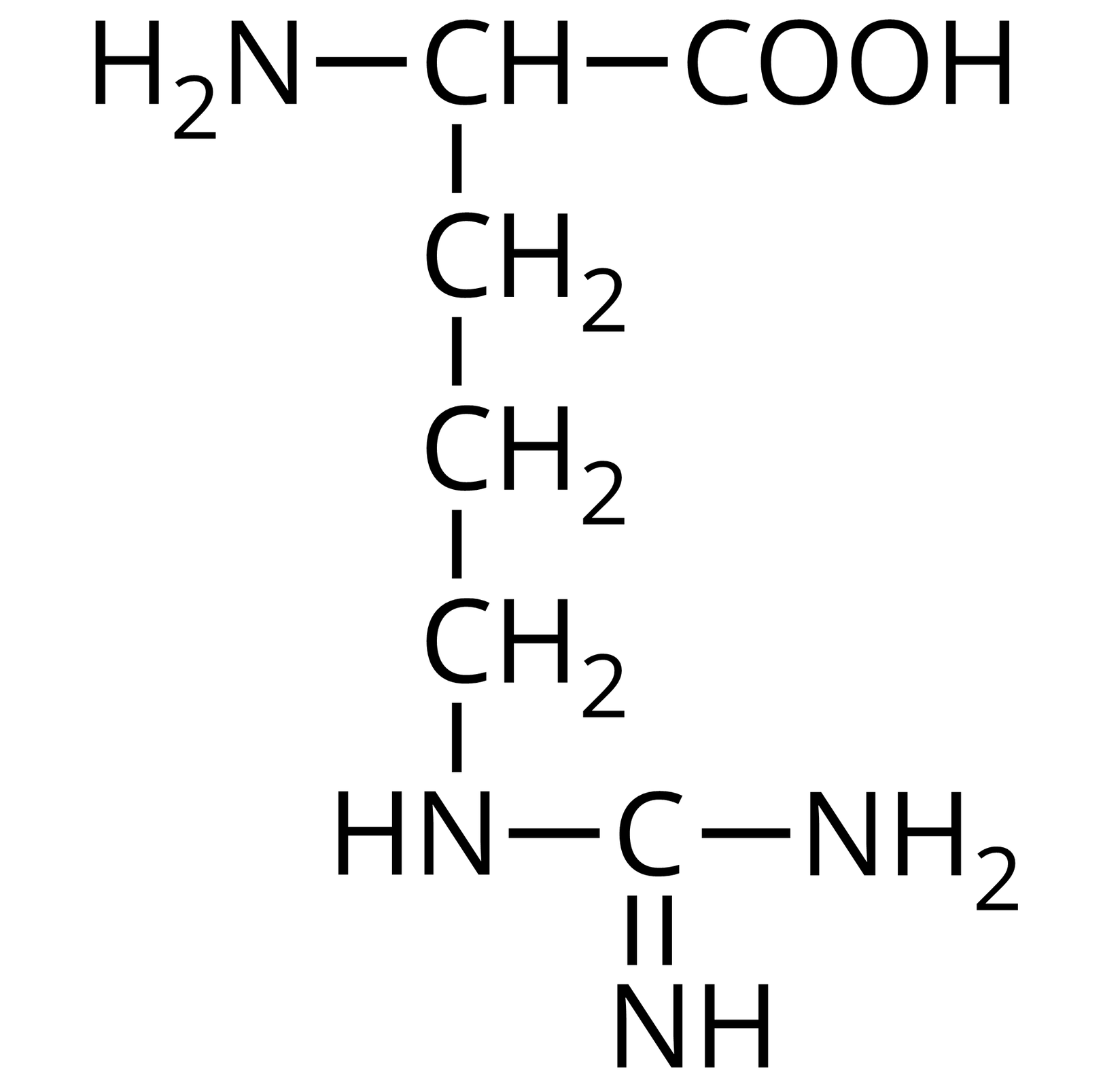 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑5- (karbaimidoamido)pentanowy | arginina | Arg | 10,76 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑3‑hydroksypropanowy | seryna | Ser | 5,68 |
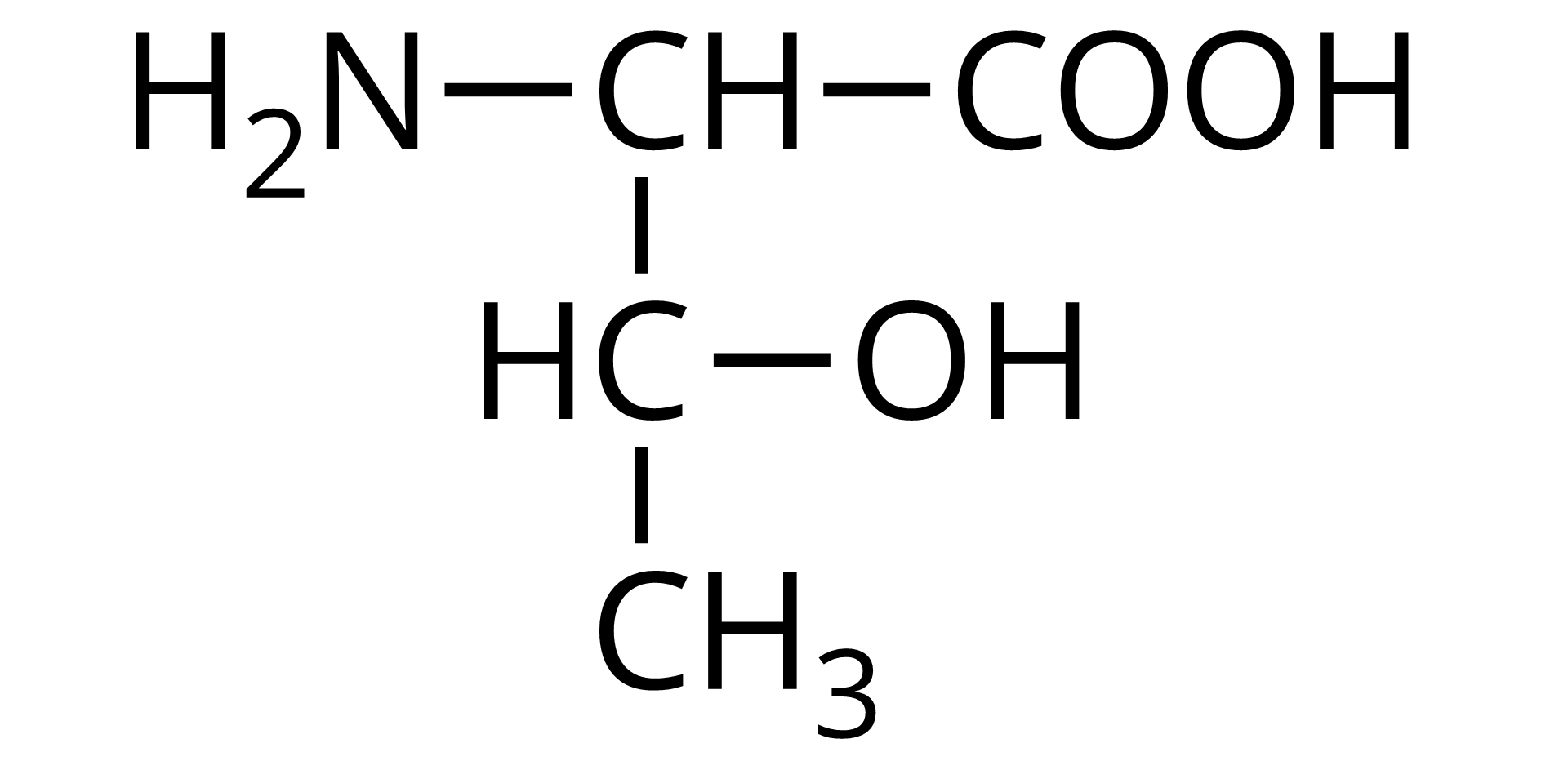 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas (2S,3R)-2‑amino‑3‑hydroksybutanowy | treonina | Thr | 5,60 |
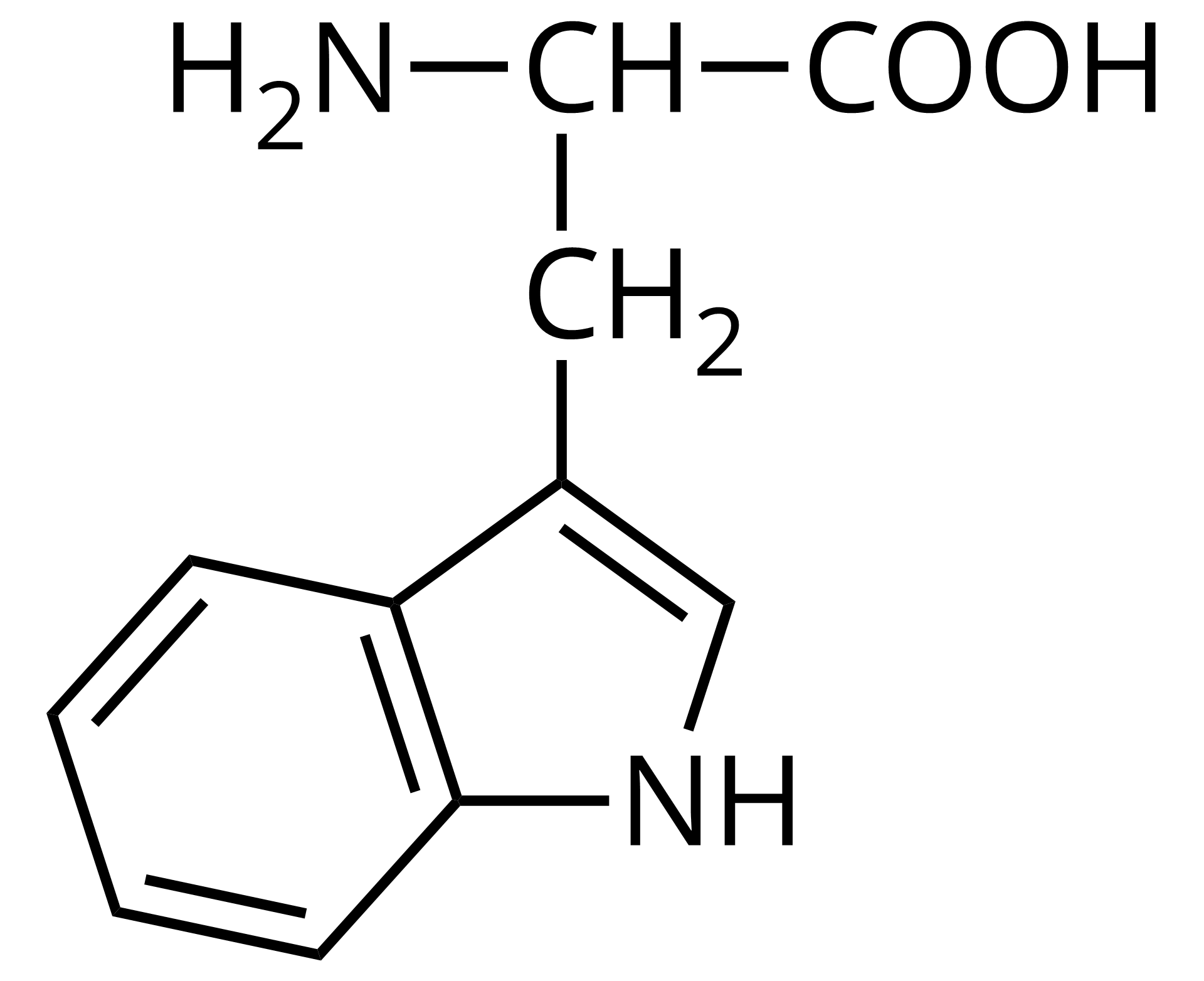 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑3-(1H-indol‑3- ilo)propanowy | tryptofan | Trp | 5,89 |
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas 2‑amino‑3-(4‑hydroksyfenylo)-propanowy | tyrozyna | Tyr | 5,64 |
Nazwa systematyczna:
kwas dwa-aminopropanowy
Wzór sumaryczny: C indeks dolny, trzy, koniec indeksu dolnego, H indeks dolny, siedem, koniec indeksu dolnego, N O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki alaniny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku alaniny jest grupa metylowa C H indeks dolny, trzy, koniec indeksu dolnego., 2. GLICYNA Gly, G
Nazwa systematyczna:
kwas dwa-aminoetanowy
Wzór sumaryczny: C indeks dolny, dwa, koniec indeksu dolnego, H indeks dolny, pięć, koniec indeksu dolnego, N O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki glicyny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego oraz grupa karboksylowa C O O H., 3. IZOLEUCYNA Ile, I
Nazwa systematyczna:
kwas dwa-amino-trzy-metylopentanowy
Wzór sumaryczny: C indeks dolny, sześć, koniec indeksu dolnego, H indeks dolny, trzynaście, koniec indeksu dolnego, N O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki izoleucyny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku izoleucyny jest grupa C H podstawiona grupą metylową C H indeks dolny, trzy, koniec indeksu dolnego oraz grupą etylową C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, trzy, koniec indeksu dolnego., 4. LEUCYNA Leu, L
Nazwa systematyczna:
kwas dwa-amino-cztery-metylopentanowy
Wzór sumaryczny: C indeks dolny, sześć, koniec indeksu dolnego, H indeks dolny, trzynaście, koniec indeksu dolnego, N O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki leucyny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku leucyny jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego połączona z grupą C H podstawioną dwiema grupami metylowymi C H indeks dolny, trzy, koniec indeksu dolnego., 5. PROLINA Pro, P
Nazwa systematyczna:
kwas pirolidyno-dwa-karboksylowy
Wzór sumaryczny: C indeks dolny, pięć, koniec indeksu dolnego, H indeks dolny, dziewięć, koniec indeksu dolnego, N O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki proliny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa karboksylowa C O O H połączona z grupą C H, która wbudowana jest w pięcioczłonowy nasycony pierścień składający się z czterech atomów węgla i jednego atomu azotu. Zatem wspomniana grupa C H z węglem alfa łączy się z grupą N H związaną z grupą metylenową C H indeks dolny, dwa, koniec indeksu dolnego, która to łączy się z kolejną grupą metylenową, ta z następną, która zamyka pierścień wiążąc się z węglem alfa aminokwasu., 6. WALINA Val, V
Nazwa systematyczna:
kwas dwa-amino-trzy-metylobutanowy
Wzór sumaryczny: C indeks dolny, pięć, koniec indeksu dolnego, H indeks dolny, jedenaście, koniec indeksu dolnego, N O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki waliny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku waliny jest grupa C H podstawiona dwiema grupami metylowymi C H indeks dolny, trzy, koniec indeksu dolnego., 7. FENYLOALANINA Phe, F
Nazwa systematyczna:
kwas dwa-amino-trzy-fenylopropanowy
Wzór sumaryczny: C indeks dolny, dziewięć, koniec indeksu dolnego, H indeks dolny, jedenaście, koniec indeksu dolnego, N O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki fenyloalaniny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku fenyloalaniny jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego połączona z pierścieniem fenylowym, to jest sześcioczłonowym pierścieniem aromatycznym., 8. TRYPTOFAN Trp, W
Nazwa systematyczna:
kwas dwa-amino-trzy- indolylopropionowy
Wzór sumaryczny: C indeks dolny, jedenaście, koniec indeksu dolnego, H indeks dolny, dwanaście, koniec indeksu dolnego, N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki tryptofanu. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a niebieskie - azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku tryptofanu jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego połączona z pięcioczłonowym pierścieniem indolu. Strukturę indolu stanowią dwa skondensowane pierścienie aromatyczne posiadające dwa wspólne atomy węgla, to jest atomy mostkowe. Pierwszy pięcioczłonowy pierścień buduje atom węgla związany z jednym z dwóch atomów mostkowych i podstawiony fragmentem zawierającym grupy aminową i karboksylową. Atom ten łączy się dalej w pierścieniu z grupą C H, ta z grupą N H, która to związana jest z drugim atomem mostkowym. Atomy mostkowe łączą się ze sobą, co zamyka pierwszy pierścień. Drugi pierścień jest pierścieniem sześcioczłonowym, do którego należą wspomniane atomy mostkowe., 9. TYROZYNA Tyr, Y
Nazwa systematyczna:
kwas dwa-amino-trzy-(cztery-hydroksyfenylo)propanowy
Wzór sumaryczny: C indeks dolny, dziewięć, koniec indeksu dolnego, H indeks dolny, jedenaście, koniec indeksu dolnego, N O indeks dolny, trzy, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki tyrozyny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku tyrozyny jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego połączona z pierścieniem fenylowym, to jest sześcioczłonowym pierścieniem aromatycznym, który w pozycji czwartej podstawiony jest grupą O H., 10. KWAS ASPARAGINOWY Asp, D
Nazwa systematyczna:
kwas dwa-aminobutanodiowy
Wzór sumaryczny: C indeks dolny, cztery, koniec indeksu dolnego, H indeks dolny, siedem, koniec indeksu dolnego, N O indeks dolny, cztery, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki kwasu asparaginowego. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku kwasu asparaginowego jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego podstawiona grupą karboksylową C O O H., 11. KWAS GLUTAMINOWY Glu, E
Nazwa systematyczna:
kwas dwa-aminopentanodiowy
Wzór sumaryczny: C indeks dolny, pięć, koniec indeksu dolnego, H indeks dolny, dziewięć, koniec indeksu dolnego, N O indeks dolny, cztery, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki kwasu glutaminowego. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku kwasu glutaminowego jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego połączona z drugą grupą metylenową C H indeks dolny, dwa, koniec indeksu dolnego podstawioną grupą karboksylową C O O H., 12. ARGININA Arg, R
Nazwa systematyczna:
kwas dwa-amino-pięć-guanidynopentanowy
Wzór sumaryczny: C indeks dolny, sześć, koniec indeksu dolnego, H indeks dolny, czternaście, koniec indeksu dolnego, N indeks dolny, cztery, koniec indeksu dolnego, O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki argininy. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a niebieskie - azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku argininy są trzy kolejno połączone ze sobą grupy metylenowe C H indeks dolny, dwa, koniec indeksu dolnego, z których ostatnia łączy się z grupą N H związaną z atomem węgla połączonym za pomocą wiązania podwójnego z grupą N H oraz za pomocą wiązania pojedynczego z grupą aminową., 13. HISTYDYNA His, H
Nazwa systematyczna:
kwas dwa-amino-trzy-imidazopropionowy
Wzór sumaryczny: C indeks dolny, sześć, koniec indeksu dolnego, H indeks dolny, dziewięć, koniec indeksu dolnego, N indeks dolny, trzy, koniec indeksu dolnego, O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki histydyny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a niebieskie - azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku histydyny jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego połączona z pięcioczłonowym pierścieniem zbudowanym z atomu węgla połączonego za pomocą wiązania podwójnego z grupą C H związaną z atomem azotu połączonym za pomocą wiązania podwójnego z grupą C H. Grupa ta wiąże się z grupą N H, która to łączy się z atomem węgla, co zamyka pierscień., 14. LIZYNA Lys, K
Nazwa systematyczna:
kwas dwa,sześć-diaminoheksanowy
Wzór sumaryczny: C indeks dolny, sześć, koniec indeksu dolnego, H indeks dolny, czternaście, koniec indeksu dolnego, N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, dwa, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki lizyny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a niebieskie azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku lizyny są cztery kolejno połączone ze sobą grupy metylenowe C H indeks dolny, dwa, koniec indeksu dolnego, z których ostatnia łączy się z grupą aminową N H indeks dolny, dwa, koniec indeksu dolnego., 15. SERYNA Ser, S
Nazwa systematyczna:
kwas dwa-amino-trzy-hydroksypropanowy
Wzór sumaryczny: C indeks dolny, trzy, koniec indeksu dolnego, H indeks dolny, siedem, koniec indeksu dolnego, N O indeks dolny, trzy, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki seryny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku seryny jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego podstawiona grupą hydroksylową O H., 16. TREONINA Thr, T
Nazwa systematyczna:
kwas dwa-amino-trzy-hydroksybutanowy
Wzór sumaryczny: C indeks dolny, cztery, koniec indeksu dolnego, H indeks dolny, dziewięć, koniec indeksu dolnego, N O indeks dolny, trzy, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki treoniny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku treoniny jest grupa C H podstawiona grupą metylową C H indeks dolny, trzy, koniec indeksu dolnego oraz grupą hydroksylową O H., 17. CYSTEINA Cys, C
Nazwa systematyczna:
kwas dwa-amino-trzy-sulfanylopropanowy
Wzór sumaryczny: C indeks dolny, trzy, koniec indeksu dolnego, H indeks dolny, siedem, koniec indeksu dolnego, N O indeks dolny, dwa, koniec indeksu dolnego, S
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki cysteiny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, kulka niebieska odpowiada atomowi azotu, zaś żółta - siarki. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku cysteiny jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego podstawiona grupą tiolową S H., 18. METIONINA Met, M
Nazwa systematyczna:
kwas dwa-amino-cztery-metylotiobutanowy
Wzór sumaryczny: >
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki metioniny. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, kulka niebieska odpowiada atomowi azotu, zaś żółta - siarki. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku metioniny jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego związana z kolejną grupą metylenową podstawioną atomem siarki połączonym z grupą metylową C H indeks dolny, trzy, koniec indeksu dolnego., 19. ASPARAGINA Asn, N
Nazwa systematyczna:
kwas dwa-amino-trzy-amidopropanowy
Wzór sumaryczny: C indeks dolny, cztery, koniec indeksu dolnego, H indeks dolny, osiem, koniec indeksu dolnego, N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, trzy, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki asparaginy. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku asparaginy jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego podstawiona grupą C O N H indeks dolny, dwa, koniec indeksu dolnego., 20. GLUTAMINA Gln, Q
Nazwa systematyczna:
kwas-dwa,pięć-diamino-pięć-oksopentanowy
Wzór sumaryczny: C indeks dolny, pięć, koniec indeksu dolnego, H indeks dolny, dziesięć, koniec indeksu dolnego, N indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, trzy, koniec indeksu dolnego
Ilustracja przedstawiająca model kulkowo‑pręcikowy cząsteczki glutaminy. Kulki czarne reprezentują atomy węgla, białe - atomy wodoru, czerwone - tlenu, a kulka niebieska odpowiada atomowi azotu. Aminokwas stanowi grupa C H, do której przyłączone są grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego, grupa karboksylowa C O O H oraz determinujący omawiany podział łańcuch boczny, którym w przypadku glutaminy jest grupa metylenowa C H indeks dolny, dwa, koniec indeksu dolnego połączona z drugą grupą metylenową C H indeks dolny, dwa, koniec indeksu dolnego podstawioną grupą C O N H indeks dolny, dwa, koniec indeksu dolnego.
Na podstawie powyższych informacji wykonaj Ćwiczenie 1.
Na poniższym rysunku przedstawiono wzór półstrukturalny pewnego aminokwasu. Podaj nazwę zwyczajową tego aminokwasu oraz jego skrót literowy. Zaznacz na rysunku „w kółko” grupy funkcyjne występujące w każdym aminokwasie. Kolorem niebieskim oznacz zasadową grupę funkcyjną, a kolorem czerwonym kwasową.
Wiesz już, jak zbudowane są aminokwasy. Teraz utrwal swoją wiedzę, wykonując symulację oraz analizując grafikę i ćwiczenia dotyczące aminokwasów białkowych zamieszczone poniżej.
Poniższa symulacja przedstawia 20 podstawowych aminokwasów białkowych wraz z ich skrótami jedno- i trójliterowymi oraz wzorami strukturalnymi. Zapoznaj się z propozycją podziału aminokwasów białkowych ze względu na elementy charakterystyczne, które wynikają z ich budowy. Czy zauważasz jeszcze inną możliwość dokonania podziału? Na podstawie symulacji rozwiąż poniższe zadania.
Zapoznaj się z opisem symulacji, a następnie rozwiąż zadania.
Poniższa symulacja przedstawia 20 podstawowych aminokwasów białkowych wraz z ich skrótami trójliterowymi oraz wzorami strukturalnymi. Zapoznaj się z propozycją podziału aminokwasów białkowych ze względu na elementy charakterystyczne, które wynikają z ich budowy. Czy zauważasz jeszcze inną możliwość dokonania podziału? Na podstawie opisu rozwiąż poniższe zadania.
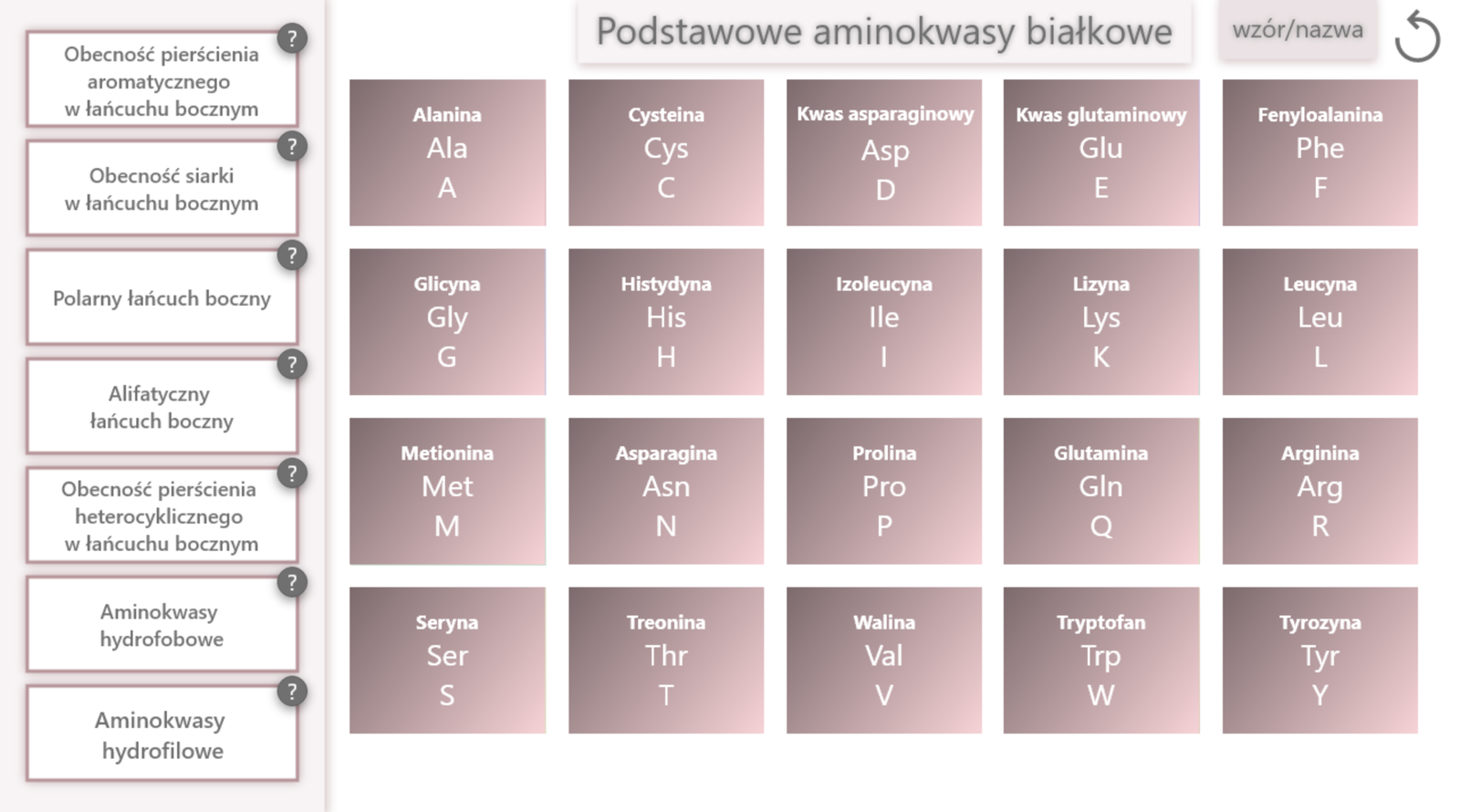
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DDC7CKLHV
Czy znasz klasyfikację aminokwasów białkowych? Zapoznaj się z poniższą grafiką interaktywną, która przedstawia podział aminokwasów białkowych ze względu na polarność łańcucha bocznego, charakter chemiczny, możliwość biosyntezy oraz budowę łańcucha bocznego.
Czy znasz klasyfikację aminokwasów białkowych? Zapoznaj się z opisem grafiki interaktywnej, która przedstawia podział aminokwasów białkowych ze względu na polarność łańcucha bocznego, charakter chemiczny, możliwość biosyntezy oraz budowę łańcucha bocznego.
Nazwy systematyczne aminokwasów:
Wymień aminokwasy, które organizm żywy jest w stanie zsyntetyzować samodzielnie (endogenne).
